
Kaisar
-
Постов
21 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Kaisar
-
-
8 часов назад, M_GM сказал:
Ждал от вас уравнений реакций, но не дождался. А из них очевидно, что n(H2) = n(H2O)
И если вы нашли:
то ясно, что n(H2) = n(H2O) = 0.6 моль
n(СO) = n(газов) - n(H2) = 0.2 моль
Но странно, что у вас с другими исходными данными тоже получилось
n(газов)=0.8 моль. Если это результат округления, то считать следует всё же поточнее,
как правило до трех значащих цифр
Далее надо учесть, что этими газами полностью восстановили 59,2 г смеси оксидов
Пусть одного оксида х моль, другого у моль, составляем систему уравнений, решаем.
А если вместо оксида хрома,будет Fe3O4, количество газов равно 0.656моль и h2o=0.5
Cu2O+H2=Cu+H2O
Cu2O+CO=Cu+CO2
Fe3O4+4CO=3Fe+4CO2
Fe3O4+4H2=3Fe+4H2O
То n(H2)=0.5,n(CO)=0.156?
P.S. в задаче написали 0.0656 моль,но помоему это опечатка
-
Только что, M_GM сказал:
Я тоже так подумал,но посмотрел образец этой задачи и там было написано так:
Только что, Kaisar сказал:И если эту задачу решить методом который вы говорите ,то выходит другой ответ
-
-
Константа диссоциации гидроксида аммония равна 1.8•10-5.Определите массу хлорида аммония,которую необходимо добавить к 500 мл 0.1М раствора гидроксида аммония,чтобы понизить концентрацию OH- ионов в растворе в 50 раз.
-
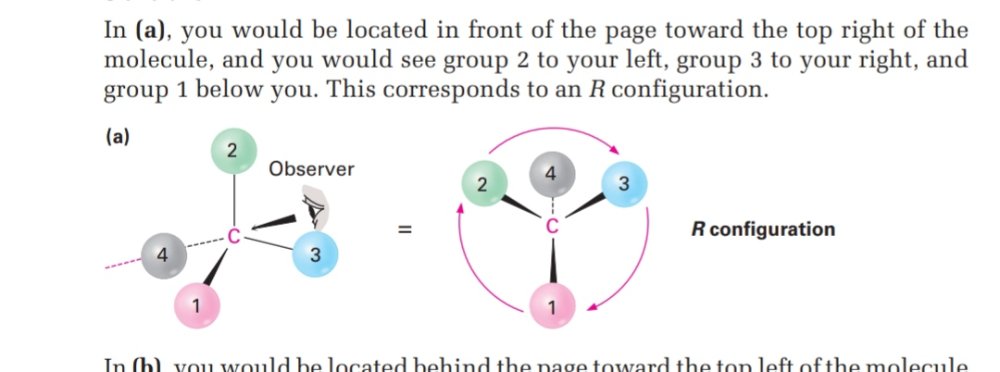
Почему 2 заместитель находится слева ?т.к. если смотреть с верхнего правого угла, то он должен быть на правой стороне,тоже самое и с 3 заместителем

-
Смесь, содержащую оксид фосфора(V) и оксид калия, в которой соотношение числа атомов кислорода к числу атомов фосфора равно 14,5 : 4, сплавили, затем растворили в горячей воде. В результате получили 447,4 г раствора, в котором массовая доля атомов водорода составляет 7,6%. Вычислите массу фосфата калия в полученном растворе.
3K2O+P2O5=2K3PO4
(y+5x)/2x=14.5/4
y=2.25x
Тогда
3K2O+P2O5=2K3PO4
2.25x. x
2.25x 0.75x
0. 0.25x. 1.5x
P2O5+3H2O=2H3PO4
. 0.5х
H3PO4+2K3PO4=3K2HPO4
было: 0.5х. 1.5х
ост: 0 0.5х 1.5х
n(H)=0.076*447.4=34
K2HPO4=n(H)=1.5x
n(H2O)=n(H)/2=(34-1.5x)/2
m(р-р)=m(K3PO4)прореаг.+ m(P2O5)прореаг.+m(H2O)
447.4=212x+0.25x*142+9(34-1.5x)
x=0.6
m(K3PO4)=0.6*0.5*212=63.6г
В ответе вышло 42.4.Где я допустил ошибку?
-
Только что, avg сказал:
нужно знать соотношение
n(C2H5COOH):n(CO2):n(CH3COOH)=1:1:2
-
CH3COC2H5+ KMnO4+H2SO4-> CO2+C2H5COOH+CH3COOH+K2SO4+MnSO4+H2O
MnO4(-)+8H(+)+5e=Mn(2+)+4H2O
C(0)-3e=C(3+)
C(0)-4e=C(4+)
Не смог уравнять.Может C(3+)окисляется до 4+,а С(0) до 2+?
-
Только что, dmr сказал:
Fe2O3+C->Fe
Выделяетя угарный газ или углекислый?
-
-
8 минут назад, avg сказал:
Находите сколько NaOH в 10мл или 11г этого раствора.
.
-
Только что, Kaisar сказал:
Просто не могу понять,зачем нужна плотность
-
Только что, avg сказал:
Это при электролизе NaCl, а далее разлагалась собственно вода. Надо найти количества газов, и насколько уменьшилась масса раствора.
Ну да ,я ее и нашел
1,5у+0,2=0,5
у=0,2 моль
m р-р=150-3,55-0,4-6,4=139,65 г
-
-
в результате электролиза 150 г раствора хлорида натрия с массовой долей соли 7,8% на электродах выделилось 11,2 л газов(н,у,) и образовался раствор с плотностью 1,1 г/мл. Какой максимальный объем (н.у.) оксида углерода 4 прореагирует с 10 мл полученного раствора?
Тут вроде хлорид натрий электролизуется ,а потом вода
2NaCl+2H2O=H2+2NaOH+Cl2
2H2O=2H2+O2
n(NaCl)=150*0,078/58,5=0,2 моль
n=11,2/22,4=0,5 моль
Какой следующий ход решений?
-
22.12.2017 в 23:52, Иван1978 сказал:
тут какая-то нестыковка в задаче
2NaCl + 2H2O = 2NaOH + H2 + Cl2
из 2 моль соли получается 2 моля щелочи и 2 моля смеси газов
а у вас 0.5 моль смеси газов
значит соли тоже 0.5 моль это 29.2 грамма.
а в растворе всего 150*0.078=11.7 грамма соли.
Откуда столько газов взялось?
Можно конечно предположить, что вся соль разложилась, а потом начала разлагаться вода.
Короче, задача длинная выходит 0.173 л углекислого газа.
Как вы получили 0,173 л CO2?
-
-
-
-



Соотношение растворов
в Решение заданий
Опубликовано
В каком соотношении по массе надо смешать 80%-ный раствор серной кислоты и 60%-ный олеум, чтобы получить 5%-ный олеум?
Допустим получилось 100г олеума ,
m(H2SO4)=95г
SO3+H2O=H2SO4
m р-р1=у
m(H2SO4)=0.8y
n(H2O)=0.2y/18≈0.011y
m(SO3)=80•0.011y=0.88y
0.8y+0.88y=95
y=56.54 ,попробовал все подставить и получить соотношение,но у меня немного отличается.Где я ошибся?