
Solovey
-
Постов
317 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Solovey
-
-
А вот хамить то не надо было.
Допущение, что плотности растворов равны 1, ничуть не лучше того, что объёмы суммируются аддитивно, а речь, напомню, шла о молярности, а НЕ о моляльности и НЕ о массовых долях.
-
03.11.2023 в 13:01, A.Schmidt сказал:
Никому не нравится выставлять на показ свои ОШИБКИ...
А это у Вас в какую сторону мысль ломанулась? Что-то я связи не улавливаю.
-
03.11.2023 в 11:35, stearan сказал:
особенно среди особий нежного пола
Вообще неаспопримо!!!
-
03.11.2023 в 11:25, stearan сказал:
не объязательно. энтропийный фактор случайности никто не отменял ?
Дык функция живого как раз таки уменьшать энтропию!
-
 1
1
-
-
Добрый день! Нашел вот такую схему установки для определения гранулометрического состава суспензии. Быть может кто-то знает, где почитать об этом подробнее, с метрическими данными?

-
А откуда 5,1 мл то взялось? Тогда уж от 700 г - 5,1 г. Безумство должно быть последовательным!
-
 1
1
-
-
Именно поэтому я и написал "примем". Точные расчеты могли быть проведены при наличии в условии задачи дополнительных данных. А исходя из того, что есть, только и остается писать "примем". Понятно, что даже без сероводорода объём, в отличие от массы, это не аддитивная величина. Или, быть может, Вы предлагаете от 700 мл отнять 5,1 грамма? Или, еще лучше, 0,15 моль?
-
Количество вещества HCl: 400*1,020----------100 %
Х--------------------4,4 %
Х=17,952 г/36,5 г/моль=0,4918 моль
Сульфида: 0,5 моль/л*0,3 л = 0,15 моль
Na2S+2HCl=H2S+2NaCl
Из 0,15 моль сульфида образуется 0,15 моль H2S и 0,3 моль NaCl
Молярная концентрация: Примем, что объем смеси равен сумме объему исходных растворов: 300+400=700 мл содержит 0,3 моль NaCl
1000 ----------------Х
Х=0,42 М
Давление: по менделклапу: PV=nRT
P= (0.15*8.31*(127+273)) / 4*10-3 = 124650 Па = 124,65 КПа
-
01.11.2023 в 13:10, Solovey сказал:31.10.2023 в 19:54, HE KOT сказал:
V(H2)=0.2*8.314*298/95=5.215941 дм³
Просто Вы спешите НеКот, а вот на олимпиаде это делать категорически не стоит...
-
26.10.2023 в 21:43, HE KOT сказал:
Исходя из этого сделаем вывод о том что при сольватации солей безводных теплота выделяется
а при растворении кристаллогидратов, у которых места для молекул воды уже нет теплота будет выделяться
?
-
https://studopedia.su/3_32895_snoNzh---.html
Там задачка на эту тему разбирается, думаю все понятно станет.
-
25.10.2023 в 01:04, aversun сказал:
Здесь можно целых три уравнения составить
Ну, тогда уж их 6 будет
-
Х=(-1,860*100)/1*0,98=-189,8 Соответствует ФС
-
18.10.2023 в 10:28, Sergus сказал:
не оцеревший
Это без церия?
-
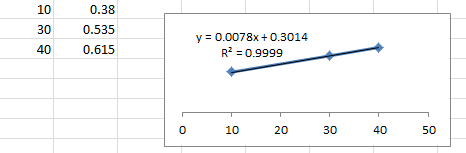
А=Е*L*C А - оптическая плотность, Е - удельный коэф. поглощения, L - длина оптического пути (1 см, если другое не указано в ФС), С концентрация в %.
С=(0,1*2)/(100*100)=2*10-5 г/мл=2*10-3 %
0,546=Е*1*2*10-3
Е=273, по требованиям ФС от 260 до 300, соответствует требованиям ФС
-
-
Нет. Сначала готовите азотную кислоту. 1 часть конц. кислоты, 2 воды. Затем в этой смеси готовите 10% р-р иодата. Р-р кислоты можно взвесить, можно по ареометру или таблицам посмотреть её плотность и пересчитать объём на массу.
-
Да в том то и дело, что это вовсе не дебри. Спектрофотометр вон стоит под рукой. Я на нем делаю измерения, но сравнить не с чем. В местном центре совместного пользования стоит лазерник, не помню как зовут. Но ничего померять на нем мне так ни разу и не смогли. Самого к прибору не пускают по понятным причинам. Так что лазерник это тоже не панацея. Просто успешный тренд
-
-
Для решения этой задачи Вам необходимо знать всего лишь две вещи. Что такое коэффициент молярной экстинкции, и свойства аддитивности оптической плотности.
Первое обычно имеет размерность л/(моль*см) и означает оптическую плотность раствора с концентрацией 1 моль/л, в кювете длиной 1 см. Второе – при наличии нескольких поглощающих соединений общая оптическая плотность будет складываться из оптических плотностей каждого компонента пропорционально их концентрациям и коэффициентам молярной экстинкции. Применительно к Вашей задаче:
Ε=D/(C*L); D=E*L*C, L= 2 см по условию.
D328=ENi(328)*CNi*2+ ECo(328)*CCo*2
D368=ENi(368)*CNi*2+ ECo(368)*CCo*2
Подставляем значения
35210* CNi*2+3910* CCo*2=0,67
21820* CNi*2+14340* CCo*2=0,45
Решаем систему уравнений, откуда Для Ni С= 9,35*10-6 Моль/л, для Со, С=1,47*10-6 Моль/л. По условиям раствор довели до 100 мл, значит никеля и кобальта там будет в 10 раз меньше, чем в литре. Умножив эту величину на атомную массу металлов мы найдем количество граммов в 100 мл, а значит, и в исходной навеске.
0,0532--------------------------------100%
9,35*10-6 /10*58,69 г/моль ----- Х %
1,47*10-6 /10*58,933 г/моль ----- У %
Х=0,103 %, У=0,016%
-
20.09.2023 в 11:18, Alfabel сказал:
Есть проверенный метод и широко представлены приборы (да, лазер) определения размера частиц. Если задача разовая, то проще заплатить и получить достоверный результат.
Вы возможно говорите о модификации Турбидиметрии, определения ряда параметров суспензий с помощью ФЭКа, если да, то нужно углубляться в литературу по этому методу.
Да, о нем, только не с калориметром, а спектрофотометром, впрочем не суть важно. То что удалось найти в нете, очень много противоречивой информации, нет точных данных о концентрации суспензии и её влияния на результате измерений. Нет точного диапазона длин волн, эмпирическая зависимость поглощения от размеров частиц, тоже очень не внятная....
-
К=(Cno)2*CO2/CNo2 =0.24*0.24*0.12/0.06/0.06=1.92
-
-
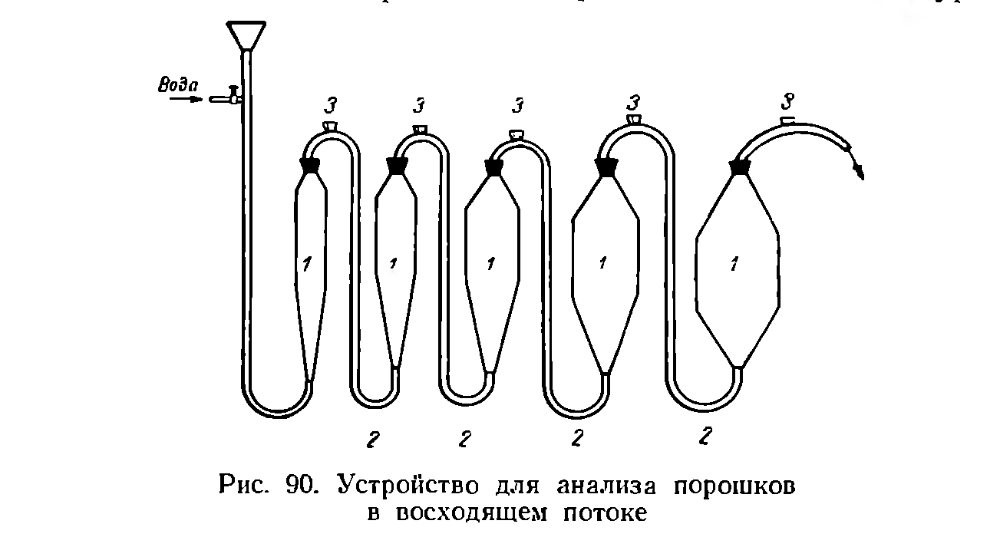
Метод потока для определения гранулометрического состава
в Коллоидная химия
Опубликовано
Ответ очевиден: цена.