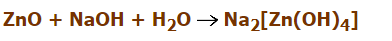Misha20062006
Пользователи-
Постов
35 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Misha20062006
-
Я имею в виду, что в задачах, когда надо найти количество водорода, считают именно так, и это правильно. Я не понимаю почему, разве не было бы логичнее делить на 2, а не умножать? В воде же два атома водорода.
-
Объясните, пожалуйста, МАКСИМАЛЬНО подробно, почему n(H)=2n(H2O).
-
Выбор между CuSO4 и ZnSO4 при реакции с NH3 в растворе
Misha20062006 опубликовал тема в Решение заданий
В двух колбах находились бесцветные растворы веществ X и Y. В обе колбы добавили избыток водного раствора аммиака. В колбе с веществом X осадок сначала выпал, а затем растворился, а в колбе с веществом Y осадок выпал и не растворился в избытке реагента. Из предложенного перечня выберите вещества X и Y, которые обладают описанными свойствами. CuSO4 H2SO4 ZnSO4 Fe2(SO4)3 K2SO4 При решении этого задания у меня возник вопрос, почему правильным ответом считается 34. То есть как вещество X взят именно ZnSO4. Почему не подходит CuSO4. Видел похожую тему на этом форуме, где человек прописал эти реакции. Они идентичны, но тогда почему не подходит CuSO4? > -
Но ведь есть правило обменных реакций, что если при взаимодействии кислоты и соли образуется осадок, то реакция идёт. Почему тут это не работает? Одна из вариаций 6 задания в ЕГЭ по химии из тестовой чати.
-
Здравствуйте, объясните, пожалуйста, почему в этой задаче нельзя взять H3PO4 вместо K3PO4? (Правильный ответ 24)
-
CaO + CO2 = CaCO3 + Q Я решал задание из ЕГЭ на равновесие. Там был вопрос о том, куда сместится равновесие, если добавить аргон (при постоянном объёме). Я думал, раз слева есть газ, то равновесие сместится вправо, ибо если мы добавим ещё газа, пусть и другого, то повысится давление, однако оказалось, что равновесие практически не смещается. Подскажите, пожалуйста, в чём я не прав?
-
На решу ЕГЭ в ответе в первом случае у хрома написано так: 2Cr+6 + 6e → 2Cr+3 А у меди так: Cu+1 - 1e → Cu+2 Вот я немного не понимаю, почему в первом случае умножили на два, а во втором нет. Я могу решать это лично сам, как мне записывать? То есть можно и так записать? Это не будет ошибкой? Cr+6 + 3e → Cr+3 2Cu+1 - 2e → 2Cu+2
-
Почему в реакции 3K2S+K2Cr2O7+7H2SO4=3S+Cr2(SO4)3+4K2SO4+7H2O в электронном балансе написано так: 2Cr+6 > (+6e-) 2Cr+3, а в реакции Cu2O + 3H2SO4 (конц.) = 2CuSO4 + SO2 + 3H2O в электронном балансе написано так Cu+1 > -1e- >Cu+2? То есть почему в первом случае в электронном балансе перед хромом стоит 2, а во втором случае перед медью нет? Во втором случае же тоже медь с индексом 2 слева.
-
Для доказательства наличия хлорид-ионов (Cl-) можно использовать реакцию с агентом, способным образовывать нерастворимое соединение с хлоридами. При добавлении такого агента в раствор с хлоридами, образуется осадок, что служит свидетельством присутствия хлорид-ионов. Один из таких агентов - серебро (Ag+). Когда в раствор Ag+ добавляют раствор хлорида (Cl-), образуется нерастворимый белый осадок хлорида серебра (AgCl): Ag+ + Cl- → AgCl↓ Таким образом, если наблюдается образование белого осадка после добавления раствора серебра в исследуемый раствор, это указывает на наличие хлорид-ионов в исходном растворе. Чтобы обеспечить оптимальные условия для этой реакции, добавляют азотную кислоту (HNO3). Азотная кислота служит для двух целей: Поддерживает кислую среду: Реакция образования осадка хлорида серебра является реакцией осаждения, которая обычно протекает в кислой среде. Азотная кислота, будучи сильным кислотным соединением, обеспечивает кислую среду, необходимую для осаждения хлорида серебра. Устраняет примеси: Азотная кислота также выполняет роль окислителя, который окисляет примеси, такие как ионы и серосодержащие соединения, в более реакционноспособные формы. Это позволяет избежать возможных побочных реакций или интерференции с осаждением хлорида серебра. Таким образом, добавление азотной кислоты вместе с раствором серебра позволяет обеспечить оптимальные условия для доказательства наличия хлорид-ионов путем образования нерастворимого хлорида серебра в кислой среде.
- 2 ответа
-
- 1
-

-
У всех ли атомов в молекулах есть имеется гибридизация? Например, в CaO?
-
Спасибо, а можете объяснить, почему в реакции 2FeCl3 + SO2 + 2H2O -> 2FeCl2 + 2HCl + H2SO4 получается FeCl2, а не FeSO4?
-
2FeCl3 + 3Na2S -> 2FeS + S + 6NaCl Почему в этой реакции получается FeS + S+ NaCl, а не, например, FeCl2 + S + NaCl?
-
1. Na[Al(OH)4] + H2S (изб.) -> Al(OH)3 + NaHS + H2O 2. Na2[Zn(OH)4] + 3H2S (изб.) -> ZnS + 2NaHS + 4H2O Почему в первой реакции получается Al(OH)3, а во второй ZnS? Объясните, пожалуйста.
-
Почему Au(OH)3 обладает слабоксилотными свойствами, а не основными?
-
Газовая смесь состоит из NO и СО2. Вычислить объемное содержание газов в смеси (в %), если их парциальные давления равны соответственно 36,3 и 70,4 кПа (272 и 528мм. рт. ст.). Ответ: 34,02%NO; 65,98%CO, так как мы сложили парциальной давление одного со вторым, разделили каждое давление на общее и умножили на 100%. Это понятно. Я не понимаю другого. Мы же нашли давление в процентах, а объём обратно пропорционален давлению. Следовательно, должно быть наоборот. Т.е. 34,02%CO; 65,98%NO Разве не так? Объясните, пожалуйста
-
NaOH | Разложение под действием электрического тока
Misha20062006 опубликовал тема в Решение заданий
В ОГЭ есть реакция NaOH > Эл. ток. Na + O2 + H2O Типа получается так, что NaOH распадается на Na2O и H2O, а потом Na2O распадается на Na и O2. Я же верно понимаю логику такой реакции? -
-
Насколько я знаю, оксид цинка амфотерный и с водой не реагирует. Однако есть вот такая реакция. Получается, что тут он всё-таки реагирует с водой и получается Zn(OH)2, а после уже он смешивается с NaOH и получается комплексная соль. Всё так или я чего-то не понимаю?
-
Почему Fe + Cl2 = FeCl3, но, например, HCl + Fe = FeCl2 + H2? Почему в одном случае железо окисляется сильнее, чем в другом? Ведь что там хлор, что тут. Объясните, пожалуйста.
-
-
А при каких условиях оксид алюминия будет реагировать с водородом?
-
Везде пишут, что водород реагирует с оксидами металлов, но на решу огэ H2 не будет правильным ответом на вещества реагирующие с Al2O3. Получается, есть какие-то исключения? Объсните, пожалуйста.
-
Почему оксид меди (2) реагирует с водородом, но не реагирует с азотом? Какое свойство тут надо знать?
-
Большое спасибо!! Вы очень помогли! У меня остался последний вопрос. Насколько я знаю, CO2 - кислотный оксид, но я посмотрел в интернете и там говорится, что реакция CuO + CO2 не идёт. Но почему, если кислотный и основный оксид должны реагировать и образовывать соль?