Vladlenin
Пользователи-
Постов
298 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Vladlenin
-
О, а вот это уже даже со слов хорошо звучит, нужно посмотреть
-
Ну теперь остаётся найти её, но это мелочь... Хорошо, лучше даже так сформировать вопрос, по каким вы книгам учулись, когда были в вузах, или может быть кто нибудь знает по каким сейчас книгам преподают в вузах?
-
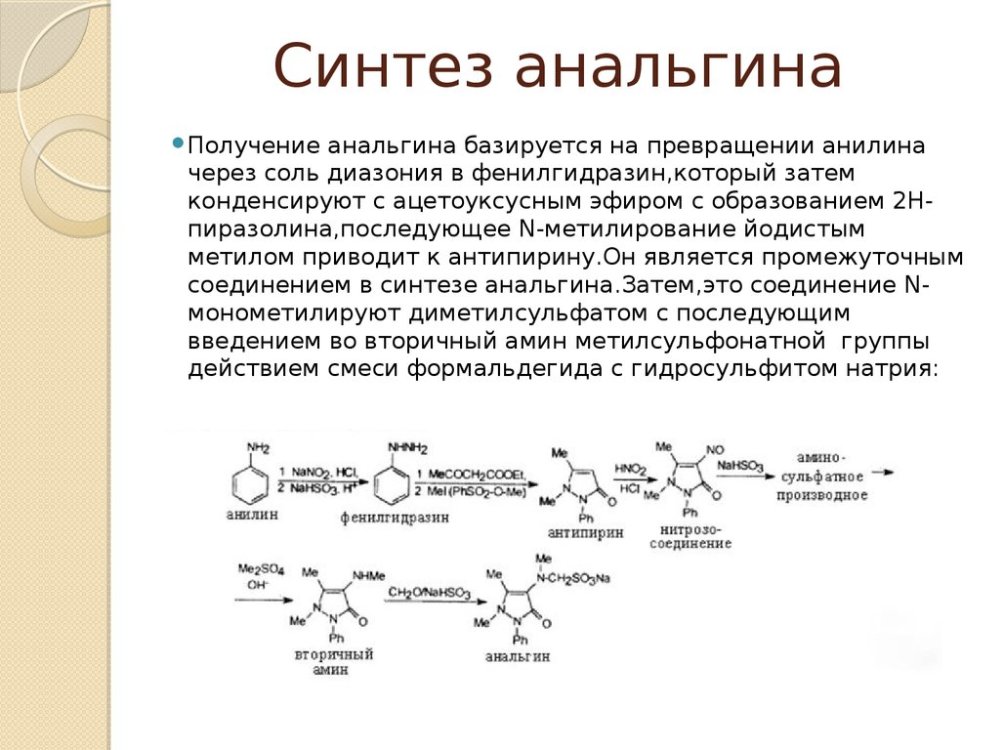
Я конечно понимаю, чтобы написать и описать каждую реакцию, потребуется как минимум не одна книжка, но я бы хочу иметь Хотя-бы олимпиадные знания. Я даже не знаю, наверное, "базовых" реакциих. Например, что амины при взаимодействии с nano3+hcl+nahso4 в H+среде дают гидразины. Вот чтобы такие реакции понять, почитав учебник А, если что, то я пытался так искать, но очень много ЕГЭшных сайтов
-
Здравствуйте дорогие химики, хотел бы найти для себя литературу, где про все органические соединения рассказывают, но не книги 10-11 класса, а что-ли вузовские. Чтобы реакции были типо таких
-
А, то есть это так работает, понял Ещё один вопрос, если я так понял, то чем выше растворимость в-ваш в растворитель, тем быстрее его кристаллизация так? Т.е если взять вещество с большей растворимостью чем у ацетата, то оно быстрее кристаллизуется чем ацетат, так?
-
Все из курса химии знают/видели что при опускании чего либо в перенасыщенный раствор ацетатаX, происходит такой опыт как "тёплый лёд", он происходит из-за кристаллизации вещества с точкой кристаллизации. Так вот, если провести такой же опыт с тем же nacl, то ничего не получится, получается у веществ есть своя "константа кристаллизации?". В чем вопрос - где найти эту таблицу и как называется эта постоянная?
-
Кто знает реакцию окисления мочевины марганцовкой? Напишите пожалуйста с коофицентами её.
-
Читал на форуме что получение из батареек, диоксида марганца очень трудное дело, но так не понял почему Разве нельзя просто взять всю эту черную субстанция и просто сжечь, углерод будет взаимодействовать с кислородом, появится co2/co и учетит, оксид марганца останется?
-
А ну т.е это вещество теоретически существует, но оно нигде не применяется, а эта реакция создана чисто чтобы была, так? (ну, а ещё ПО тестить)
-
Вот есть знаменитая, наверное, реакция 312(Cr(N2H4CO)6)4(Cr(CN)6)3 + 11354KMnO4 + 14847H2S2O7 → 1092K2Cr2O7 + 11354MnSO4 + 1008C13H10 + 10296N2O5 + 4585K2S4O6 + 24783H2O Она знаменита, то что дул много коойицентов, но меня интересует что это за окисляемое вещество? Узнал что его название гексациано-хром (II) гексамочевины-хрома (III) Но также меня интересует, зачем оно, существует оно и зачем оно надо?
-
Так т.е, считаем массу раствора который остался : 47+21.2-46.9432=21.2568+50=71.2568-4.5901=66.6667 Если что то m(BaCO3) :0.0233*197=4.5901 Wna2co3=1.325/66.6667=0.0198 Wnaoh=2.864/66.6667=0.04296
-
А, точно, ну короч, во втором задании полностью оплошал, ну да, нужно будет пересчитать это
-
В растворе будет одно вещество, т.к карбонат бария - осадок, а вот про дополнительную воду от раствора гидроксида бария - ты прав, не учёл. Насчёт газа - это я для точности делал.
-
Приготовленный при растворении 21,2 г карбоната натрия в воде при температуре 80оС насыщенный раствор охладили до 20оС. Выпавший осадок декагидрата карбоната натрия отфильтровали, высушили и обработали избытком хлороводородной кислоты. К фильтрату прилили 50 г раствора с массовой долей гидроксида бария 8%. Растворимость карбоната натрия составляет 45,1 г / 100 г Н2О при 80оС и 21,8 г / 100 г Н2О при 20оС. 1) Какой объём (н.у.) газа выделился при обработке осадка кислотой? 2) Рассчитайте массовую долю вещества в растворе после обработки фильтрата щёлочью Р(Na2Co3 при 80*)=45.1/145.1=0.3108 P(na2co3 при 20*)=21.8/121.8=0.1789 W(Na2Co3 в кристаллогидрате) =106/286=0.3706 P(na2co3 при 80*)=21.2/x+21.2=0.3108 X=47г ->h2o P(na2co3 при 20*)=21.2-0.3706x/68.2-x=0.1789 X=46.9432 ->кристаллогидрат Дальше ищу сколько осталось в растворе m(Na2Co3)=46.9432*0.3706=17.3971 Т. Е 21.2-17.3971=3.8029г na2co3 в растворе осталось m(H2O)=68.2-46.9432-3.8029=17.4539 Na2CO3+Ba(OH)2->BaCO3+2NaOH n(Na2CO3)=3.8029/106=0.0358 m(Ba(OH)2)=50/100*8=4 n(Ba(OH)2)=4/171=0.0233 n(Na2CO3)осталось в растворе =0.0358-0.0233=0.0125 m(Na2CO3)ост=0.0125*106=1.325 W(Na2CO3)=1.325/17.4539+1.325=0.0705 Сколько CO2 выделилось? Масса кристаллогидрат а выпавшего =46.9432 m(Na2Co3) =46.9432*0.3706=17.3971 Na2CO3+2HCl->NaCl+H2O+CO2 n(Na2CO3)=17.3971/106=0.1641 n(Na2CO3)=n(CO2) V(CO2)=0.1641*22.4=3.6758л
-
Опечатка, солянка(соляная кислота, hcl)
-
Из 209,6 г смеси углекислого аммония, железоаммонийных квасцов и кислого углекислого натрия выделили 15,68 л углекислого газа (н.у.) и 18,24 л. (н.у.) аммиака. С помощью каких реактивов это сделали? Запишите уравнения реакций. Определите массовые доли веществ в исходной смеси. Я представил что сначала мы все это дело поливает naoh, а потом добавляем hcl, в результате мы получаем из (Nh4)2CO3->1xCO2+2xNH3 FeNH4(SO4)2->1yNH3 NaHCO3->1zCO2 Записываю имеющиеся формулы X+z=0.7 2x+y=0.8142(я сразу перевёл литры в моли) 96x+265y+84z=209.6 Привожу последнее к 1 переменной 96x+265(0.8142-2x)+84(0.7-x)=256 Считаю..... X=125411моль Ищу z 0.7-0.125411=0.574589 Ищу y 0.8142-0.250822=0.563378 Дальше нахожу массу всех веществ и их процентное соотношение Правильно ли я решил?
-
Ну вот +-я так и думал, ну и с последним я согласен, сделал пост чисто на то "а вдруг" Ну подведу, частота нужна для того чтобы мелкий слой хорошо "реагировал" А Медь, графит и алюминий нужны чтобы это частоты вызывать, так?
-
Объясните пожалуйста простым языком что тут написано :В качестве источника высокой частоты для частиц, употребляемых в реакторах, могут применяться закалочные индукционные генераторы с частотой 300 - 500 кгц. Для получения режима кипения слоя при высокочастотном способе нагрева частиц необходимо применять материалы с малой магнитной проницаемостью. Применение ферромагнитных материалов исключено, так как в этом случае частицы располагаются по магнитным силовым линиям. Как показали наши исследования, могут применяться медь, алюминий, графит.(https://www.ngpedia.ru/id639999p3.html) Так вот 1)Что это за реактор? 2)Зачем там частота? 3)Где именно и почему именно используется Медь, алюминий, графит?
-
Появился недавно гидроперит, вот и подумал провести пару опытов, марганцовка и аспирин - банально, хочу что нибудь эдакого. Увидел на форуме что гидроперит можно растолоч смешать с железной стружкой и вроде как поджечь/ударить и будет взрыв. 1)правильно ли я описал проходимость реакции? 2)Кто знает ещё какие нить опыты (главное эффектные или нестандартные) с гидроперитом?
-
Ну хорошо, спасибо
-
Аааа, так это не так уж и сложно.... Я то думал, от души, но все-же, я уже загорелся этим уравнением, есть какой нибудь материал про него?
-
Решал задачи, наткнулся на вот такую про электронейтральности, так как я не вкурсе что это и с чем это едят не решил, посмотрел в ответы - не помогло :Судя по условию задачи, при взаимодействии MoO3 с аммиаком образуется соль состава (NH4)xMoyO4x. Запишем уравнение электронейтральности: x + 6y = 8x → 6y = 7x. Наименьшим из решений является пара x = 6, y = 7 и тогда H – (NH4)6Mo7O24 Так вот, объясните как они это получили и подкиньте материала, чтобы понять эти уравнения
-
Хм им, спасибо, сейчас времени нет, но позже посмотрю С книгами немного напряг, но попытаюсь найти, спасибо
-
Хм, да мне и немного нужно, просто посмотреть порадоваться и забыть, а как я уже сказал, во всех ближайших ко мне автомагазинах электролит не продаётся, ну ладно, получется как получется
-
ООО, спасибо за информацию, понял, ну надо попробовать