-
Постов
59 -
Зарегистрирован
-
Посещение
Посетители профиля
Блок последних пользователей отключён и не показывается другим пользователям.
Достижения Alex021
-
проведите свой
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
это дегидрированный Дохренища HCl осталось в пробирке. Потом долго содой гасил. В пропорциях было слишком много солянки. Я так понял что часть солянки CaCl2 все таки обзвожил, но высвобожденный HCl просто повысил концентрацию остальной солянки в пробирке (судя по нагреву). Чуть-чуть вышло в воздух. И то наверное из-за повышения концентрации HCl в солянке. Были еще пузырьки, но не факт что это HCl, а не воздух, затесавшийся между гранулами CaCl2. Цель была - выяснить отнимает ли CaCl2 воду у солянки. Цель достигнута - выяснил - отнимает. Все остальное - различные косяки процесса. Небыло времени заморочиться. Еще с серной кислотой не попробовал.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Поглядел. Реакция идет. 1/3 пробирки сухой CaCl2 + 1/3 пробирки солянка 14%. индикаторная бумажка в верхней части пробирки показала pH=0...2 там как-то пятнами и влага заблестела на бумажке, хотя ставил сухую. Пробирка ощутимо нагрелась. Вышло конечно HCl кот наплакал, но я и не делал какую-то пропорцию, так, на глазок закинул.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
ставки делали на то что пойдет или не пойдет. А точные замеры... ХЗ, может смесь неделю будет идти к своему насыщению.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Ну тут уже ставки пошли. На пару пробирок можно пожертвовать реактивов чтобы выяснить кто же прав.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Я тут посмотрел краткий химический справочник Рабиновича 1978 года, и вот что нашел: Таблица играет против вашей ставки. Доберусь до реактивов - проверю.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
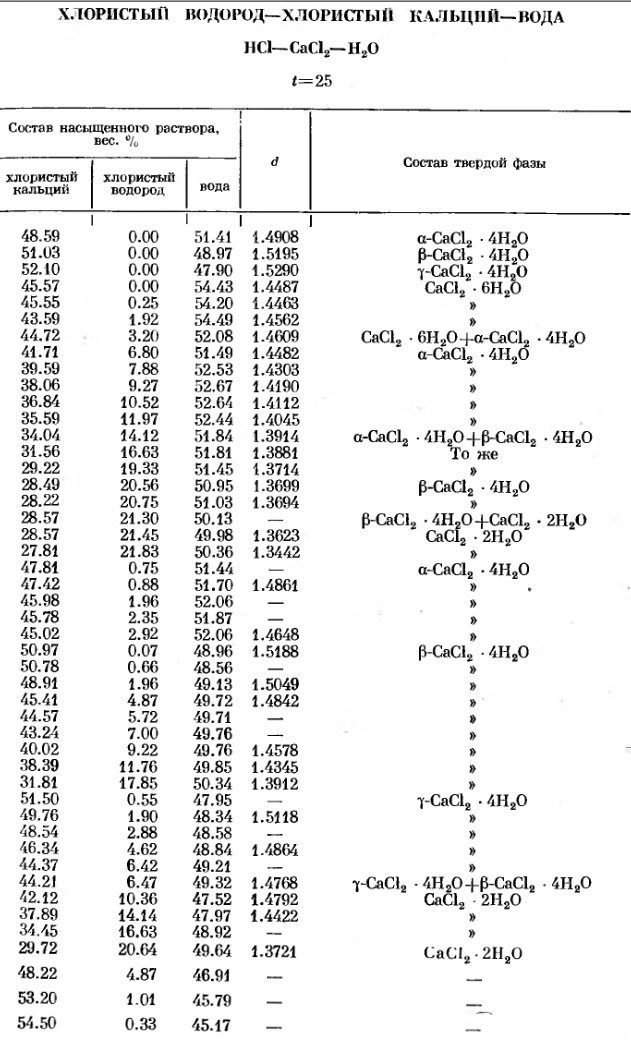
вот таблица для +25С А почему именно хлорида кальция, а не хлороводорода? Насколько я понимаю - речь идет о насыщенном растворе. Справа указан состав только твердого осадка. Если чего-то не хватает, то раствор ненасыщенный и по-возможности будет стремиться к насыщению, вытесняя лишнее. Может я не правильно понимаю? Объясните пожалуйста как правильно понимать таблицу? То есть если я в солянку добавлю хлорид кальция, то хлороводород не полетит? Или надо наоборот солянку капать на сухой хлорид кальция? Нет реактивов под рукой чтобы прям сейчас взять пробирку и попробовать
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Он уже показал что и где искать. Нашел. Изучаю.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Вот такая табличка №1020 есть в справочнике по растворам Т3,кн.1 стр.561 Здесь только вершинка таблицы поместилась. Правда я не понимаю что здесь означает параметр "d" Спасибо chemister2010, показал где искать. В ближайшем будущем буду проверять эти таблицы на практике.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Огонь! Правда с Гуглом пришлось попыхтеть. Нашел такой ресурс https://makston-engineering.ru/perevedennye-materialy#3r Скачал справочники и энциклопедии - столько всего интересного! Никак оторваться не могу. H2SO4 - H2O - HCl таблицы для разных температур! Поищу и CaCl2 - H2O - HCl, о которых спорят знатоки.
- 92 ответа
-
- 1
-

-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Где добыть такой справочник по растворимости ? Выходит что до 73.7% серную можно разбавлять без существенных потерь HCl.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
По осушению хлористым кальцием вот такая штука смущает: 2HCl + 2CaCl2 → 3Cl2 + 2HCa То есть хлороводород еще будет реагировать с хлористым кальцием, выделяя ненужный хлор ?
- 92 ответа
-
- 1
-

-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
Ваша правда. Озон на эту страничку не выводит. Ценник конечно конский. По ГОСТ 4204-77 это 93,6%...95,6% Упариванием (на шлифах: колба→большой_сухопарник→Вюрц→Либих→алонж) из 5л 44% (840руб) с учётом потерь получим 1,35 литра 93%. Конечно не такой чистой, как по ГОСТ. Но можно и перегнать.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
я покопал на озоне. не нашел.
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )
-
дайте ссылку
- 92 ответа
-
- серная кислота
- водоотнимание
- (и ещё 2 )