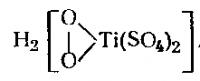-
Постов
602 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент mastersam
-
Его самого
-
Заходим по адресу %HOMEPATH%\Application Data\CMedia (Так и набираем в строке адреса, ничего не изменяя) Открываем какой-то .dat (вроде cmedia.dat) В последней строке устанавливаем 0 вместо стоящего числа Запускаем деинсталлятор (вроде uninstall.exe) Живем без данной рекламы....Я написал бы это раньше, но реклама пошла у меня только через сутки(почти не пользуюсь компьютером)
-
Эта вырезка из лицензионного соглашения. Так что написавший эту программу - не создатель вирусов
-
Ну, насчёт реакции с водой дело идёт примерно так: щелочные и щелочно-земельные металлы являются более сильным основанием, чем Н+,ОН- является кислотой(вероятно слабой). Значит происходит банальное замещение слабого основания более сильным. У меня так это описано... Гидроксиды, образующиеся при присоединении воды к оксидам вышеупомянутых металлов, растворимы, значит идёт постоянное образование щёлочи. Менее активные металлы образуют нерастворимые в воде оксиды и гидроксиды. Металлы пассивируются...
-
пропан + аль(альдегид)--->пропаналь \ C=O - кетонная группа ---> соединения с этой группой - кетоны / ди(2)метил(CH3)кетон(CO) пропан +ол(спирт)--->пропанол метан(CH4)+ол--->метанол(CH3OH) ; ди(2)этиловый(CH3CH2+)эфир(-O-) тоже и с метиловым эфиром этановой кислоты: CH3COOH - этановая(уксусная кислота) CH3OH - метиловый(спирт) CH3COOCH3 - метиловым(CH3) эфиром(-O-) этановой кислоты(CH3COO) И про пропановую кислоту:у неё 3 атома углерода, нет непредельных связей....А ну ка какой предельный углеводород имеет 3 атома углерода? -это пропан, значит и кислота пропановая
-
Многие соли олова подвергаются гидролизу. Судя по таблицам растворимости(1), единственная соль олова(2), не подвергающаяся такому сильному гидролизу - сульфат олова. 1.У меня 3 или 4 таблицы растворимости и во всех разные данные! Например, в 2 из 4 указывается, что CuCO3 не растворим в воде, в других - гидролиз. Но они сходятся в одном: SnSO4 растворим, по поводу остальных солей они друг другу противоречат. 2.Единственная из солей, указанных в таблице т.е из Sn(OH)2 SnF2 SnCl2 SnBr2 SnI2 SnS SnSO3 SnSO4 Sn(NO3)2 Sn(NO2)2 Sn3(PO4)2 SnCO3 Sn(CH3COO)2 SnSiO3
-
.....!@!!@(&($^%#!~...................
-
Можно прокаливать на открытом огне - и получить горящие пары ацетона, которые можно распознать... А триэтилборат( (C2H5O)3B ) горит зелёным пламенем...(Как наверное уже всем известно, получается B2O3)
-
3. Со спиртом получается триэтилборат, а с камфорой в нём - не представляю
-
Да их всех за это надо...!
-
Сульфат магния, в отличие от хлорида кальция обладает большей инертностью к высушиваемым им веществам. Не я кусок срезал - такая скан-копия...
-
Хотя бы ссылки на методики...
-
Согласен,этот способ лучше,но ортофосфорную кислоту ещё раздобыть надо, а так идёшь в аптеку, покупаешь аскорбиновую кислоту(1уп=1г. 5 рублей.) и смешиваешь с йодом
-
Йодоводород также можно получить при смешивании йода с аскорбиновой кислотой.
-
Плюс к этому, в растворе выделяется водород и имеет место быть высокая(относительно высокая) температура
-
Это медь. Я таким образом получал медь для использования в качестве катализатора
-
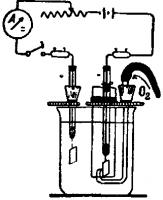
Опыт. Получение перекиси водорода катодным восстановлением молекулярного кислорода водородом. Реакция протекает по уравне¬нию O2 + 2Н —> Н2O2+138 ккал. Прибор собирают в соответствии с рис. 128. Электролитической ванной служит стакан емкостью 250—300 мл, заполненный серной кислотой (уд. вес 1,2—1,25) и накрытый асбестовой пластинкой. Сквозь пластинку пропускают анод и стеклянный цилиндр диа¬метром 3 см, внутри которого находится катод, а также стек¬лянную трубку, по которой из газометра или баллона поступает чистый кислород. Подающая кислород трубка с оттянутым кончиком проходит снизу под цилиндр и заканчивается у самого катода. Вблизи анода в асбестовой пластинке проделывают еще одно отверстие для удаления кислорода, выделяющегося у анода. Анодом служит платиновая пластинка, расположенная на бо¬лее высоком уровне по сравнению с катодом. Катод изготовляется из платиновой или палладиевой пластинки. Рис. 128. Источником электрической энергии является батарея аккуму¬ляторов напряжением 10 в. После сборки прибора берут пипеткой из анодного пространства 10 мл электролита, выливают его в стакан и добавляют несколько капель раствора сульфата титанила. Никакого окра¬шивания в этом случае не происходит. Через 5—10 минут после начала электролиза при силе тока 4—5 а и пропускании сильной струи кислорода выключают ток и берут пробу электролита. На этот раз при добавлении сульфата титанила электролит окрашивается в желто-оранжевый цвет; это объясняется образованием пероксодисульфатотитановой кислоты При более длительном электролизе пробы на сульфат титанила дают более интенсивное окрашивание. При этом имеют место сле¬дующие реакции: а) TiОSO4 + Н2O2+Н2O = Н2ТiO4+Н2SO4, б) TiОSO4 + Н2O2+ Н2SO4 =Н2[ТiО2(SO4)2] + Н2O. Это отрывок той статьи... Вроде была где-то на сайте... Полную статью качайте тут...Нет не тут, он(сервер) файл загружает, а после пишет "Вы не выбрали файл для загрузки"
-
У меня где-то был способ получения водородной перекиси при электролизе крепкой серной кислоты...Точного механизма не помню, найду - размещу
-
Я написал своё личное отношение к кошкам(с тех пор я недолюбливаю кошек), иначе форумчане-любители кошек меня бы уже съели...
-
Как и у нас в Иркутске...
-
Нет магазина хим. реактивов поблизости. А при обычном горении серы выделяется только SO2 или SO с SO2?