
Заряночка
-
Постов
182 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Заряночка
-
-
Да, это их ответы. Как я понимаю, растворимость показывает, какая максимальная масса вещества может раствориться в 1000 или 100 г воды при данной температуре.
-
-
Ответ: m(кристаллогидрата)= 248х= 21,824г, m (воды)= 18,558г.
Масса третьего раствора равна 175,38г, объем его равен 118,5мл
-
Спасибо, что снова откликнулись, но, вот отправляю так, как написано.

-
M_GM, доброе время суток! Я же не на олимпиаде сижу. Задача за прошлый год. Хочу разобраться. А потом сама начала бы решать.
-
Растворимость пентагидрата тиосульфата натрия в воде при 00С равна 82,42г. Какие массы данного кристаллогидрата и воды необходимо взять для получения раствора, насыщенного при 0ºС, чтобы при его сливании со 100 мл 70%-ного раствора (ρ = 1,65 г/мл), насыщенного при 70ºС, был получен третий раствор, из которого при 50ºС (массовая доля соли в насыщенном растворе равна 62,92%) можно выделить 30,0 г пентагидрата тиосульфата натрия? Какова масса и объем полученного насыщенного раствора при 500 С. Плотность третьего раствора принять равной 1,48 г/мл.
Это олимпиадная задача. Не смогли бы кто-нибудь подробное решение написать? Спасибо.
-
От потенциалов которые легко считаются, но на практике идет вторая.
Спасибо!
-
Скажите, пожалуйста, какая реакция верна?
1. 2KMnO4 + KI + H2O = KIO3 + 2MnO2 + 2KOH
2. 2KMnO4 + 6KI + 4H2O = 8KOH + 2MnO2 + 3I2
3. 2KMnO4 +KI + H2O = KIO + MnO2 + KOH.
От чего зависят продукты реакции?
-
Если катионы, частицы с зарядом +, значит потеряли электроны
При этом на внешнем слое у них осталось 3 электрона
Значит у исходных атомов на внешнем слое было больше 3-х электронов
Такими здесь являются только атомы элементов V группы N и P
Одно но - в соединениях такие элементы не склонны к образованию ионной связи, тем более в роли катионов
Поэтому катионы такого строения они могут образовывать
только в ходе каких-то физических процессов
N (1s22s22p3) - 2e => N+2(1s22s22p1)
Спасибо вам большое! Я тоже так думаю. Но это вопрос ЕГЭ(
-
Даны:
1)N, 2)Be, 3)B, 4) AI, 5) P
какие из указанных в ряду элементов образуют катионы, которые могут иметь электронную конфигурацию внешнего энергетического уровня ns2np1?Не понимаю, кто может подробно объяснить?
-
Электролиз K2SеO3.
Я пишу для расплава так:
K2SеO3 = 2K+ + SеO32-
на катоде: K+ + 1е = К0 *2
на аноде: SеO32- -2e = SeO3
суммарное: 2K+ + SeO32- = 2К0 + SeO3
уравнение электролиза: K2SeO3 = 2К + SeO3для раствора:
K2SеO3 - среда раствора щелочная.
K2SеO3 = 2K+ + SeO32-
Н2О = Н+ + ОН-
на катоде 2Н2О + 2е = Н2↑ + 2ОН- *2
на аноде: 4ОН- - 4е = О2↑ + 2Н2О; (в щелочной среде)суммарное: 4Н2О + 4ОН- = 2Н2↑ + 4ОН- + О2↑ + 2Н2О
уравнение электролиза: 2Н2О + 2Н2↑ = О2↑Почему тут раствор рассматривается совсем по-другому? Где я ошибаюсь? Помогите, пожалуйста!
-
Электролиз K2SеO3.
Я пишу для расплава так:
K2SеO3 = 2K+ + SеO32-
на катоде: K+ + 1е = К0 *2
на аноде: SеO32- -2e = SeO3
суммарное: 2K+ + SeO32- = 2К0 + SeO3
уравнение электролиза: K2SeO3 = 2К + SeO3для раствора:
K2SеO3- среда раствора щелочная.
K2SеO3 = 2K+ + SeO32-
Н2О = Н+ + ОН-
на катоде 2Н2О + 2е = Н2↑ + 2ОН- *2
на аноде: 4ОН- - 4е = О2↑ + 2Н2О; (в щелочной среде)суммарное: 4Н2О + 4ОН- = 2Н2↑ + 4ОН- + О2↑ + 2Н2О
уравнение электролиза: 2Н2О + 2Н2↑ = О2↑Почему тут раствор рассматривается совсем по-другому? Где я ошибаюсь? Помогтье, пожалуйста!
-
Спасибо!!!!!
-
Вот так можно написать: H2ZnO2 + CaCO3 = CaZnO2 + H2O + CO2 ?
-
-
-
Очень интересная дискуссия получилась) Не зря сказано, что в споре рождается истина. Много для себя поняла. Я просто привыкла уравнивать методом полуреакции, так легче для меня. А на егэ быстро переведу на ЭБ. Эб не так быстро получается у меня. Поэтому хотелось добить до конца, почему не получается. Теперь поняла, оказывется, остаток. что не получается , нужно перепроверить и подбирать самим допускается. Спасибо большое всем!
-
Я вот никогда электронно-ионным методом не уравнивал. Гораздо проще по химическому смыслу.
Здесь реакция сводится к следующему:
J2O5 + SO2 -> J2 + SO3
Коэффициенты очевидны:
J2O5 + 5SO2 -> J2 + 5SO3
Навешиваем на оксиды K2O
2KJO3 + 5K2SO3 = J2 + 5K2SO4 + K2O
Чтобы в продуктах не было K2O (т.е, KOH в водной среде), добавляем в исходные H2SO4, справа появляется вода. И все!
2KJO3 + 5K2SO3 + H2SO4 = J2 + 6K2SO4 + H2O
Это я тоже поняла, но мне именно электронно-ионным методом нужно уравнять!
-
. Думается, должно быть так:
5K2SO3 + 2KIO3 + H2SO4 = 6K2SO4 + I2 + H2O
Согласна. Тогда где ошибка в полуреакции?
. Думается, должно быть так:
5K2SO3 + 2KIO3 + H2SO4 = 6K2SO4 + I2 + H2O
Получается, полуреакция правильна, а уравниваем в конце методом подбора?))
-
Задание такое: Для выполнения задания используйте следующий перечень веществ: сульфит калия, йодат калия, серная кислота, сульфат калия, сульфид серебра. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна окислительно-восстановительная реакция, и запишите уравнение этой реакции. Составьте электронный баланс, укажите окислитель и восстановитель.
Может у меня уравнение реакции неправильное?
Пробовала исправить, теперь не уравнивается калий.
-
Здесь подробно расписано, как пользоваться электронно-ионным методом
http://forum.xumuk.ru/index.php?showtopic=206938
Пробуйте и получится
Я пробовала так уже, не получается. Где ошибка, не пойму. Может посмотрите?
-
KIO3 + K2SO3 + H2SO4 =
что получается и как уравнять электронно-ионным методом?
Я пробовала написать уравнение так: KIO3 + K2SO3 + H2SO4 = I2 + K2SO4 + H2Oтолько у меня не получается уравнять методом полуреакции.
А методом электронного баланса получается так:
2KIO3 + 5K2SO3 + H2SO4 = I2 + 6K2SO4 + H2O
-
Из предложенного перечня веществ: аммиак, феррат железа, серная кислота, гидроксокарбонат меди(II), сульфат калия выберите вещества, между которыми возможна окислительно-восстановительная реакция, и запишите уравнение этой реакции. Допустимо использование водных растворов веществ.
Я даже не нашла как пишется формула феррата железа(... Ферраты калия, натрия есть, а железа не могу найти. Еще не указана степень окисления его. Если предположить, что Fe(II), то думала, что FeFeO2. А как написать ОВР?
-
Я присоединяюсь к предыдущему ответу, но хотелось бы уточнить. Электролиз обычно сходен с протеканием простой редокс-реакции в растворе и дает те же продукты. Что мы получим, если подействуем перманганатом на раствор кислого оксалата натрия? Никто ведь не сомневается, что углекислый газ. Почему тут надо в этом сомневаться? Да, есть хитрые случаи, вроде реакции Кольбе для солей карбоновых кислот... Ну пусть тут работает этот механизм (наверняка нет, но - допустим), и получающийся радикал НОСО. будет стабилизироваться димеризацией. В ходе реакции получим щавелевую кислоту, и можно начинать все сначала. Такое каталитическое декарбоксилирование с выделением того же углекислого газа.
Спасибо всем большое! А это нужно ведь для ЕГЭ!!)
Если элемент аниона в высшей степени окисления (сульфат, карбонат, нитрат) то да, окисляется кислород.
В оксалат-ионе степень окисления углерода +3, и окислить его легче чем кислород.
Поэтому окисляется гидрооксалат-ион до гидрокарбонат-иона.
Можно так: Катод 2H2O + 2e = H2 + 2OH-
Анод HC2O4- + 2H2O - 2e = 2HCO3- + 3H+
=====================================
Суммарно: HC2O4- + 2H2O = H2 + 2HCO3- + H+
Но накопление ионов водорода переводит часть гидрокарбонат ионов в угольную кислоту,
которая разлагается: HC2O4- + H2O = H2 + HCO3- + СO2
Отсюда продукты: водород на катоде, СО2 на аноде, гидрокарбонат в растворе
Очень понятное объяснение для егешника! Спасибо!
Спасибо всем большое! А это нужно ведь для ЕГЭ!!)
Очень понятное объяснение для егешника! Спасибо!
ссылку неправильно написала. вот тут: https://reshimvse.com/zadacha.php?id=4321
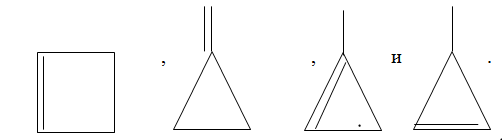
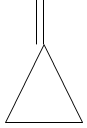 Как можно назвать вот этот изомер С4Н6?
Как можно назвать вот этот изомер С4Н6? 


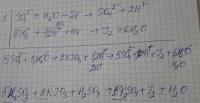

Циклические изомеры С4Н6
в Решение заданий
Опубликовано
может метиленциклопропан? )