
torpedineformes
-
Постов
306 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные torpedineformes
-
-
доброго времени суток!
вопрос возник на повестке дня - как в промышленных масштабах получить этилен из этилового спирта? (все обычно делают наоборот... )
есть беглые данные про получение из этилового спирта пропусканием его паров через окись алюминия при 450С , но никак не могу найти литературу или хотя бы описание сего чудного процесса.
если у кого то есть на примете какая либо информация - буду премного благодарна!
C2H5(OH) ---> H2C=CH2↑ + HOH. Реакция проходит в присутствии H2SO4(конц.) и под действием температуры(t>140oC)
-
-
-
Я смотрю тут всем так нравится ЙОД...

-
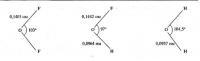
Вот картинка из Гринвуда (слева F2O, в центре HOF, справа H2O):
Ничего особого в строении нет, обычные ковалентные связи, только угол более острый. Просто пример с HOF является одним из тех, которые наиболее ярко демонстрируют всю условность понятия С.О. Тут Вы абсолютно правы. Понятие степени окисления является условным и было введено для удобства описания процессов, связанных с переходом электронов (ОВР), поэтому значения С.О. являются формальными величинами (реальные эффективные заряды на атомах намного меньше их значений С.О.). В сущности, совершенно безразлично, какие конкретные значения зарядов приписать тем или иным атомам. Главное при уравнивании ОВР - чтобы соблюдалось условие электронейтральности молекул (не нарушался баланс при обмене электронами).
Вот пример, как путаются в мыслях авторитеты (может быть, они просто поручают писать свои статьи другим?)
 :
:"Образование так называемых «мостиковых» связей (а в них могут быть задействованы атомы кислорода, серы, фтора, причем атомы фтора могут заменять атомы кислорода) не укладывается в рамки классической теории валентности, которую уже давно «подкрепляют» иным понятием – степени окисления. А с ней все в порядке: степень окисления фтора в соединениях всегда отрицательна и равна единице". Э.Г. Раков, профессор: "Парадоксальная химия фтора". http://him.1september.ru/articlef.php?ID=199900701
"Степени окисления галогенов: — 1 (наиб. характерная); + 1 (НОF, НХО и др.); + 3 у Сl и Вr (НХО2, XF3); + 4 у Сl, Вr, I (ХO2); + 5 (НХO3, XF5 и др.); + 6 у Сl (Сl2О6); + 7 у Сl, Вr и I (HClO4, Cl2O7, НВrO4, IF7 и др.)". Э.Г. Раков: ст. "Галогены", Химическая Энциклопедия под ред. И.Л. Кнунянца http://www.xumuk.ru/encyklopedia/909.html
P.S. Со степенями окисления элементов в HOF мы в своё время прикалывались над абитуриентами - говорили им, что этот вопрос часто встречается в билетах и с интересом наблюдали, как они постепенно впадают в транс. :D
?!
-
Это что за суперлегковес? Такого нуклида вроде бы нет.
-
гелий в термоядерном синтезе участвует в виде изотопа 3He. 4He обычно неактивен, потому что имеет слишком высокую энергию активации по сравнению с более легкими ядрами.
Данная рекция ведь возможна: 42He + 11H → 43Li + n и мне кажется она отвечает требованиям термоядерной реакции(слияние сверхлёгких ядер в более тяжёлые).
-
Да выпить его в конце концов.
-
А еще можно вспомнить озон О4+О2-2, и вся формальность степени окисления предстает во всей красе.
Какая графическая формула будет у озона?
-
А уж чем вызвало затруднение K2O понять не могу. +1 у K и -2 у кислорода.
Перепутал с KO2
-
Степень окисления - понятие условное, на него равняться не стоит. Вот вам еще несколько примеров, где степень окисления кислорода равна нулю (одного из атомов): NO3F, ClO4F. И ничего, живут!
А тут какие степени окисления: HCN, K2O? Просто интересно.
-
Продукты реакции:
NaHS+ CaCO3=
2NaHS+ 2CaCO3=Na2CO3+2S+H2CO3(разлагается на воду и CO2)???
Ну я написала явно бред((
Вы чё забыли, Вы уже спрашивали об этом, в этой же теме.
-
Коллега, просто тема посвящена восстановительным свойствам фтора, а во фтороноватистой кислоте фтор - окислитель, а потому зачем считать степени окисления остальных атомов?
Свою попытку torpedineformes уже привел, правда неверную Строение оксофторида водорода необычное, степень окисления кислорода в нем равно 0.
Если 0, то что он(кислород) там делает? Получается там электостатическая связь?
-
H:+1;
O:+2;
F:-1.
-
Но всё же: Если реакция обратима то считается что реагенты взаимодействуют между собой или нет?
-
а как определить какая более нерастворима?
По таблице растворимости различных соединений.спасибо кэп
-
А продукты этой реакции?
NaHS+CaCO3=?
Возможна ли она вообще?
Помоему невозможна.
-
-
А фторид ксенона (VIII) разве существует? Я слышал, что были заявления о его обнаружении в спектре, но они были опровергнуты. Вот XeO4 существует по данным любой литературы.
Понятно, что все это написано в википедии, но как-то не верится...
Я видел своими глазами тока XeF2. Читал, что есть ещё XeF4 и XeF6. А они неустойчивы?
Если неустойчивы, то можно не спорить за существование XeF8.
XeF2 хранят в тефлоновых контейнерах, почему?
-
-
Я уже давно знаю, что фиолетовый перманганат калия под действием бесцветной лимонной кислоты даёт жёлтое окрашивание.
А что его вызывает? Ионы Mn3+?
У Mn3+ - цвет тёмно-сиреневый
-
1.почему нельзя физическими методами получить 100%-ный этанол из его водного раствора?
2.сколько изомерных третичных спиртов имеют состав C6H13OH? написать формулы и названия.
3.написать уравнения реакций, в результате которых можно получить: из метана->диэтиловый эфир.
4.какую массу бутадиена-1,3 можно получить из спирта объемом 230л и плотностью 0,8 кг/л, если массовая доля этанола в спирте равна 95%? выход продукта реакции составляет 60%.
5.из пропанола-2 массой 24г добыт 2-бромпропан, из которого синтезировали 2,3-диметилбутан.вычислить массу добытого продукта, если выход на обеих стадиях синтеза составляет по 60%.
3.
CH4 + Cl2 = CH3Cl + HCl;
2CH3Cl + 2Na = CH3-CH3 + 2NaCl;
CH3-CH3(1500oC,Ni)= H2C=CH2 + H2;
H2C=CH2 + HOH(t,p,кат.)= CH3-CH2-OH;
CH3-CH2-OH(140oC, H2SO4(конц.))= C2H5-O-C2H5 + HOH;
-
А почему???
А потому что вонючий.
-
Спасибо. чем слабее притяжение между частицами кислоты, тем сильнее кислота? то есть чем слабее связь, тем сильнее кислота?
Немножко не так сформулированно, но в общем так
Сложный ли предмет химия?
в Курилка
Опубликовано
Химия сложный предмет, тут и говорить нечего