-
Постов
34 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные 1tata1
-
-
Если в живом организме, то вспоминайте, с каким ферментом он взаимодействует и как, что является субстратом фермента и какие продукты реакции.
да,в живом организме
взаимодействует с Ацетилхолинэстеразой. т.е. надо написать реакцию : ацетилхолин+вода---ацетилхолинэстераза-->холин и уксусная кислота?
-
Пожалуйста помогите написать реакцию, скорость которой изменяет хлорофос.
-
При такой маленькой концентрации можно принять, что плотность раствора равна 1 г/мл
Значит 1 л раствора имеют массу 1000 г и содержит 28 г вещества C6H5NH2, находите количество вещества (моль) и молярную концентрацию С.
"а степень ионизации равна 3,8*10-10 " - очевидно, что это не степень, а константа ионизации, т.е. константа равновесия реакции
C6H5NH2, + H2O ↔ C6H5NH3+ + OH-,
и степень ионизации можно посчитать по закону разбавления Оствальда: α = (K/C)0,5.
спасибо большое вам,а то то,что нет плотности, в какой-то ступор ввело меня
-
Рассчитать степень ионизации pH раствора C6H5NH2, если концентрация равна 2,8%,а степень ионизации равна 3,8*10-10. помогите пожалуйста разобраться с данной задачей,ну или как начать ее решать, точнее как найти концентрацию,чтобы она была не в процентах уже?
-
помогите пожалуйста с этим заданием,т.к. подобного до этого не решалось. заранее спасибо
укажите графически электронные эффекты функциональных групп в молекуле 4-гидросибутановой кислоты.укажите вид и знак этих эффектов
-
Сегодня явно не ваш день в математике. Сначала вы делите, вместо того, чтобы умножить, потом умножаете вместо деления.
Как может эквивалентная концентрация быть меньше молярной????
точно не мой день
надо умножить на 2,а не на 1/2.
еще раз огромное спасибо за помощь
-
Да не за что, только делить нужно не на 0,1, а на....
Подумайте сами, опирайтесь на это:
т.е.чтобы найти Сэквивалентную,надо Смолярную=0,1 умножить на 1/2? и все это подставить в формулу?
-
спасибо
-
Сосуд для измерения электропроводности наполнен раствором сульфата меди, содержащим 0,1 моля CuSO4 в 1л. Поверхность каждого электрода – 4 см2. Расстояние между ними – 7 см. Сопротивление слоя раствора, заключенного между электродами равно 23 Ом. Определить удельную и эквивалентную электропроводность этого раствора.

отсюда k= l / (R*S), где K-удельная электропроводность
подставив значения,получила такое ответ 0,076 Ом-1* см-1
Как теперь найти эквивалентную электропроводность?точнее за К подставить полученный результат,а что дальше?просто подставить вместо С 0,1 моль и разделить на 1000(т.к. у нас измерение в литрах)?

-
-
Да, это степень извлечения, только показывает она не сколько извлечено, а сколько останется.
В человеческом виде (да и всем понятном), формула закона распределения (для однократной экстракции) запишется.
m = m0*K*Vр-ра / (K*Vр-ра + Vэкстрагента)
Тут m - масса вещества, которая останется!!!!, (но не извлечется), с объемами, думаю тоже понятно.
Попробуйте теперь подставить все числа.
я вот что-то совсем запуталась с массами.подскажите пожалуйста,что m ,а что m0.просто с такой формулой не решала задачи
-
Конечно. Только останется вспомнить, что такое и как рассчитывается хB и все.
спасибо.с этой задачей уже разобралась
-
Что такое R в вашей, через чур сокращенной формуле?
это в учебнике дана такая формула. R-это степень извлечения. так эта формула совсем сюда не подходит?
-
коэффициент распределения SO2 между водой и хлороформом равен 0,0953. сколько воды надо добавить к 1л раствора, чтобы извлечь 25% SO2
R=D/(D+VB/V0)
0,25= 0,953/(0,953+1/V0)
правильно ли я подставляю данные?просто путаюсь,куда надо подставить 1л(вверх- VB или вниз-V0)
-
1 закон Рауля используйте
 эту формулу необходимо использовать?
эту формулу необходимо использовать? -
Помогите пожалуйста решить задачу,хотя бы с принципом решения
Давление пара над раствором, содержащим 13 г растворенного вещества в 100 г воды, при 28 ºС равно
0,03645*105 Па. Вычислите молярную массу растворенного вещества.Давление насыщенного пара воды при указанной температуре
составляет 0,0374*105 Па.
-

определите массы H2O и C4H9OH в водном и бутанольном растворах,если 1 кг системы с массовой долей равной 40% C4H9OH охладить до 350 K
-
спасибо,все понятно теперь
-
Это называется подгонкой под ответ, а не решением.
а как можно решить,не могли бы вы объяснить,если несложно?хотя бы принцип решения
-
Примерно так. lg1 = 0
а не могли бы вы еще тут подсказать.
какое соотношение компонентов ацетатного буфера необходимо взять,чтобы поддержать постоянство pH среды,равное 5?
а) [CH3COOH]/[CH3COONa]=1/1,74
б) [CH3COOH]/[CH3COONa]=1,74/1
в) [CH3COOH]/[CH3COONa]=1,74/1,74
ответ "а"? мы просто должны подставить это значение в логарифм или нет?
-
Ответ верный. А почему, на формулу Гендерсона - Гассельбаха посмотрите.
т.е. логарифм будет равен нулю,так как объемы и концентрации сократятся, и поэтому pH=pKa.верно?
-
каков pH ацетатного буфера,полученного смешиванием равных объемов эквимолярных растворов CH3COOH и CH3COONa?
а)pH>pKa б)pH
ответ вроде "в". если это так,не могли бы объяснить почему?
-
В зависимости от вида реакции ничего не меняется, иначе это не закон получится, а "что хочу, то ворочу"
Хоть горения, хоть соединения, да хоть ядерного взрыва. Изменение энтальпии реакции равно одному и тому же:
ΔН = ΔНобр(продуктов) - ΔНобр(исходных веществ).
Это - закон!!!!!!
я понимаю,что это закон,просто на лекции нам дали еще одну формулу.энтальпия сгорания :
ΔН = ΔНсгорания(исходных веществ) -ΔН сгорания(продуктов)
-


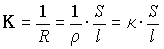
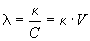
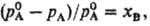 эту формулу необходимо использовать?
эту формулу необходимо использовать?
Реакция, скорость которой изменяет хлорофос
в Решение заданий
Опубликовано
спасибо