
Marin
-
Постов
7 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Marin
-
-
приведите электронно-ионный баланс:
S2O3(2-) + H(+) → SO2 + S + H2O
-
Слева: 2-гидроксипропановая кислота, циклогексанол, пара-аминобензойная кислота
Справа: 2-оксопентандиовая кислота, гепта-2,4-диен
Большое спасибо за ответ!)
-
1. Назовите соединения по заместительной номенклатуре ИЮПАК
2. Напишите структурные формулы следующих соединений: 2-аминоэтантиола-1;
о-гидроксибензойной кислоты.
3. Какие из приведенных соединений содержат сопряженные фрагменты? Укажите вид
сопряжения. Укажите вид гибридизации орбиталей каждого атома углерода.
4. Выберите соединение, молекула которого хиральна: 2-гидроксипропановая или
4-аминобутановая кислота. Напишите формулы стереоизомеров. Назовите их по D,L- и
R,S-номенклатуре (с использованием правил преобразования формул Фишера).
Дайте определение энантио- и диастереомеров.
7. Дайте определение конформации. Напишите в виде проекций Ньюмена конформации
бутаналя. Приведите их энергетическую кривую.
-
1 Выберите из приведенных структур ароматические: анилин, нафталин, циклогексан.
Приведите критерии ароматичности и обоснуйте принадлежность выбранных структур
к ароматическим.
2 Укажите вид и знак электронных эффектов в следующих соединениях: этилбензол,
нитробензол, пентен-1, пропановая кислота. Обозначьте эффекты графически.
3 Дайте определение понятия «кислота» по теории Брёнстеда. Сравните кислотность
этанола, пропанола, пропантриола-1,2,3, основываясь на стабильности соответствующих
анионов. Напишите уравнение реакции образования натриевой соли для наиболее
сильной кислоты.
4 Дайте определение понятия «основание» по теории Брёнстеда. Сравните основность
в растворе этанола, диэтилового эфира, этиламина.
Напишите уравнение реакции солеобразования для наиболее сильного основания.
-
Спасибо!))) И еще, если не затруднит посмотрите одно задание
Используя величины констант нестойкости соответствующих комплексных ионов, сделайте выводы о возможности образования нового комплексного соединения и напишите уравнения соответствующей реакции в молекулярном и ионном виде
[Cu(NH3)4]Cl2 + KCN=
-
1) Пероксид натрия. Указать степень окисления кислорода в этом соединении. Написать уравнения реакции перманганата калия с пероксидом натрия в кислой среде.
2) Закончить и уравнять ионно–электронным методом следующую реакцию: К2МnO4 + Н2O2 + Н2О =
3) Пользуясь методом валентных связей, объяснить механизм образования химической связи, тип гибридизации и геометрическую конфигурацию следующего комплексного иона: [Zn(OH)4]2–
4) Подобрать коэффиценты ионно–электронным методом:
АLСL3 + Nа2СО3 + Н2O = AL(OH)3 + CO2↓ + NaCL
5) Уравнять ионно–электронным методом следующую реакцию: Na2S2O3 + CL2 + H2O = H2SO4 + NaCL + HCL
6) Объяснить характер изменения устойчивости, силы кислот и окислительной активности в ряду НСlO— НСlO2— НСlO3—НСlO4. В каких средах проявляют окислительные свойства: а) гипохлориты; б) хлораты? Написать уравнения реакции бромата калия с бромидом калия в сернокислой среде и уравнять ионно–электронным методом.
7) Написать уравнение реакции для следующего превращения: МnSO4 → МnSO4
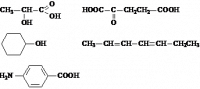
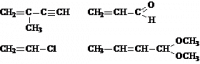
Электронно-ионный баланс
в Решение заданий
Опубликовано
Спасибо Вам огромное!