Vilanda
Пользователи-
Постов
52 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Vilanda
-
Так? (NH4)2SO4 + 2HNO3 = 2N2 + H2SO4 + 4H2O + О2
-
-
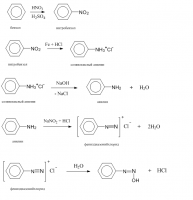
Помогите составить уравнение реакции окисления аммония азотной кислотой. В условии сказано, что это один из способов получения азота. (NH4)2SO4 + HNO3 = N2 + ? Я подумала и составила такое уравнение: 5(NH4)2SO4 + 6HNO3 = 8N2 + 5H2SO4 + 18H2O 2N-3 ‒ 2·3e = N20 │5 2N+5 + 2·5e = N20 │3 Такая реакция возможна?
-
Спасибо!
-
-
Спасибо за подсказку! Теперь все сходится. Сейчас допишу всю цепочку.
-
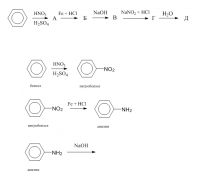
Спасибо за ответ. Возможно, в задании ошибка? Мне нужно написать уравнения реакции по такой схеме: Не знаю, что там будет с анилином?
-
Что образуется при взаимодействии анилина с NaOH? Идет ли такая реакция?
-
Подскажите, где можно найти значение константы Генри для паров ацетона (нужно для расчета абсорбера). В русскоязычной литературе не нашла, но видела в англоязычной литературе в интернете, но размерность - моль/кг*бар или атм*м3/моль. Ведь она должна быть к тех же единицах, что и давление?
-
Спасибо за подсказку.
-
Пожалуйста, помогите решить задачу: Вычислите тепловой эффект (кДж) плавления льда. ∆ H298(H2OЖ) = -285,84 кДж/моль, ∆ H298(H2Oкр) = -291,9 кДж/моль. Вычислите тепловой эффект (кДж) плавления льда. ∆ H298(H2OЖ) = -285,84 кДж/моль, ∆ H298(H2Oкр) = -291,9 кДж/моль.
-
Пожалуйста, помогите с заданием: Покажите механизм растворения MgCl2 в HCl.
-
Спасибо. А как с сулемой? Там будет какое-то комплексное соединение? Может так: Na2S2O3 + HgCl2 = Na2SO4 + HgS + NaCl а, с водой действительно все уравнивается спасибо
-
Помогите пожалуйста составить уравнения: Na2S2O3 + KCN = Na2S2O3 + HgCl2 = Мне совсем ничего в голову не приходит:(
-
Ясно. А после т.э. рН будет определяться только соляной кислотой, которая теперь уже в избытке, поэтому и будет резкое снижение рН, там вроде все ясно. Все, поняла, спасибо огромное! Просто сначала запуталась с тем фенолом - все как-то хотелось считать его основанием, так как он содержит группу ОН.
-
А для точки эквивалентности как рассчитать рН?
-
Проверьте, пожалуйста, правильно ли я делаю. (решаю по примеру с книги В.П.Васильев "Аналитическая химия", т.1) Дано: 15 мл 0,05 М раствор фенолята натрия титруют 0,05 М раствором HCl. рКосн = 10,0. Для начального раствора (до начала титрования) вычисляю концентрацию гидроксид-ионов по формуле: [OH-] = корень(Косн*С) = корень(10-10*0,05) = 2,24*10-6 Тогда рассчитываю концентрацию [Н+] = 10-14 / 2,24*10-6 = 4,46*10-9 моль/л рН= -lg(4,46*10-9) = 8,35 Далее рН рассчитываю для буферного раствора. При добавлении 5 мл соляной кислоты (или 0,005*0,05 = 0,00025 моль) фенолята натрия остается столько: n(C6H5ONa) = 0,015*0,05 - 0,00025 = 0,0005 моль, тогда его концентрация: [C6H5ONa] = 0,0005 / 0,015 = 0,033 моль/л (принимаем, что объем не изменяется и остается равен 15 мл). Тогда концентрация фенола равна: [C6H5OН] = 0,00025 / 0,015 = 0,0167 моль/л Тогда рН раствора равен: рН = 14 - рКосн + lg(0,033/0,0167) = 4,3 Далее аналогично, при добавлении: 10 мл HCl рН=3,7 14 мл HCl рН=2,85 14,9 мл HCl рН=1,82 14,99 мл HCl рН=0,82 Меня смущает очень резкое снижение рН. Правильно ли я решаю?
-
Спасибо огромное, что подсказали верное направление решения. Дальше постараюсь разобраться сама.
-
Задача: построить кривую титрования раствора фенолята натрия раствором соляной кислоты. Сам фенолят натрия в водном растворе гидролизуется: C6H5ONa + H2O = C6H5OH + NaOH Так вот, при титровании соляной кислотой оттитровываться будет именно гидроксид натрия, поскольку фенол - это слабая кислота, верно? Тогда рН до точки эквивалентности рассчитывать как рН раствора сильного основания? Подскажите, пожалуйста. правильно ли я мыслю. Спасибо.
-
Физическая теплота топливного газа рассчитывается по этой формуле, верно?: Q = m*Cp*(T - 273) Вот сомневаюсь: в этой формуле должна быть разница температур (Т - 273) или просто температура топлива Т? И еще: так как топливный газ - это смесь нескольких газов (метана, этана и т.д.), то его физическая теплота - это сумма теплот каждого из компонентов?
-
там варианты ответа -0,7; -0,14; 0; 0,7; 0,14 а у меня получается 0,4 а зачем дана концентрация кислоты - 0,05 М?
-
-
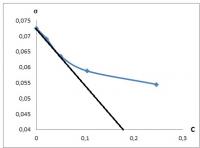
Пожалуйста, помогите решить задачу, хотя бы напишите ход действий, а то никак не получается решить((( Пользуясь графическим методом, найти поверхностную активность 0,05 М раствора масляной кислоты на границе с воздухом при 200С по следующим данным: С, кмоль/м3 0 0,021 0,05 0,104 0,246 σ · 103, Н/м 72,53 69,12 63,53 58,80 50,81 Спасибо.
-
нужно рассчитать поверхностную активность.
-
Помогите решить задачу. Определить поверхностную активность 0,12 М муравьиной кислоты, если ее поверхностное натяжение равно 72,6·10-3 н/м, а поверхностное натяжение воды 72,55·10-3 н/м. Заранее спасибо.