
docanton
-
Постов
145 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные docanton
-
-
Здравствуйте, какая размерность концентрации вещества в формулах расчёта молярного и удельного показателя погашения раствора в фотоколориметрических и спектрофотометрических исследованиях: г/мл, или моль/л, или %?
У меня пот по этой задаче значения удельного и молярного коэффициентов экстикции что-то большие. Где здесь неправильно посчитано.
Не пропечатались нарисованные в хемдроу удельный коэффициент погашения раствора
Измерение спектра поглощения субстанции рибофлавина (витамина В2) в видимой области спектра. Рибофлавин обладает характерным спектром поглощения в видимой области спектра при 445 нм и в ультрафиолетовой области спектра при следующих длинах волн: 347, 268 и 223 нм. При этих длинах волн субстанция рибофлавина имеет следующие молярные показатели погашения раствора субстанции рибофлавина в 0,05 моль/л раствора натрия гидроксида: 12300 л/моль•см, 10800 л/моль•см, 31400 л/моль•см, 30100 л/моль•см соответственно. Молярная масса рибофлавина составляет 376,4 г/моль.
Ход работы следующий:
1) приготовление раствора натрия гидроксида с концентрацией 0,05 моль/л.
2) приготовление исходного раствора рибофлавина с концентрацией 0,004 г/мл в растворе натрия гидроксида с концентрацией 0,05 моль/л.
3) приготовление серии растворов рибофлавина с различными концентрациями (таблица 7).
Таблица 7
Параметры приготовления растворов субстанции рибофлавина
с различными концентрациями
Концентрации растворов рибофлавина, г/мл
Объём воды очищенной, мл
Объёмы внесённого раствора рибофлавина, мл
Оптическая плотность растворов при длине волны 445 нм
1
0
2
0
0
2
0,000016
2
0,4
0,469
3
0,000020
2
0,5
0,533
4
0,000024
2
0,6
0,720
5
0,000028
2
0,7
0,713
6
0,000032
2
0,8
0,864
4) регистрируют спектр поглощения рибофлавина с концентрацией 0,0001 моль/л в видимом диапазоне в области от 300 до 500 нм, определяя оптическую плотность через каждые 10 нм. Отображается график зависимости оптической плотности от длины волны.
Для расчёта удельного и молярного коэффициентов погашения (поглощения) растворов рибофлавина необходимо пересчитать концентрацию растворов из г/мл в моль/л. Так как знаменатель в обеих формулах разный, то итоговую формулу надо умножить на 1000, что значит 1000 мл или 1 л для перевода мл в л.
C = (m × 1000) / (М.м. × V) = (0,000016 г × 1000 мл) / (376,4 г/моль × 1 л) = 0,0000425 моль/л.
C = (m × 1000) / (М.м. × V) = (0,000020 г × 1000 мл) / (376,4 г/моль × 1 л) = 0,0000531 моль/л.
C = (m × 1000) / (М.м. × V) = (0,000024 г × 1000 мл) / (376,4 г/моль × 1 л) = 0,0000638 моль/л.
C = (m × 1000) / (М.м. × V) = (0,000028 г × 1000 мл) / (376,4 г/моль × 1 л) = 0,0000744 моль/л.
C = (m × 1000) / (М.м. × V) = (0,000032 г × 1000 мл) / (376,4 г/моль × 1 л) = 0,0000850 моль/л.
5) рассчитывают коэффициент экстикции – удельный коэффициент погашения раствора при длине волны 445 нм.
= Dиссл. / (C × L) = 0,469 / (0,0000425 моль/л × 1 см) = 11035,29 (100 мл/г•см).
= Dиссл. / (C × L) = 0,533 / (0,0000531 моль/л × 1 см) = 10037,66 (100 мл/г•см).
= Dиссл. / (C × L) = 0,720 / (0,0000638 моль/л × 1 см) = 11285,27 (100 мл/г•см).
= Dиссл. / (C × L) = 0,713 / (0,0000744 моль/л × 1 см) = 9583,33 (100 мл/г•см).
= Dиссл. / (C × L) = 0,864 / (0,0000850 моль/л × 1 см) = 10164,71 (100 мл/г•см).
6) рассчитывают коэффициент экстикции – молярный коэффициент погашения раствора при длине волны 445 нм.
Молярный показатель поглощения (погашения) – оптическая плотность раствора вещества с концентрацией вещества 1 моль/л и толщиной поглощающего слоя в 1 см (л/моль•см)
ε = (М.м. × ) / 10 = (376,4 г/моль × 11035,29) / 10 = 415368,32 (л/моль•см).
ε = (М.м. × ) / 10 = (376,4 г/моль × 10037,66) / 10 = 377817,52 (л/моль•см).
ε = (М.м. × ) / 10 = (376,4 г/моль × 11285,27) / 10 = 424777,56 (л/моль•см).
ε = (М.м. × ) / 10 = (376,4 г/моль × 9583,33) / 10 = 360716,54 (л/моль•см).
ε = (М.м. × ) / 10 = (376,4 г/моль × 10164,71) / 10 = 382599,68 (л/моль•см).
-
Здравствуйте, есть ли специальные химические программы для расчёта (предположения, предвиденья) коэффициентов ионизации (pKa или pKb) и коэффициента липофильности LogP сложных органических молекул, для которых нет таких данных в справочниках?
-
Здравствуйте, как рассчитать заряды всех атомов в органической молекуле (по их электрохимической активности) с целью вольтамперометрического метода её количественного определения в рамках квантово-химических расчётов?
Я нашёл программу ChemBio3D Pro 11 и Chem3D Pro 12, Нарисовал молекулу, перекопировал её в программы эти. Нарисовались 3D структуры молекул. А как дальше? Подскажите
-
Коллеги, подскажите, есть ли нормальный магазин фитохимических стандартов по типу американского chromadex.com но только китайский магазин? Сигма Алдрич как вариант не предлагать. он дорогой!Поисковики предлагаю алибабу, алиэкспресс, но что-то к ним доверия нет.
-
особо чисто вещество, если речь идет о количественном определении хроматографически или спектрофотометрически
-
 1
1
-
-
значит практически нерастворимое в воде
-
Данная растворимость 0,003 г/100 мл в воде. Вещество с данной растворимостью является хорошо или плохо растворимым в воде?
-
Здравствуйте, мне требуется очистить экстракт из растения, содержащего стероид, от балластных веществ: белков, фенолов, минералов и сахаров.
Т.е. депротеинизация, дефенолизация, деминерализация, дегликозидация. В интернете нашёл метод депротеинизации полисахаридов по методу Севага и есть очистка крови от белка. Есть ли методики такие?
-
Только подделать документ о результате исследования на ВИЧ, или подменить свою кровь в лаборатории на образец неинфицированной крови.
Больше никак.
-
docanton - вот чего-то я не понял про дериватизацию. Это Вы так проявление на пластинках (в смысле - визуализацию пятна) называете? Или имеете в виду предварительное химическое модифицирование, перед хроматографическим процессом? Может быть, все можно сделать проще: опрыскать пластинку своим реактивом и убедиться, что пятна - видны. Или - чистых "свидетелей" - нет, и Вы рассчитываете увидеть свои вещества только после проявления "специфическим" реагентом?
Да, я неправильно выразился, только для визуализации пятна, когда искомое вещество осталось на пластине. Дериватизация - это и есть химическая модификация, а потом хроматографирование. Визуализация, реактив на неё
Просю пардону, не ту статью прикрепил!
Таблица 6
 tmp_22138-Chromatographic_procedure_for_the_isolation_of_pla825862764.pdf
tmp_22138-Chromatographic_procedure_for_the_isolation_of_pla825862764.pdfА вообще, с давних времён, для выявления стероидных алкалоидов на тонкослойной применяют пары йода — просто и без особых заморочек, хоть и не специфично. (см. "Химический анализ лекарственных растений" Ладыгиной)
Спасибо за статью, очень полезная
-
Прочитал статью, но в ней ни одного упоминания на стероидные алкалоиды, указаны стероидные препараты синтетические, полусинтетические, природные стероиды животного происхождения, например, холестерин. Но про алкалоиды стероидные - ни слова.
вот на данном сайте http://orgchemlab.com/chromatography/reagents-for-vizualization-of-tlc-organic-compounds.html
представлены реактивы для дериватизации на пластинах искомых веществ. Но вот вопрос: чего больше в стероидных алкалоидах - стероидности или алкалоидности, то тот реактив и надо использовать. Что можете посоветовать на стероидные алкалоиды для дериватизации с данного сайта?
-
Здравствуйте, если ли на просторах интернета российские и зарубежные сайты интернет-магазинов по продаже растительного сырья? Не обязательно лекарственного. Кто-нибудь знает такой (такие)?
-
в методе тонкослойной хроматографии на этапе дериватизации?
-
Здравствуйте, можно ли использорвать реактив железа-аммония сульфат в о-фосфорной кислоте для идентификации (открывания) стероидных алкалоидов?
-
Здравствуйте, уважаемые коллеги, для растворения веществ лучше какой взять растворитель и его концентрация (раствора стандартного вещества) для ТСХ для приготовления стандартного раствора из стандартов.
Для сапонинов стероидных:
Cycloastragenol
Diosgenin
Diosgenin
Hecogenin
Neoruscogenin
Ruscogenin
Sarsasapogenin
Smilagenin
Tribulosin
Cyclovirobuxin
Protoveratrine A
Solanidin
Tomatidine
Tomatin
Для экдизонов
Ecdysone-beta
Turkesterone
-
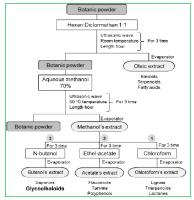
Спасибо за совет. Для ВКР нужно. Вот что он по дизайну схемы извлечения гликоалкалоидов для последующей предварительной идентификации методом тонкослойной хроматографии. Но в статье иностранной не расписано объёмы реагентов. Можете помочь?
-
А какой тогда лучшем метод по опыту?
-
А может использовать метод Крамаренко для изолирования стероидных алкалоидов из растительного сырья? Крамаренко изучал влияние рН среды на извлекаемость алкалоидов. А стероидность молекулы никак не влияет на выбор метода и эатпность анализа?
Метод Крамаренко в чистом виде:
· Настаивание измельченного объекта с водой, подкисленной 20 % раствором серной кислоты до рН = 2-3, в течение двух часов. Вода берется в количестве 1:2 по отношению к навеске объекта. Водное извлечение фильтруется. Операция повторяется двукратно;
· Очистка водного извлечения от белковых соединений путем насыщения его сульфатом аммония, настаивания в течение часа и фильтрования образовавшегося осадка;
· Очистка фильтрата от жиров, смол, пигментов путем экстракции эфиром. Эфирное извлечение отбрасывают;
· Подщелачивание водного извлечения 20 % раствором гидроксида натрия и экстрагирование веществ основного характера хлороформом при pН = 9-10 (трехкратная экстракция), отделение органической фазы и концентрирование полученного извлечения упариванием.
-
А у кого-нибудь есть методика выделения (изолирования) стероидных алкалоидов чемерицы Лобеля из растительного сырья?
Правильно ли я методику создала выделения стероидных алкалоидов:
Для экстракции искомых веществ использовали воздушно-сухое сырьё растительных организмов. Сырьё измельчали до размера частиц, проходящих сквозь сито с диаметром отверстий 2 мм. Сырьё полностью заливали водой очищенной до зеркальной поверхности, подкисляли до рН=2 по универсальному индикатору 3 % раствором кислоты серной. Сырьё настаивалось в кислой среде в течение 48 ч. После настаивание кислое водное извлечение фильтровалось через бумажный фильтр. Шрот сырья повторно заливалось водой очищенной до зеркальной поверхности и подкисление повторялось. Шрот повторно настаивался в течение 48 ч, затем фильтровалось через бумажный фильтр. Оба фильтрата объединялись. Затем надосадочную жидкость подщелачивали 25 % водным раствором аммиака до рН = 9 по универсальному индикатору. Выпавший осадок оснований СА отфильтровывали через бумажный фильтр. Высушивали в сухо-жаровом шкафу при температуре 40 ℃ в течение 1 ч.
-
какие именно интересуют СО?
ГСО согласно гос фармакопее - только по металлам и неметаллам на AAC, кроме того, еще пара флавоноидов и серд гликозидов - но это все
СО других веществ называются Secondary standard compounds - вторичные (рабочие) СО
Требуются: диосгенин, кавказосапонин, кавказопросапогенин, рускогенин, смилагенин, фенугрекин, гитогенин, ваккарогенин, тигогенин. Названия вторичных стандартов стероидных сапонинов по трём томам "Биологически активные вещества растительного происхождения" (2001-2003 гг).
По каталогам Sigma Aldrich, Fluka и Supelco. на сайте Европейской Фармакопеи нашлись следующие стандарты: гекогенина ацетат (CAS 467-55-0), сарсасапогенин (CAS 126-19-2). рускогенин (EPY0000494, CAS 472-11-7), трибулозин (CAS 79974-46-2), диосгенин (EPY0001871, CAS 512-04-9), очищенные сапонины Куалайи (EPY0001537), смилагенин (CAS 126-18-1), гитогенин (CAS 511-96-6), тигогенин (CAS 77-60-1).
Это вещество сапонин (CAS 8047-15-2) - рубеановодородную кислоту, исключить из списка. Эти вторичные стандарты нужны для аналитической ВЭТСХ. Некоторых веществ в продаже не найти, только под заказ, думаю, что дорого выйдет, остальные - тоже не дешёвые. Может, у китайцев на сайтах химических посмотреть?
-
Доброго времени суток. Нужны ГСО стероидных сапонинов с чистотой не менее 95 %. В интернете посмотрел: либо нет нужных, либо стоимости высокие. Чем можно заменить, исходят их похожести по их молекулярным массам и физико-химическим свойствам? Есть ли такая практика?
-
Приготовление первых, более концентрированных, растворов описано правильно. Только точно Вы их будете готовить именно из фармсубстанций? Хотя, "по чистой науке", так и нужно делать, но... Они у Вас есть? Точно не из коммерческих форм ЛС, как делает 95% народа (включая и представителей той же самой "чистой", но еще и бедной, науки)?
А вот дальше - хочется стукнуть!.. Сильно!.. Больно!.. И только потом - отправить изучать арифметику, хотя бы на уровне ЦПШ. Ибо, чтобы получить раствор с концентрацией 0,5 мг/мл из основного стандартного раствора 2 мг/мл, его нужно разбавить всего лишь в 4 раза. Но не в 200! Т.е., 12,5 мл - до 50 мл. Вторую концентрацию -0,75 мг/мл - получили, разбавив 18,75 мл до 50 мл. Третью - 1 мг/мл - разбавив 25 мл до 50 мл. Теперь - угу?..
И - последнее: все эти расчеты строите исходя из того, какая мерная посуда (колбы, пипетки) и сколько солянки (растворителя) имеются под рукой, и какой объем конечных стандартных растворов нужен. Фсе!..
Точно всё расписали, а поняла и пошла читать математику, фармсубстанции с чистотой не менее 99 %. Взяла в производственной аптеке экстемпоральных и готовых лекарственных форм.
-
Здравствуйте, помогите разобраться.
Как приготовить стандартные растворы папаверина и дибазола с концентрациями 0,002 г/мл (2 мг/мл) объёмами по 100 мл?
Как приготовить из этих же стандартных растворов растворы папаверина и дибазола с концентрациями 0,0005 г/мл, 0,00075 г/мл и 0,001 г/мл каждый с использованием в качестве растворителя 0,1 М раствор кислоты хлористоводородной?
Правильно ли я расписала:
Приготавливается стандартный раствор папаверина гидрохлорида и дибазола с концентрацией 0,002 г/мл. Отвешивают по 200 мг субстанций папаверина гидрохлорида и дибазола, и растворяют по отдельности в 0,1 моль/л раствора кислоты хлористоводородной объёмом по в мерной колбе на 100 мл.
Приготовление эталонных растворов из стандартных:
для приготовления растворов двух субстанций необходимо отмерить мерной микропипеткой по 0,25 мл, 0,375 мл и 0,5 мл стандартных растворов папаверина гидрохлорида и дибазола с концентрациями по 0,002 г/мл и помещают по отдельности заранее помеченные мерные колбы на 50 мл и доводят объем раствора до метки 0,1 моль/л раствором кислоты хлористоводородной, тщательно перемешивают.
В результате операции разбавления в соответствии с метками мерных колб вместимостью 50 мл в 6 мерных колбах двух лекарственных веществ будут содержаться по 0,0005 г/мл; 0,00075 г/мл и 0,001 г/мл каждого лекарственного вещества.
Но объёмы 0,25 мл, 0,375 мл и 0,5 мл - маленькие и отмеривать не очень удобно, можно ли как то исходные данные другие взять, чтобы с нормальными объёмами работать с целью получения эталонных растворов.
-
Анализируя данные иностранной литературы, обнаружила несколько методик хроматографий, я предполагаю, что некоторые из них – одно и тоже, помогите разобраться и правильно ли я сделала их точный научный перевод?
1
High-performance countercurrent chromatography (высокоэффективная противоточная хроматография)
2
Ultra-performance liquid chromatography (ультраэффективная жидкостная хроматография)
3
High-performance liquid chromatography - quadrupole time- of-flight mass spectrometry (высокоэффективная жидкостная хроматография с квадрупольной времяпролётной масс-спектрометрией)
4
Ultra-performance liquid chromatography and hybrid quadrupole time-of-flight mass spectrometry (ультраэффективная жидкостная хроматография с гибридной квадрупольной времяпролётной масс-спектрометрией)
5
Ultra-high-performance liquid chromatography (ультравысокоэффективная жидкостная хроматография)
6
Countercurrent chromatography (противоточная хроматография)
7
Liquid chromatography - tandem mass spectrometry (жидкостная хроматография с тандемной масс-спектрометрией)
8
Supercritical fluid chromatography (сверхкритичная жидкостная хроматография)
9
High-liquid chromatography tandem multi-stage mass spectrometry (высокоэффективная жидкостная хроматография с многоступенчатой масс спектрометрией)
10
High-performance liquid chromatography coupled with time-of-flight mass spectrometry and ion trap mass spectrometry (высокоэффективная жидкостная
хроматография с времяпролётной масс-спектрометрией и ионной ловушкой)
11
High-speed countercurrent chromatography - evaporative light scattering detection (сверхбыстрая противоточная хроматография с ?????)
12
Ultra-performance liquid chromatography - high-definition mass spectrometry (ультравысокая жидкостная хроматография с высоким разрешением)
13
High performance liquid chromatography - electrospray ionization mass spectrometry (высокоэффективная жидкостная хроматография с электро-ионизированной масс-спектрометрией)
14
Electrospray ionization and fast-atom bombardment tandem mass spectrometry (электро-ионизированная с электронной бомбардировкой масс-спектрометрия)
Размерность концентрации
в Решение заданий
Опубликовано
Спасибо за поправку. А как такое может быть, что в формуле расчёта концентраций по оптической плотности в соответствии с законом светопоглощения Бугера-Ламберта-Бера на одном и том же месте два разных показателя - коэффициента экстикции? Например,
C = D / (удельный коэффициент * L)
C = D / (молярный коэффициент * L)
исходя из вашей поправки