-
Постов
229 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные natitali
-
-
Задача на смеси
Имеется задача:
Газ, полученный при обжиге 32,6 г смеси сульфида цинка и сульфида железа (II), пропустили через 181,8 мл раствора гидроксида натрия с массовой долей щелочи 12% и плотностью 1,1 г/мл, в результате чего было получено 200 мл раствора с молярной концентрацией кислой соли 1 моль/л. Определите массовые доли сульфидов в исходной смеси.
Имеется решение: (прикрепляю файл)
Уважаемые химики! Прошу помочь понять, почему в действии 2) количество NaHSO4 0,1 моль? По условию задачи 200 мл с молярной концентрацией кислой соли 1 моль/л. Разве не 0,2 моль NaHSO4 получится в уравнении (4)?
Второй вопрос: объясните, пожалуйста, зачем в системе в первом уравнении все члены равенства умножили на 44? Мне не понятно решение этой системы уравнений. Помогите разобраться, если не трудно.
-
-
Так мы и есть нехимики-гуманитарии. Не волшебники, а только учимся.
-
Задача по химии на нахождение МФ
После сожжения 27,9 г соли органической кислоты, и приведения продуктов сгорания к нормальным условиям образовалось 23,5 г соляной кислоты с массовой долей хлороводорода 31,06% и 20,16 л смеси оксида углерода (IV) и азота с плотностью по водороду 21,12. Предложите возможную структурную формулу соли, если известно, что кислота может иметь два структурных изомера.
РЕШЕНИЕ:
Горит соль: СxHyClzNmOn + O2 ® HCl + H2O + N2 + CO2
1) Найдём массу и количество HCl. 23,5 · 0,3106 ≈ 7,3 г. 7,3/36,5 ≈ 0,2 моль. Следовательно, количество атомарного хлора 0,2 моль. Количество атомарного Н по НCl тоже 0,2 моль.
Необходимо найти воду, чтобы ещё установить количество водорода. Будем находить по соляной кислоте – это раствор хлороводорода в воде. Раствора кислоты получилось 23,5 г. HCl, как установлено, 7,3 г. Воды будет 16,2 г (23,5 – 7,3 = 16,2). Количество воды Н2О равно 0,9 моль (16,2/18 = 0,9). Водорода элементарного в воде 1,8 моль.
Суммарно водорода будет 2 моль (1,8 + 0,2 = 2).
2) Нам необходимо установить количества азота и углерода.
Будем решать задачу на смеси.
Дано: 20,16 л смеси СО2 и N2; ДН2 = 21,12
Найдём молярную массу и количество смеси. М(смеси) = 21,12 · 2 = 42,24 г/моль
ν(смеси) = 20,16/22,4 = 0,9 моль
Найдём массу смеси, решив пропорцию:
1 моль смеси -------------- 42,24 г
0,9 моль смеси ------------ Х г
Х = 38
m(смеси) = 38 г
Вводим допущения.
Пусть масса СО2 в смеси будет Х г, тогда масса N2 будет (38 - Х) г.
Выразим количества СО2 и N2:
ν(СО2) = Х/44
ν(N2) = (38 – Х)/28
Тогда Х/44 + (38 – Х)/28 = 0,9
Решаем и находим Х.
Х = 35,15.
m(CO2) = 35,15 г; m(N2) = (38 – 35,15) = 2,85 г
Устанавливаем количества азота и углерода.
ν(СО2) = 35,15/ 44 ≈ 0,8 моль. Отсюда ν(С) = 0,8 моль
ν(N2) = 2,85/ 28 ≈ 0,1 моль. ν(N) = 0,2 моль (атомов в 2 раза больше, чем молекул!).
3) Теперь соотношение С : Н : N : О : Cl = 0,8 : 2 : 0,2 : Y : 0,2
Сколько кислорода установим позже. Упростим соотношение. Для этого каждый член разделим на самое маленькое число (0,2):
0,8 : 0,38 : 0,2 : 0,2 = 4 : 10 : 1 : 1
4) Формула без кислорода С4Н10NCl. Это простейшая формула.
5) Наличие кислорода обязательно, так как в условии задачи речь идёт о соли органической кислоты. А в карбоксильной группе два кислорода. Следовательно, истинная молекулярная формула соли C4H10NClO2.
6) Ну, а поскольку в условии говорится о двух изомерах кислоты, то и возможны две формулы солей, например:1) CH3-CH(CH2Cl)-COO(NH4)
2) CH3-CCl(CH3)-COO(NH4)6 часов назад, XemX64 сказал:C4H10O2NCl Аммония хлоризобутират
Я поняла, что Вы задачу решили, но не захотели выложить решение.
-
 1
1
-
-
Сейчас! Сейчас! Не волнуйтесь! Я вообще-то сама просила помощи, но долго никто не отвечал.пришлосьдействовать по принципу "Спасение утопающих = дело рук самих утопающих".
Я прикрепила вордовский документ. Не вижу, что он прикрепился. Что-то не так?
-
 1
1
-
-
-
Нашла ошибку!
-
После сожжения 27,9 г соли органической кислоты, и приведения продуктов сгорания к нормальным условиям образовалось 23,5 г соляной кислоты с массовой долей хлороводорода 31,06% и 20,16 л смеси оксида углерода (IV) и азота с плотностью по водороду 21,12. Предложите возможную структурную формулу соли, если известно, что кислота может иметь два структурных изомера.
РЕШЕНИЕ:
Горит соль: СxHyClzNmOn + O2 ® HCl + H2O + N2 + CO2
1) Найдём массу и количество HCl. 23,5 · 0,3106 ≈ 7,3 г. 7,3/36,5 ≈ 0,2 моль. Следовательно, количество атомарного хлора 0,2 моль. Количество атомарного Н по НCl тоже 0,2 моль.
Необходимо найти воду, чтобы ещё установить количество водорода. Будем находить по соляной кислоте – это раствор хлороводорода в воде. Раствора кислоты получилось 23,5 г. HCl, как установлено, 7,3 г. Воды будет 16,2 г (23,5 – 7,3 = 16,2). Количество воды Н2О равно 0,9 моль (16,2/18 = 0,9). Водорода элементарного в воде 0,18 моль.
Суммарно водорода будет 0,38 моль (0,18 + 0,2 = 0,38).
2) Найдём по относительной плотности массу смеси СО2 и N2. 21,12 · 2 = 42,24 г.
3) Найдем количество смеси СО2 и N2. 20,16/ 22,4 = 0,9 моль.
4) Нам необходимо установить количества азота и углерода.
Будем решать задачу на смеси. Вводим допущения.
Пусть количество азота будет Х моль, тогда количество СО2 будет (0,9 – Х) моль.
Масса азота – это 28Х; масса СО2 – это 44(0,9 – Х); масса смеси СО2 и N2 равна 42,24 г.
Следовательно, 28Х + 44(0,9 – Х) = 42,24. Решаем это математическое выражение и находим Х.
28Х + 39,6 – 44Х = 42,24
39,6 – 42,24 = 44Х – 28Х
- 2,64 = 16Х
Х не может быть величиной отрицательной в нашем случае. Делаем другое допущение.
Пусть количество СО2 будет Х моль, тогда количество азота будет (0,9 – Х) моль. Масса СО2 – это 44Х; масса азота 28(0,9 – Х). Масса смеси этих газов 42,24 г.
Тогда 44Х + 28(0,9 – Х) = 42,24
Решаем это математическое выражение и находим Х.
44Х + 25,2 – 28Х = 42,24
44Х – 28Х = 42,24 – 25,2
16 Х = 17,04
Х = 1,065
Х больше 1, тогда как масса смеси 0,9. В чём моя ошибка?
-
Да, пожалуй, что так.
-
Так вот не следует ответ из "Химули". Карбид кальция формально можно отнести к солям. В нём нет кислотного остатка. Но карбид кальция разлагается водой. Почему конкретно никто не скажет, какой ответ правильный в задании?
-
Так гидролиз идёт? Это реакция ионного обмена с водой? Какой ответ правильный в задании?
-
-
-
Спасибо большое. Конечно же, алкин!
-
Подскажите, пожалуйста, наимудрейшие! Сомневаюсь я...
Известно, что галогенпроизводные алканов могут быть:
- геминальные (hemi – близнецы) – оба атома галогена находятся при одном углеродном атоме;
- вицинальные – атомы галогенов находятся у соседних углеродных атомов.
А какое название будет у галогенпроизводных, если галогены расположены через один и более атомов углерода в цепи?
И ещё. На второй стадии хлорирования этана образуется геминальный, вицинальный дигалогеналкан, или же их смесь? По-моему, вицинального получается немного больше в смеси. Я не права?
И ещё опять. При взаимодействии со спиртовым раствором щелочи получают алкин в случае вицинального или геминального хлорпроизводного? По-моему, и в том, и в другом случае получится алкин. Я не права?
-
А разве фосфорный ангидрид с водой не образует кислоту?
-
-
Уважаемые химики, поделитесь, если вам ведомо, в чём делают такую красоту?
http://lifebio.wiki/_media/ropivacaine.gif
-
Спасибо. Будем разбираться. В школе этому не учат.
Ещё раз СПАСИБО господину Korenev.
-
Задача из пособия Н. Кузнецовой для 10 класса. Сначала найти формулу АМИНА. Затем написать 4 формулы ИЗОМЕРОВ и дать им названия по радикально-функциональной и заместительной номенклатуре. Формулу нашли: С6Н7N. Анилин. Фениламин. А дальше не знаем. Поможете?
Ещё пиридин, в котором один Н заменим на СН3. А как он будет называться?
На основе азациклобутадиена можно ещё составить изомер к этому заданию. Радикал с двойной связью будет. А назвать как?
-
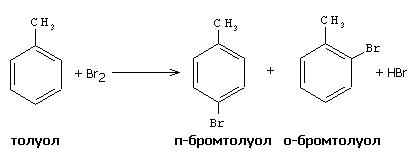
Здравствуйте! Объясните мне пожалуйста, почему толуол не реагирует с бромной водой, но реагирует с бромом? Чем бромная вода отличается от брома (насколько известно, бром-это всё-таки тоже жидкость)? И для справки: с БРОМНОЙ ВОДОЙ точно реагируют алкены, алкадиены, алкины, фенолы, анилин, жиры? А альдегиды и карб. кислоты не реагируют с БРОМНОЙ ВОДОЙ? Простите меня за дотошность, просто попалось такое задание, а в учебнике пишут иногда просто галогенирование, а с водой оно или нет-догадывайся:(
А задание было такое: Какой углеводород может реагировать с бромом на свету, но не реагирует с бромной водой?
1) толуол
2) бензол
3) бутадиен-1,3
4) циклопропан
Ответ: толуол-1.
А чем бутадиен хуже алкенов? Те же двойные связи и там, и там.
Реактивы: бромная вода, толуол.
Материалы и оборудование: микрохимическая пробирка, электроплитка, стаканчик с водой.
В микрохимическую пробирку вводят 5 капель бромной воды и 5 капель толуола, смесь подогревают в стаканчике с горячей водой, постоянно встряхивая. Наблюдают исчезновение окраски брома, в результате протекания реакции, с образованием о- и п-бромтолуолов:

- БРОМИРОВАНИЕ ТОЛУОЛА. http://orgchem.tsu.ru/ggf/lab2.htm
- И здесь: http://medlec.org/lek-29928.html
-
Да где угодно! Если идти от начала, то приходим к бутадиину-1,3. Если идти от конца (от этина), то вся цепочка рушится напрочь. Может там что-то пропущено, может из двух задачек одну сделали.
Есть, конечно, некоторая вероятность, что ассистент придумал новую реакцию, но это уже - компетенция Нобелевского Комитета

Скорее, из двух слепили одну.
-
Быть может автор, когда набивал это задание в ворде, хотел только одного - бутылку холодного пива! Но реальность требовала от него совсем другого. В результате он нечувствительно синтезировал этин из субстрата, для этого совсем не предназначенного.
ЕГЭ - это такое йегэ...
Где ошибка в задании?
-
Великолепно! Осталось всю эту красоту загнать между двомя стрелочками в задании ЕГЭ (не к ночи будь сказано), где перед стрелочкой марганцовка с бутадиеном - а за стрелочкой X1

Это напоминает четвёртый сон Веры Павловны - красиво, но - ни в п... партизанский отряд, ни в Красную Армию

А если такое приснится на экзамене? Нам говорят: надо стать на позицию автора. Что ОН хотел?





Задача на смеси
в Решение заданий
Опубликовано
Я решила эту задачу.