
Масечка New
-
Постов
92 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Масечка New
-
-
1. Помогите разобраться в чем суть задач.
Вычислить процентное содержание CaCO3,MgCO3 в пробе биологического материала, если при растворении 1 г пробы и соответствующей обработке объем довели до 100 мл и на титрование 20 мл его для определения суммы Ca и Mg , затратили 19,625 мл 0,05 М раствора трилона Б, а на титрование магния израсходовали 6,26 мл того же раствора.
2.На титрование 10 мл минеральной воды с индикатором эриохромом черным пошло 8,5 мл 0,0505 N раствора трилона Б, а при титровании10 мл мин. воды с мурексидом пошло того же титранта 5.5 мл. определите содержание магния и кальция в исследуемой воде. Помогите пожалуйста!!!
-
Помогите пожалуйста!
-
Помогите написать правильную формулу альдегида
-
Неужели ни у кого нет никаких мыслей? :(Пожалуйста помогите!
-
Пожалуйста помогите!
-
К 20 мл 0,08 М раствора Na3AsO4 прилили 30 мл 0,12 М раствора AgNO3. Выпадет ли осадок Ag3AsO4? Сколько мг серебра останется в растворе?
Вот ход моих действий: ПР(Ag3AsO4)= 1*10-22, находим концентрацию Ag из AgNO3 c=(Ag+ )*V/Vобщ; аналогично и для арсената. Хотела уточнить нужно ли молярную концентрацию переводить в нормальную? Затем находим концентрацию ионов (ПИ), сравниваем с ПР.
А вот с массой я совсем запуталась... Помогите разобраться и проверить ход моих действий!
-
Вы мне очень помогли!!! Спасибо Вам огромное!!!2CH3-COO-C2H5 --(NaOC2H5, -C2H5OH)--> CH3-CO-CH2-COO-C2H5
CH3-CO-CH2-COO-C2H5 --(HCN, KCN)--> NC-C(OH)(CH3)-CH2-COO-C2H5
NC-C(OH)(CH3)-CH2-COO-C2H5 --(H2O, H+, -NH4+, -C2H5OH)--> HOOC-C(OH)(CH3)-CH2-COOH
Сначала надо ввести в АУЭ нужные радикалы.
CH3-CO-CH2-COOC2H5 --(NaOC2H5, -C2H5OH)--> [CH3-CO-C-H-COOC2H5]Na+ (натрийацетоуксусный эфир)
[CH3-CO-C-H-COOC2H5]Na+ + C2H5-Br --(-NaBr)--> CH3-CO-CH(C2H5)-COOC2H5
Кетонное расщепление:
CH3-CO-CH(C2H5)-COOC2H5 --(NaOH разб., t)--> CH3-CO-CH2-CH2-CH3 + Na2CO3 + C2H5OH
[CH3-CO-C-H-COOC2H5]Na+ + CH3-Br --(-NaBr)--> CH3-CO-CH(CH3)-COOC2H5
Кислотное расщепление:
CH3-CO-CH(CH3)-COOC2H5 --(NaOH конц., t)--> CH3-CH2-COONa + CH3COONa + C2H5OH
CH3-CH2-COONa --(HCl)--> CH3-CH2-COOH
-
У меня еще возникли затруднения насчет схемы синтеза - 1)из этилацетата получить 2-окси-2-метилбутандиовую кислоту.
А в этом задании я просто не могу понять, 2)необходимо получить метилпропилкетон; пропионовую кислоту, исходя из ацетоуксусного эфира, нужно ведь использовать разбавленный (в первом случае) NaOH, а во втором концентрированный, но сразу эти продукты не получаются.
-
Огромное спасибо!!!OHC-CHO + 2HCN --(KCN)--> NC-CHOH-CHOH-CN --(H2O, H+, -NH4+)--> HOOC-CHOH-CHOH-COOH
СH2OH-CHOH-CH2OH --(2HCl)--> СH2Cl-CHOH-CH2Cl (реакция достаточно селективная - вторичный гидроксил в глицерине замещается труднее первичных)
СH2Cl-CHOH-CH2Cl --(K2Cr2O7, H2SO4)--> СH2Cl-CO-CH2Cl (описанный в литературе способ синтеза симметричного дихлорацетона)
СH2Cl-CO-CH2Cl + 2KCN --(-2KCl)--> NC-СH2-CO-CH2-CN
NC-СH2-CO-CH2-CN + HCN --(KCN)--> NC-СH2-C(OH)(CN)-CH2-CN
NC-СH2-C(OH)(CN)-CH2-CN --(H2O, H+, -NH4+)--> HOOC-СH2-C(OH)(COOH)-CH2-COOH
-
-
Спасибо большое!Читаем "чтобы после заполнения водой до метки раствор стал 0,5 N" - значит надо получить объем 200 мл с концентрацией 0,5 моль/л.
Далее: n =C*V - считаете, сколько эквивалентов (=молей) должно стать в колбе
-
как это определить?
-
-
-
-
я не могу найти продукты, что может получится в ходе реакции?)))Скорее всего, просто кислотно-основная реакция. Пикриновую кислоту часто применяют для осаждения солей аминов, особенно с гидрофобными заместителями.
-
помогите написать уравнение, ничего не получается(
-
А потом посмотреть,в каких случаях E больше, и сделать вывод идет ли реакция или нет???А теперь складывайте соответствующие полуреакции и потенциалы.
Стоп. Тут не та полуреакция с железом. Оно окисляется до Fe3+
-
и что делать дальше??Fe+2+2e=Fe, E=-0,440
I2+2e=2I-, E=0,535
Cl2+2e=2Cl-, E=1,36
-
Fe+2+2e=Fe, E=-0,440Для начала напишите полуреакции и их потенциалы
I2+2e=2I-, E=0,535
Cl2+2e=2Cl-, E=1,36
-
Можно ли окислить ионы Fe+2 хлором,йодом в стандартных условиях? в обосновании ответа приведите стандартные потенциалы полуреакций
Помогите разобраться!!!
-
Спасибо большое за подробное описание решения задачи!!! Очень Вам благодарна!!!7.2*10-2 Н/м (для 20 оС вроде все же 7.28*10-2), т.е. 0.072. Отнимаете 0.0433 от 0.072(8)
-
Значит,если поверхностное натяжение воды равно 72,то мы отнимаем 4,33*10-2 от 72???Ну это некая дурь из серии как по одному значению найти производную. Решается через уравнение изотермы адсорбции Гиббса. Нужна упрощенная форма, записываемая через концентрации. Можно посмотреть здесь:

Чтобы посчитать производную, надо знать изменение поверхностного натяжения при изменении концентрации ПАВ. Напрашивается изменение σ от значения для чистой воды (взять из справочника) до значения 4,33*10-2 Н/м, получившегося при введении 0,056 моль/л ПАВ. Разность σ делим на 0,056, получаем как бы производную. То есть, при таком подсчете по разностям мы реально получим производную в некоторой промежуточной точке взятого интервала независимой переменной. Авторы задачи, очевидно, полагают, что ровно в середине этого интервала, т.е. при концентрации ПАВ 0,028 моль/л. Ну, ничего не остается, как так и принять. Значит, производная у нас есть, подставляем концентрацию 0,028 моль/л и прочие величины в формулу, считаем адсорбцию. Точность результата будет плюс-минус километр.
-
подскажите решение!!!!Поверхностное натяжение водного раствора поверхносто-активного вещества с концентрацией 0,056 моль/л при 293 К равно 4,33*10-2 Н/м. Вычислите адсорбцию этого вещества из раствора с концентрацией 0,028 моль/л при 293 К.
Помогите пожалуйста!
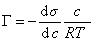
Комплексонометрическое титрование(определение процентного содержания CaCO3, MgCO3
в Решение заданий
Опубликовано
помогите разобраться!