
venisyella1995
-
Постов
57 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные venisyella1995
-
-
http://znanija.com/task/492176
я вот смогла наити, хочешь посмотреть, тут есть данная реакция
ребята, кто нибудь может помочь
1) Mg->CH3MgJ->CH3MgJ->CH3COOMgJ->MgJCl
2)в организме взрослого человека содержится около 20 г катионов магния, а кальция 1000г. вычислите массовую долю кальция и магния в организме человека, масса которого 75 кг.
-
да это реакция поидет
2fe2o3+3c=4fe+3co2 - реакция замещения
-
1) Mg-CH3MgJ-CH3COOMgJ-MgJCl
2)в организме взрослого человека содержится около 20 г катионов магния, а кальция 1000г. вычислите массовую долю кальция и магния в организме человека, масса которого 75 кг.
-
Спасибо, вам большое
-
нет, я подобную не писала,
machdems у меня просто с этим не очень хорошо, но я очень была бы вам благодарна, если бы вы мне помогли, с этой проблемой, дело в том, что я написала реакцию но дальнейший ход решения не знаю
-
Если честно, я ни чего не поняла, просто у меня не очень хорошо, это получается, и может вы мне по порядку будете говорить, что делать
-
1) уравнение реакции будет
2К+2H2O=2KOH+H2( выделиться)
больше я ни чего не знаю
-
1) Навеску калия массой 0,39 г опустили в химический стакан с водой. вычислите массу и объем выделившегося водорода образовавшейся щелочи
2) вычислите массу натрия , который можно получить электролизом 1 кг расплава поваренной соли, если выход натрия составит 75%
3)вычислите выход натрия , если в ходе электролиза 500г расплава поваренной соли удалось получить 100 г натрия
4) вычислите объем этанола ( плотность 0,8 г/см3), который потребуется для утилизации 100 г натрия
5) вычислите массу натрия и 10%-го раствора гидроксида натрия, которые потребуются для приготовления 400г 20%-го раствора гидроксида натрия
6) вычислите массу натрия , который необходимо добавить к 50 г 10%-го раствора гидроксида натрия , чтобы получить 20%-й раствора гидроксида натрия
-
ну ошиблась, будто вы не разу не ошибались
-
-
Не много
попробуй ввести саму реакцию в поисковик в яндексе, или в гугле, и посмотри что он тебе выдаст
-
вы сомневаетесь на счет второго уравнения Ca(OH)2+SO3=Ca2SO3+H2O? почему вас это смущаетCa2SO3?
-
a) 2KOH + SO3 → K2SO4 + H2O
б) Ca(OH)2+SO3=Ca2SO3+H2O
в)точно не знаю
-
пример 1
Окислительно-восстановительная реакция между водородом и фтором

Разделяется на две полуреакции:
1) Окисление:

2) Восстановление:
 пример 2
пример 2 (NH4)2CrO4® Cr2O3 + N2 +H2O + NH3
Решение
2 (NH4)2CrO4 = Cr2O3 + N2 +5 H2O + 2 NH3
CrVI + 3 e- = CrIII 2
2N-III - 6 e- = N20 1 пример 3 2 H2S + SO2 = 3 S + 2H2O S-II- 2 e- = S0 2
SIV + 4 e- = S0 1 пример 4 4 Fe(S)2 + 11 O2 = 2 Fe2O3 + 8 SO2 FeII- e- = FeIII-11 e- 4 2S-I- 10 e- = 2SIV O20 + 4 e- = 2O-II + 4 e- 11 пример 5
FеS2 + НNO3(конц) →Fе(NO3)3 + Н2SО4 + NО2.
Fe+2 – e → Fe+3
2S- - 14e → 2S+6.
Вместе железо и сера отдают 15 электронов. Полный баланс имеет вид:

15 молекул НNО3 идут на окисление FеS2, и еще 3 молекулы НNО3 необходимы для образования Fе(NО3)3:
FеS2 + 18НNО3 → Fе(NО3)3 + 2Н2SО4 + 15NО2 .
Чтобы уравнять водород и кислород, в правую часть надо добавить 7 молекул Н2О:
FeS2 + 18НNО3(конц) = Fе(NО3)3 + 2Н2SО4 + 15NО2 + 7Н2О.
Используем теперь метод электронно-ионного баланса. Рассмотрим полуреакцию окисления. Молекула FеS2 превращается в ион Fе3+ (Fе(NО3)3 полностью диссоциирует на ионы) и два иона SO42- (диссоциация H2SO4):
FeS2 → Fe3+ + 2SO24-.
Для того, чтобы уравнять кислород, в левую часть, добавим 8 молекул H2O, а в правую – 16 ионов Н+ (среда кислая!):
FeS2 + 8H2O → Fe3+ + 2SO42- + 16H+.
Заряд левой части равен 0, заряд правой +15, поэтому FеS2 должен отдать 15 электронов:
FеS2 + 8Н2О - 15е → Fе3+ + 2SО42- + 16Н+.
Рассмотрим теперь полуреакцию восстановления нитрат-иона:
NO-3 → NO2.
Необходимо отнять у NО3- один атом О. Для этого к левой части добавим 2 иона Н+ (кислая среда), а к правой — одну молекулу Н2О:
NО3- + 2Н+ → NО2 + Н2О.
Для уравнивания заряда к левой части (заряд +1) добавим один электрон:
NО3- + 2Н+ + е → NO2 + Н2О.
Полный электронно-ионный баланс имеет вид:

Сократив обе части на 16Н+ и 8Н2О, получим сокращенное ионное уравнение окислительно-восстановительной реакции:
FеS2 + 15NО3- + 14Н+ = Fе3+ + 2SО42- + 15NО2 + 7Н2О.
Добавив в обе части уравнения соответствующее количество ионов по три иона NО3- и Н+, находим молекулярное уравнение реакции:
FеS2 + 18НNО3(конц) = Fе(NО3)3 + 2Н2SО4 + 15NО2 + 7Н2О.
-
помогите пожалуйста
-
1)Пластинку из алюминия массой 27,0 г поместили в 240,8 г раствора хлорида меди (II). Через некоторое время пластинку вынули и высушили, осадок на дне сосуда отфильтровали и тоже высушили. Масса пластинки и осадка составила 40,8 г. Вычислите массу алюминия, растворившегося в ходе реакции, массу восстановившейся меди и массовую долю сульфата алюминия в растворе после реакции.2). Цинковую пластинку поместили в 248,2 г раствора сульфата железа(II). Через некоторое время пластинку вынули и высушили, осадок на дне сосуда отфильтровали и тоже высушили. Масса пластинки с осадком по сравнению с исходной массой пластинки уменьшилась на 1,8 г. Вычислите массу цинка, перешедшего в раствор, массу восстановившегося железа и массовую долю сульфата цинка в растворе после реакции.2)Пластинку из некоторого металла массой 50 г опустили в 208 г раствора сульфата железа (II). Через некоторое время пластинку и осадок высушили и взвесили. Масса пластинки с осадком оказалась равной 58 г. В растворе появился сульфат металла, в котором степень окисления металла равна +2. Массовая доля сульфата металла равна 1 5 %. Из какого металла изготовлена пластинка?В этой и последующих задачах условно будем считать, что весь восстановленный металл остается на пластинке, если в условии задачи не обозначены другие особенности осаждения металла.3)Пластинку из некоторого металла массой 1 00 г опустили в 51 5,2 г раствора нитрата серебра. Через некоторое время пластинку и осадок металла высушили и взвесили. Масса пластинки с осадком оказалась равной 1 15,2 г. В растворе появился нитрат металла, его массовая доля равна 3,76%. Степень окисления металла в нитрате равна +2. Из какого металла сделана пластинка?4)Железную пластинку массой 20 г поместили в 1 2 %-й раствор нитрата серебра массой 80 г. Через некоторое время пластинку вынули, высушили и взвесили. Рассчитайте, какова должна быть масса пластинки после реакции, если массовая доля нитрата серебра в растворе уменьшилась до 8 %.
-
Если честно, задачи я решаю не очень хорошо, точнее я их просто не понимаю... я очень быстро пишу реакции ,но задачи это моя слабость... И я надеюсь на вашу помощь....
-
я знаю, просто там такая тема уже есть, и он ее не принимал. Помоги мне пожалуйста, я тебя очень прошу. пожалуйста
-
1)Пластинку из алюминия массой 27,0 г поместили в 240,8 г раствора хлорида меди (II). Через некоторое время пластинку вынули и высушили, осадок на дне сосуда отфильтровали и тоже высушили. Масса пластинки и осадка составила 40,8 г. Вычислите массу алюминия, растворившегося в ходе реакции, массу восстановившейся меди и массовую долю сульфата алюминия в растворе после реакции.2). Цинковую пластинку поместили в 248,2 г раствора сульфата железа(II). Через некоторое время пластинку вынули и высушили, осадок на дне сосуда отфильтровали и тоже высушили. Масса пластинки с осадком по сравнению с исходной массой пластинки уменьшилась на 1,8 г. Вычислите массу цинка, перешедшего в раствор, массу восстановившегося железа и массовую долю сульфата цинка в растворе после реакции.2)Пластинку из некоторого металла массой 50 г опустили в 208 г раствора сульфата железа (II). Через некоторое время пластинку и осадок высушили и взвесили. Масса пластинки с осадком оказалась равной 58 г. В растворе появился сульфат металла, в котором степень окисления металла равна +2. Массовая доля сульфата металла равна 1 5 %. Из какого металла изготовлена пластинка?В этой и последующих задачах условно будем считать, что весь восстановленный металл остается на пластинке, если в условии задачи не обозначены другие особенности осаждения металла.3)Пластинку из некоторого металла массой 1 00 г опустили в 51 5,2 г раствора нитрата серебра. Через некоторое время пластинку и осадок металла высушили и взвесили. Масса пластинки с осадком оказалась равной 1 15,2 г. В растворе появился нитрат металла, его массовая доля равна 3,76%. Степень окисления металла в нитрате равна +2. Из какого металла сделана пластинка?4)Железную пластинку массой 20 г поместили в 1 2 %-й раствор нитрата серебра массой 80 г. Через некоторое время пластинку вынули, высушили и взвесили. Рассчитайте, какова должна быть масса пластинки после реакции, если массовая доля нитрата серебра в растворе уменьшилась до 8 %.
-
большое спасибо вам ребята, я вам так благодарна...))) огроменное..))
-
1) Напишите уравнения реакций, с помощью которых можно получить:б) цинк из сульфида цинка;в) железо из дисульфида железа (II);г) натрий из хлорида натрия;д) натрий из гидроксида натрия.
2)Навеску некоторого металла массой 11,2 г растворили в избытке соляной кислоты. В результате выделился водород объемом 4,48 л (н. у.) и образовался дихлорид металла. О каком металле идет речь?
3)Навеску некоторого металла массой 12,0 г растворили в избытке соляной кислоты. В реакции выделился водород объемом 11,2л (н. у.) и образовался сульфат металла, в котором степень окисления металла равна +2. О каком металле идет речь?4)Навеску некоторого металла массой 14 г сожгли в хлоре. В результате образовался трихлорид этого металла массой 35,3 г. О каком металле идет речь? Что вы знаете об истории открытия этого металла?5)Для утилизации 7,8 г некоторого щелочного металла провели его взаимодействие с водой. Для нейтрализации образовавшейся щелочи был затрачен 1 0 %-й раствор азотной кислоты массой 126 г. О каком щелочном металле идет речь? Найдите объем такой порции щелочного металла. Какие меры предосторожности надо соблюдать при выполнении такого опыта? Как правильно утилизировать щелочные металлы?6).Пластинку из железа массойт1г опустили в раствор сульфата меди (II). Через некоторое время пластинку вынули, высушили и взвесили. Ее масса оказалась равнойт2г. Вычислите массу железа, перешедшего в раствор, и массу меди, осевшей на пластинке", если значенияm, иm2соответственно равны: а) 10,0 г и 10,8 г; б) 20 г и 22 г; в) 1 2 г и 1 3 г; г)"50 г и 54 г. -
спасибо)) большущее))
-
1)какую массу воды потребуется разложить электрическим током,что бы полученным кислородом можно было сжечь 16г серы?
2)какая масса пергидроля 30% раствора пероксида водорода ) потребуется для получения кислорода,достаточного для сжигания 8 г серы?
-
1)Вычислите массу воды, необходимую для гидротации 1 л этилена (25 oC, 101,3 кПа)?
2)кусочек натрия массой 4,6 г добавили к 200 гр воды вычислите массовую долю и молярную концентрацию гидроксида натрия в растворе после реакции.( плотность раствора примите равной 1,0 г/см3)?
3)оксид кальция массой 0,56 г добавили к 500 г воды. вычислите массовую долю гидроксида кальция в растворе. (плотность раствора примите равной 1,0 г/см3)?
4) в кристаллогидрате сульфата натрия массовая доля воды составляет 55,9%. составьте формулу кристаллогидрата сульфата натрия?
5)в кристаллогидрате сульфата марганца (II) массовая доля воды составляет 45,5%. составьте формулу кристаллогидрата сульфата марганца (II)?


 пример 2
пример 2 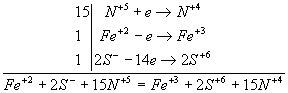
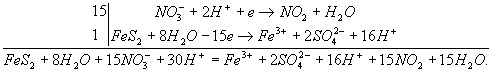
органика.реакции
в Решение заданий
Опубликовано
если честно я на счет первого сама не уверена, но в любом случае спасибо, я тебе так благодарна