-
Постов
61 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные join
-
-
Помогите, пожалуйста, нарисовать механизм для данной р-и. Имидазол, я так понимаю, хороший нуклеофуг? От этого отталкиваться?
-
Могу предположить что это можно объяснить стерическим фактором, т.е. размер V(4+) настолько мал, что, чтобы координировать вокруг себя определенные остатки, он присоединяет кислород, для увеличения размера катиона. Но сказали, что это нужно объяснить исходя из электронной конфигурации атома. Как это лучше сделать?
-
-
Реакции с жидким SO2
-
И какая форма ожидается? Т-образная, или просто плоский треугольник?
-
-
-
Травеня скачайте в главе стереоизомерии хорошо написано
Большое спасибо, почитал, все очень доходчиво!
-
-
-
с концентрированной и горячей - нитрат железа (III), фосфорная и серная кислоты.
Спасибо!
-
Какие продукты возможны?
-
А под аминоуксусным ангидридом подразумевается H2N-CH2C(O)-O-C(O)-CH2NH2?
Если да, то он гидролизуется в воде до глицина, а потом глицин образует гидрохлорид по азоту.
Да, именно об этом веществе.
-
Соляная кислота это раствор HCl в воде. Так что скорее всего, никакого ангидрида там уже не будет.
То есть, вы считаете, что даже в теории ангидрид не будет реагировать с HCl?
-
-
-
Всё зависит от концентрации соляной кислоты. В разбавленной кислоте возможна реакция диспропорционирования с образованием MnO2, KMnO4 и KCl .
в том то и проблема, в задаче не указана концентрация..
-
-
Какие все таки продукты этой реакции?
-
При прокаливания оксид меди(II) разлогается
-
Оксид меди разложится на оксид одновалентной меди и кислород, на сколько я знаю, да?
-
C3H3Br4 - не существует, т.к. сумма чисел атомов H и Br - нечетное. Нет и углеводородов с нечетным числом атомов водорода (C3H3)
А вот HC≡C-CH2-CH2-C≡CH - очень похож
Хм, в принципе да. И молекулярная формула как раз C6C6Br8

-
А полностью условие есть?
Да. Вот: Углеводород, который содержит 7,7% (по массе) водорода, присоединяет бром. Образуется вещество, которое имеет 89,2% брома. Известно также, что при действии натрия на углеводород, образуется производная, которая имеет два атома металла. Определить молекулярную формулу углеводорода, написать возможные структурные формулы, назвать их.
-
По условию вообще очень похоже на ацетилен. Количество атомов углерода и водорода равное (сказано что это углеводород и процент водорода составляет 7,7) и при взаимодействии с натрием получается производная с двумя атомами натрия, ну явно ацетилен. А при бромировании образуется вещество с содержанием брома 89,2%. А у тетрабромэтана 92%. Что ж это такое?


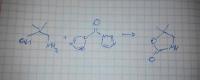
Механизм реакции карбонилдиимидазола с кислотами
в Решение заданий
Опубликовано
Каков механизм реакции карбонилдиимидазола с кислотами, если она протекает с декарбоксилированием кислоты, и получением имидазолида этой кислоты?