-
Постов
75 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Bastvil
-
Механические методы пока кажутся менее сложными для данной ситуации.
-
Приветствую. Так выходит, что всё больше задачек подкидывают мне своеобразных. Сегодня пришла тема экологичная. На производстве карбамида в стоке после десорбера (конечного аппарата очистки конденсата сокового пара от карбамида, аммиака и углекислоты) внезапно обнаруживается нитрит и нитрат ионы. В аппаратах до десорбера (гидролизёрах) отсутствуют нитрит-ионы, но имеются в большем количестве нитрат-ионов. Также в аппарат подаётся острый пар, получаемый в соседнем цехе производства азотной кислоты. Если не вдаваться далее в технические подробности (переточности т/о, качество методик анализа), то может ли в условиях десорбера, при t = 140 °С и P = 300÷500 кПа-а, идти реакция между аммиаком, СО2 (нитрификация)? Я же правильно понимаю, что не о какой жизнедеятельности бактерий в условиях десорбера говорить не приходится?
-
Применение карбамида для осушки? Интересно. Правда потребуется много испытаний, как выше писали "Разбираться с влагой". Те, кто задачу ставит, совсем мало знакомы со словом "промышленные эксперименты и испытания". Ведь улетающий аммиак - нужно уловить. Это опять аппарат, вода, сток. Нужно подобрать концентарцию карбамидного раствора. Это лабораторные испытания, много испытаний. Всё выливается в немалую сумму средств и сложность организации. Решение интересное, но для барыг засевших на заводах - не изящное. Им подавай куб 1 см х 1 см, который ничего не потребляет, и из которого под чудодейственной магией химии синтезируются зелёные купюры.
-
Понятно. Спасибо за пояснения. Да вот растворимость у соды отличная и по действующей схеме сейчас вся пыль из электрофильтра ссыпается в чан с водой, в котором растворяется и отправляется водным раствором на нужды производств. Тут проблема в том, что она отлично растворяется в воде, и я с трудом себе представляю скопление соли, пересыщенные растворы. Задача усложняется в таком варианте, как мне кажется. Особенно учитывая строгое требование в целом на производстве сокращать все стоки.
-
А вальцами разве не дробление происходит? Немного не представляю, как ими уплотняется материал? Лучше без увлажнения. Нужно повысить плотность так, чтобы получилось более плотное, но сухое вещество. Из-за особенностей процесса уже попадала увлажнённая сода в мешок. Там она превращается в отдельные крупные камни, а нужен всё-таки однородный сыпучий материал. Или идея состоит в увлажнении, а потом обработка вальцами? Интересная идея. Но вот не уверен, что смогу обосновать её применение, особенно конвейер, запретное слово. Посмотрим, может к ней вернёмся. Отметить как решение
-
Увлажнять можно, но боюсь появляется серьёзная угроза получить монолит в биг-беге, что должно быть исключено. Прессовать в формах? Пресс я рассматривал (в том числе и производство таблеток). Неплохой способ, но нам нужны не блоки и таблетки - а насыпь, а прессы заточены больше под них. Плюс весьма большой ценник на такую малышку. В любом случае спасибо за идеи. Пусть они сейчас и не пригодятся. Может в процессе к ним обратимся.
-
Здравия, товарищи форумчане. Нужен совет в области немного незнакомой для меня. Имеется электрофильтр, который улавливает пыль кальцинированной соды, далее эта пыль в виде пудры ссыпается в нижний конус под фильтром, где скапливается и после открытием шибера ссыпается в биг-бег/бункер (пока ещё неясно куда именно). Возник практический вопрос, как уплотнить данную пылевидную пудру с плотности ~400 кг/м3 до н/м 600 кг/м3? Наверняка кто-то сталкивался с подобной задачей. Первые мысли которые возникли - использование вибростола под биг-бегом. Но результата уплотнения ненадёжный. Поэтому сразу интересует вторая мысль - применение шнека с сужающим диаметром и увеличением числа витков к выходу и после ссыпка в биг-бег. Но с шнеками никогда не доводилось работать. К тому же слышал, что к ним в конце предусматривается регулируемая насадка, которая якобы может менять плотность выходящего материала чуть ли не на ходу. Также был бы признателен за литературу в которой эти вопросы по уплотнению на шнеке раскрывались. какая-нибудь библия шнековальщика Если есть ещё какие-либо способы, то с интересом послушал бы. Всё-таки твёрдая фаза мне совсем непривычна. Обычно работал с жидкостями-газами.
-
Да, согласен. Надо будет поспрашать про это. Отбираемая проба почти всегда с капельками в стеклянном отборнике, а как они эту пробу к анализу готовят (готовят ли?) и вводят - вопрос.
-
Методом хроматографии. Детали не скажу - делали не в моём присутствии. Методика проведения измерений может быть вполне ошибочной, тут удивляться не стоит.
-
Хотелось бы, чтобы она была равновесной (капельки выделяются на всём протяжении своего нелёгкого пути при ударе об стеночки на поворотах). А также хотелось бы это не считать, но требуют состав для расчёта оголовка (понятия не имею зачем и к чему для этого потребовались объёмные проценты). Уравнением Дмитрия Ивановича применял. Что-то вышло, но меньше, чем то, что считали забугорные гении в своих матбалансах. Интересно, что у них плотность газовой смеси принята в районе 12 кг/м3. Ладно, наверное задача требует ещё условий, которые надобно уточнить. Просто предполагал, что упускаю из виду какую-нибудь известную методику для конкретно таких вот своеобразных расчётов.
-
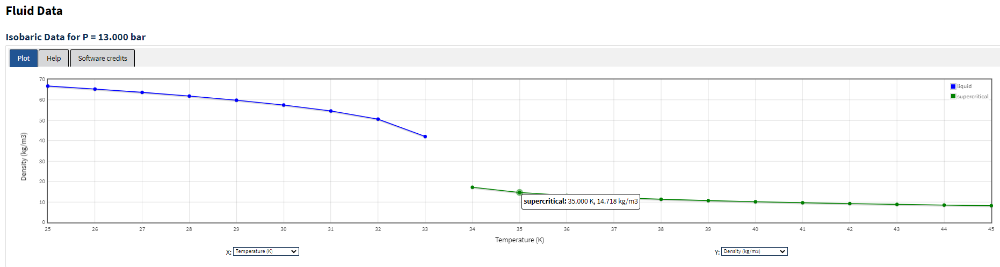
Здравствуйте, товарищи. Вопрос банальный, потому рука не дрогнула вписать его в этот раздел. Банальным он мне самому казался, пока не стал считать. Вот есть у нас газ, в котором содержится (для данного примера): 75 % мас. N2, 7 % мас. СО2 , 6 % мас. циклогексан, 3 % мас. СО, 2 % мас. кислород, 1 % мас. циклогексанон 1 % мас. циклогексанол и 5 % мас. воды. Как перевести эти значения массового содержания в объёмные? Параметры газа в точке измерения - 15 °С и 101,325 кПа-а. Первая мысль, которая сразу приходит на ум - через плотности (идеального газа из воды и органических компонентов не очень получится, если только как крайний случай). Берём условный вес смеси для пересчёта - 100 кг. Соответственно высчитываем вес каждого компонента в смеси. А потом берём плотности. Соответственно плотность азота, кислорода, углекислого газа и угарного газа при таких параметрах вопроса не вызывают - они находятся в газообразном состоянии. Тут всё ясно. Но вот встал вопрос в другом - а какая плотность будет у циклогексана, циклогексанола, циклогексанона, ежели при таких параметрах они сконденсированные и жидкие. Т.е. тут стоит уточнить - газ идёт после очистки абсорбцией, и органика попадает как "унос". И с этого момента мне не совсем понятна физическая природа уноса - вещества, которые уносит газ являются газообразными по своим свойствам или жидкими? К тому же у меня вызывает некоторое непонимание то, что имеются экспериментальные данные по плотности газообразного циклогексана при 15 °С соответствует ~18 кг/м3. Я представил себе это как плотность паров циклогексана при равновесии в состоянии насыщения для 15 °С (что значит давление значительно ниже атмосферного), однако в электронном справочнике мне для равновесного (насыщенного) состояния при 15 °С выдало плотность ~0.29 кг/м3. И тут я совсем запутался. Т.е. 18 кг/м3 это что-то вроде недогретых паров или как? А всё начиналось так просто - % мас. в % об. В общем мог бы уже забить, пересчитав через молярные объёмы, но хочется разобраться в этом моменте. Может кто подсказать?
-
Во. Теперь понятнее. Для меня просто это казалось одним и тем же состоянием, если преодолена критическая точка (сверхкритический флюид и "сверхкритический газ"?). Ближе к "жидкому" виду такое агрегатное состояние приближается, когда плотность флюида равна или больше критической плотности (плотности в критической точке) как я понимаю? Выходит это состояние хоть и однородно, но видимо в разных частях диаграммы фазового состояния - оно обладают разными "ощутимыми" свойствами на краях этой диаграммы (большая компонента давления ближе к жидкости - большая компонента температура ближе к газу)? Эх, как-то в руки не попадался букварь, который бы вот это всё подробно разжёвывал. Ну, дак. Я хотя бы теперь смогу подкалывать на производстве технологов, что они не знают, что у них компрессора качают. Это ж какой простор теперь открывается.
-
Интересно. Это значит справочник NIST обманывает меня, называя плотность ниже критической плотности "сверхкритический флюид"? Ну я в начале писал - умозрительный интерес. Простой вопрос с одной точки зрения. Просто занимался расчётами тепловых потоков и обнаружил, что водород в моих расчётах оказывается в необычной области сверхкритической жидкости. Вот и решил поспрашать народ - может всё-таки неправильно понял сущность вопроса.
-
Интересно. Я думал критическая точка является константой для индивидуального вещества. Т.е. для сверхкритической жидкости важно ещё соответствие критической плотности?
-
Я понимаю, что это не будет обычной жидкостью. Даже на морозе. Речь идёт о том, будет ли он сверхкритической жидкостью? Как это понять.
-
Согласен. Но и газообразным он получается не является. Не совсем. Водород при температуре 32К и давлении ниже 1297 кПа будет также полноценной жидкостью. И водород при давлении выше 1297 кПа, но с температурой ниже 33,15К - тоже полноценная жидкость. А всё остальное - сверхкритический флюид. Я имел ввиду два условия получения критического флюида.
-
Ну исключим разночтение. 33,15 К - критическая температура водорода. Температура на нагнетании компрессора +/- 333 К. Получается в десять раз превышает границу перехода в критическое состояние водорода по температуре. Если я правильно понимаю - всё, что имеет температуру ниже 33,15 К и одновременно давление ниже 1297 кПа-а - является полноценным газом/жидкостью. В случае компрессоров - и давление, и температура одновременно превышают критические параметры и, следовательно, водород находится на нагнетании в состоянии сверхкритического флюида.
-
Меня засмущал в этом тот факт, что визуально флюид выглядит как жидкость (смотрел видео с СО2).
-
Здравствуйте форумчане. Заходите, присаживайтесь. Чайку кому? Вопрос чисто умозрительный (и предположения, что он может меня скоро коснуться Оо). Есть у нас водород, который приобретает свойства сверхкритической жидкости при достижении параметров: 240,2 -°С и 1297 кПа-а. Далее есть компрессор поршневой нагнетающий водород до 1800 кПа при температуре 50-60 °С. Я правильно понимаю, что компрессор на выходе выдаёт сверхкритический флюид, а не газообразный водород? И ещё дополнительно - если в водороде появляются примеси (например органические вещества или азот в пределах =/- 1 % мас. - будет ли это как-то влиять на агрегатное состояние водорода?
-
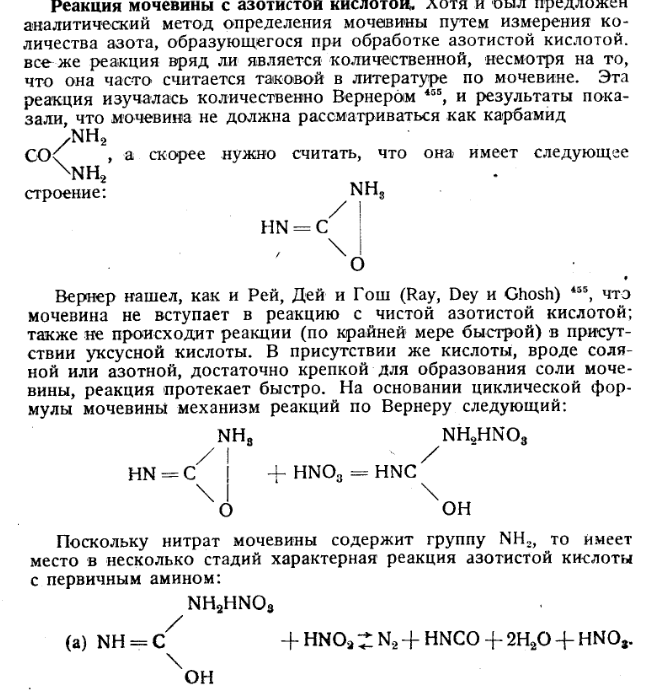
Нашёл отрывок из книги, решил закинуть в улей. Всё-равно скучаете.
-
-
Хорошая статья, но, к сожалению, для диапазона до 27 °С. Её я имел ввиду говоря о низких температурах теплоёмкости (фазовый переход твёрдое -> жидкое). NIST данные собирал. Тоже проблема - все значения в незначительном температурном диапазоне. А как же вездесущие исследования для советских справочников для работников химической промышленности?) Слышал, что исследования в БССР или СССР где-то проводились и куда-то делись. Вроде направление их исчезновения было в сторону западных демократий. Но там "молчат" об их судьбе. Только ценниками машут перед физиономией.
-
Приветствую форумчане. Долго занимался поисками в различных местах (возможно недостаточно хорошо) значений зависимости теплоёмкости циклогексанона/циклогексанола от температуры (о давлении и не мечтаю). И возник вопрос из наблюдений при изучении научных работ связанных с изучением теплоёмкости для циклогексанола/циклогексанона в зависимости от температуры - и вот есть неплохие данные теплоёмкости (Ср) для твёрдых и газообразных состояний циклогексанола/циклогексанона, но практически нет возможности найти теплоёмкости в зависимости от температуры для жидкого состояния данных веществ (да, я знаю о данных Голубева из "Производство капролактама" Овчинникова-Ручинского и парочка значений из иностранных справочников). В чём причина? Почему скрупулёзно изучаются области -40 °С и 300-1000 °С, достижение которых весьма затруднительно в лабораторных условиях, но при этом в научных публикациях мёртвая тишина о самом обычном состоянии в пределах 20-150 °С? Табу маркетинга продажи пакетов физико-химических свойств компонентов? Или что-то ещё?
-
Если катализатор не пирофорен после прожига - то сухой азот избыточное удовольствие. Если на производстве имеется подобие воздуха для пневматике с контролируемой точкой росы - то можно попробовать использовать его.
-
Ну, если в реакции образуется вода, а кислотный остаток без изменений переходит к Mg+, то стоит. Энергии там выделяется очень много, лично проверял, небольшая засыпка в колбу слабой азотной кислоты происходит бурно с вспениванием и выделением рыжих окислов, если не попытаться охладить. Учитывать нужно полное разрушение кристаллической решётки и растворение всего вещества, за исключением нерастворимого шлама в составе ПМК-83 (там нужно поискать ТУ, вроде указывалась доля примесей). Реакция должна включать в себя выделение тепла от растворения, от самой реакции и от разбавления раствора до нужной концентрации. Учитывать разбавление водой стоит, т.к. раствор готовится порционной заливкой воды, кислоты, засыпкой кислоты и после доливка воды по тому, как проходит реакция (т.е. сколько фактически воды выделится в процессе). Как раз данный фактор, который не учитывался на производстве (выделение воды в реакции) стал причиной больших экономических затрат в цехе на последующую упарку соли, в которую вводилась, без должного контроля, слишком разбавленная добавка Mg/Ca(NO3)2. Откуда требование вести процесс при 80 оС? Если мне не изменяет память, то данная температура максимальная и нежелательная для данного процесса. Реакция идёт бурно, системе достаточно и 50 оС. На практике, конечно, такое встречается на старых производствах, где процесс ведётся при 90 оС, вызывая неконтролируемые выбросы окислов в атмосферу, но это плохой пример ведения реакции. Технология хорошо работает и с дозировочным шнеком, циркуляционным насосом с холодильником, поддерживающим температуру 40-60 оС в зоне реакции. В такой ситуации окислы тоже выделяются, но уже значительно меньше. Данные по равновесным долям выделяемых окислов при различных температурах можно попробовать поискать, но эти потери на практике проще считать в виде общих производственных потерь по затратам азотной кислоты и выходу добавки - средний анализ шлама на содержание натрат-нитритных групп. Впрочем если порыться, то попадаются такие исследования: https://cyberleninka.ru/article/n/desorbtsiya-oksidov-azota-iz-produktsionnoy-azotnoy-kisloty-58-60-mass по которым можно, собрав предварительно данные из реального процесса, сделать оценку выделения окислов азота при различных режимах приготовления добавки. Визуально в отобранной из трубы слабой азотной кислоте при 50 оС содержится тонкий слой окислов всегда, так что тут условно потери начинаются уже с момента выхода свежеприготовленной азотной кислоты, что делает задачу ещё более сложной, в то время как влияние этого процесса на тепловой баланс стремится к нулю.