-
Постов
285 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Sejay358
-
Я впитал эту информацию. А вы почитайте ниже. Таблица. Столбик назван "ВЕЩЕСТВО". Азот - 14 г/моль. Вещество азот, у которого формула N2 имеет молярную массу не 14, а 28 г/моль! То же самое и с кислородом, и с водородом. Столбик же не озаглавлен "Молярная масса атомов и веществ", а "Вещество". Значит, они написали, что вещество азот имеет молярную массу 14г/моль. Да и потом, цитата: Моля́рная ма́сса вещества — масса одного моль вещества. Для отдельных химических элементов молярной массой является масса одного моль отдельных атомов этого элемента. В этом случае молярная масса элемента, выраженная в г/моль, численно совпадает с массой атома элемента, выраженной в а.е.м. (атомная единица массы). (Ну, здесь имеется в виду атомы металлов, т.к. они не соединяются в молекулы и атомы инертных газов, они же и молекулы) Однако надо чётко представлять разницу между молярной массой и молекулярной массой, понимая, что они равны лишь численно и отличаются по размерности. Как можно говорить, что элемент имеет молярную массу?? Он имеет а.е.м., и таки да, она в некоторых случаях (металлы и инертные газы) совпадает с молярной массой. Поэтому говорить, что элемент азот имеет молярную массу - некорректно. Да и потом, в вики есть страница и про а.е.м. Надо было туда и вписать о.а.м. элементов, зачем их сюда всовывать? Разве правильно включать в таблицу и элементы, и молекулы, при этом называя элементы веществом, а также говоря, что элементы имеют молярную массу???
-
Блин, ну конечно если много его получить, то он будет опасным. Я же не советую, блин, покупать пол литра нашатырного спирта и литр йода и смешивать. Я разве говорил про большие количества? Насчет оглушения - если брать полкило, как вы говорите, то, по моему, и так понятно, что полкило может оглушить. Если же вы имели в виду, что маленькое на фильтре количество йодистого азота может оглушить, то вы говорите полный бред. Петарда по сравнению с таким малым количеством хлопает громче, сам сравнивал. А малое кол-во йодистого азота щелкает с такой громкостью, как ломается пластмассовая линейка. Ну, в подъезде акустика хорошая, там он погромче хлопнет, как петарда, тоже сам проверял)). Понятно, в больших количествах опасен. Но все же получение йодистого азота в небольшом количестве безопасно. Сам проверял. Я писал уже, у меня фильтр в руках взорвался, никакой даже боли не было, просто хлопнул как надувной шарик. Такое малое кол-во не может принести какой-нибудь вред.
-
http://ru.wikipedia.org/wiki/%D0%9C%D0%BE%D0%BB%D1%8F%D1%80%D0%BD%D0%B0%D1%8F_%D0%BC%D0%B0%D1%81%D1%81%D0%B0 Что за хрень??? С каких пор молярная масса азота N2 14 г/моль? Водорода H2 - 1 г/моль??? А главное - углекислый газ написали правильно - 44 г/моль. Вот дол...бы писали это!
-
Короче, директор немного ошибся, как я понял, в этой школе лаборатория была лучшей всегда. И была она всегда, т.е. открыли её уже давно. Там периодически обновляют оборудование, говорят, там классно, оно современное, хорошее, раз все ребята туда на практику приезжают. Правда, я там еще не был. А вот новый крутой учитель действительно будет вести факультатив!
-
А собственно почему не советуете? Ну в маленьких количествах он безопасен. Я сам при своём знакомстве с химией получал йодистый азот, это был мой второй по счету синтез. (Ну синтез это громко сказано конечно))). Ну, а я брал вроде 10 мл йода и гидроксида аммония (да, пропорции не соблюдены), смешивал, отфильтровывал и оставлял сушить в подъезде. Достаю потом фильтр, а он у меня в руках хлопает. Ну, понятно, что его было очень мало, чтобы нанести мне хоть какой-нибудь вред. Потом я уже научился обращаться с ним аккуратно. Но нужно учесть, что он ОЧЕНЬ нестабильный, взрывается от малейшего прикосновения. Так что DinoMat, можете попробовать, но не берите много йода и нашатырного спирта, 5-10 мл хватит.
-
Поздравьте меня! Как я уже говорил, я недавно переехал из Молдовы, из Кишинёва в Беларусь, Минск и ПОСТУПИЛ В ЛУЧШУЮ ШКОЛУ! Там отличные преподаватели по химии, есть кандидат наук. Как раз в этом году открыли современную химическую лабораторию, куда будут приезжать заниматься химики со всех школ, и даже университетов Минска! УРРРААА!!! :D :ce: :cq:
-
Как бы там ни было, под фотой подписано "Кварц", нет указания на то что это монослой. В любом случае, надо указывать структуру полностью, а не частично. Что я и исправлю.
-
Вот ещё одна ошибка, она указывалась в моей теме Химические связи. Вот собственно ссылка (страница Оксид кремния), http://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D0%BA%D1%80%D0%B5%D0%BC%D0%BD%D0%B8%D1%8F(IV), где указано такое строение оксида кремния: Каждый атом кремния должен быть соединён с 4-мя атомами кислорода, а не с 3-мя, как показано здесь. Надо исправить ошибку (залить другую картинку). Я кстати недавно учебники получил, там в учебнике по химии как раз была правильная картинка. Могу залить её на Вики.
-
Анекдот в тему: Прочитал на шампуне надпись - "Длина и сила". Конечно, маловероятно, но решил мазать им не только волосы...
-
Да, мой вопрос может звучать, как от Кэпа, я его уже задавал, правда в другой теме, но: Вы эти ошибки потом исправляете или просто говорите о них???
-
Ещё раз отвечаю на аналогичное сообщение от chip7277: Неправильная реакция. Правильная выглядит так: 2NaCl + 2H2O => эл. ток => 2NaOH + H2 + Cl2 Причём не понимаю, как можно было ошибиться, если сами же писали правильную в теме про получение гипохлорита. Самое ржачное - где в вашей реакции хлор, чтобы можно было утверждать что он с чем-то прореагирует? В итоге, если не использовать диафрагму, получится раствор щёлочи с небольшой примесью гипохлорита натрия, т.к. выделяющийся с анода хлор, пока будет всплывать в растворе, частично прореагирует с щёлочью. Для того, чтобы раствор содержал только гипохлорит, нужно, чтобы хлор подольше реагировал с раствором щелочи, дольше находился с нею в непосредственном контакте. Так вся щелочь прореагирует с хлором и получится раствор гипохлорита натрия.
-
Неправильная реакция. Правильная выглядит так: 2NaCl + 2H2O => эл. ток => 2NaOH + H2 + Cl2 Причём не понимаю, как можно было ошибиться, если сами же писали правильную в теме про получение гипохлорита. Это я про электролиз. Электролизом затратно, если нет халявного или дешёвого источника мощного постоянного тока. А если имеется в виду гидролиз, то тоже бред, соли сильного основания и сильной кислоты не гидролизуются.
-
Да, я уже понял, просто тупанул поначалу)). Вечером активность мозга снижается. :co: А может быть так что не метил, а CH2 группа, например, ну, показанная в виде "излома", но волнистого, подразумеваться, как с неподелённой конфигурацией? Или аналогично CH группа, показанная волнисто? Я думаю, что тоже можно.
-
А как будет записываться строение других групп этой волнистой связью? Можно картинку (если есть где взять)? А то мне так понятнее.
-
А эта висюлька может подразумевать только метильную группу неопределённой конфигурации, или же и другие группы могут обозначаться аналогичной висюлькой?
-
То есть, в любом случае висюлька будет означать не определённую в конфигурации метильную группу? А, и зачем это указывать в строении вещества, если это не принципиально важно? Ну, свойства вещества ведь от этого не меняются, разве что разные формы отражают свет по-другому. Зачем же делать путаницу? На схемах, где показывается не общее строение, а именно строение форм, или там где указывают именно это свойство веществ, это нужно показывать. Опять непрофессионалы умничают?
-
Возможно, это какое-то устаревшее понятие, сейчас по-другому называется. В советском учебнике химии за 10 класс такая связь указывалась.
-
И в вики на другой картинке в этой же молекуле на месте этой связи показана CH3-группа.
-
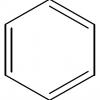
Вот еще вопрос. На рисунке показано строение вещества амф**ам*на. Что означает сия висюлька (волнистая линия) и как её читают в органике (как эта группа называется)?
-
Насчёт пылесоса - у меня тётя как-то раз разбила градусник и тоже ртуть пылесосом собирала. Никто не отравился и пылесос не выбрасывали.
-
Ты про последнюю картинку? Ну это же элементарно, Гугл хром - это браузер.
-
Свойства - то есть реакция смеси с веществом А и квасцов с этим же веществом А. Да? А я всегда считал, что раз у веществ разная формула, то и свойства будут разными. А если не в растворе? То свойства квасцов будут отличаться от свойств смеси сульфата калия и алюминия?
-
У меня такой вопрос. В растворах соли существуют в виде ионов. Например, в растворе хлорида натрия находятся ионы натрия и хлора. В смесях растворов - разные ионы, например, в смеси растворов хлорида натрия и хлорида калия присутствуют ионы натрия, калия и хлора. Ионы в растворах существуют самостоятельно, окружённые "оболочкой" (или как это ещё называется не помню) растворителя, например воды. И вот в чём вопрос: существуют соли, которые диссоциируют на ионы, аналогично смеси других солей. Пример: алюмокалиевые квасцы AlK(SO4)2 и смесь сульфата калия и сульфата алюминия K2SO4 и Al2(SO4)3. В растворах и того, и другого присутствуют ионы калия, алюминия и сульфат-ионы, ну с той разницей что в разных соотношениях. Почему свойства таких растворов различны, хотя ионы одни и те же?
-
Вы вообще к кому обращаетесь? Ко мне? И причём тут алюминий и то, что после него руки чёрные???