
Джастин Бибер
-
Постов
104 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Джастин Бибер
-
-
«г/моль-экв» или «г-экв/моль»?
Как н-н-надо писать?
-
Почему на лабах применяют перманганат калия, а не перманганат натрия, если у последнего р-римость выше?
-
Почему на лабах применяют хлорид бария, а не нитрат, если последний использовать целесообразнее?
-
как из малонового эфира получить α, α' диметилянтарную кислоту?!

-
5,33 г/моль-экв, не? -_-5,33 г-экв./моль
-
Заранее Спасибо!
S + 4ClO2 + 6NaOH → 4NaClO2 + Na2SO3 + 3H2O
KIO3 + 3K2SO3 → KI + 3K2SO4
-
5,33 г/моль-экв, сера.если при сгорании 3,2 г этого элемента образуется 8г оксида
(O_o)
SO3 при сгорании образуется?
-
i-PrCH2CH2CH2Cl —КОН(спирт.)→ i-PrCH2CH=CH2 —НСl→ i-PrCH2CHClCH3—КОН(спирт.), t→ i-PrCH=CHCH3 —КМnO4, H2O, 0°C→ i-PrCH(OH)CH(OH)CH3
i-PrCH2CH=CH2 —ВН3→ i-PrCH2CH2CH2BH2—Н2О2, ОН-→ i-PrCH2CH2CH2OH
-
Фенилацетилен.
PhCH=CH2 ---hν, Cl2, - HCl→ PhCCl=CH2 ---KOH(спирт.), - KCl, - H2O→ PhC≡CH
Радикальное замещение, а не электрофильное присоединение, потому что под действием света происходит гомолиз молекулы хлора*
-
-
Кетонов, не?в) окисление до кислот или альдегидов ( в заависимости от строения)
-
CH3CH2CH(OH)CH2CHOподскажите развернутую формулу 3-оксипентаналь плиз

-
п-CH3C6H4OH + CH3COCl → п-CH3COOC6H4CH3 + HClЯ извиняюсь распишите её пожалуйста поробно
-
Образование сложного эфира.Непоняла хлорангидрида этановой кислоты, это что
p-MeC6H4OH + MeCOCl → p-MeC6H4OCOMe + HCl объясните эту реакцию плиз
СН3COCl - хлорангидрид этановой (уксусной) к-ты, ацетилхлорид.
-
p-MeC6H4OH + NaOH → p-MeC6H4ONa + H2OКакая булет реакция п-крезола и едкого натрия, хлорангидрида этановой кислоты, бромной воды. Помогите пожалуйста
p-MeC6H4OH + MeCOCl → p-MeC6H4OCOMe + HCl
p-MeC6H4OH + 2Br2 → 2HBr +

-
«Игра света». Что преподу сказать, как это явление назвать? Здесь скорее физика, нежели химия. Не дифракция/интерференция, не рефракция, не дисперсия......игра цвета. Конц. р-ры нитрата меди зелёные, при уменьшении концентрации на одну молекулу нитрата меди приходится больше молекул воды, и цвет кажется синим.
-_-Может, изменяется состав комплекса (на одну молекулу нитрата меди приходится больше молекул воды).Вообще нитрат, сульфат и карбонат меди очень странные.
-
-
You don't say!?Концентрированные растворы нитрата меди зеленые, если растворить, то все хорошо - синие
Но почему?
-
-
2Na3PO4 + 3Ca(OH)2 → 6NaOH + Ca3(PO4)2↓Помогите синтезировать фосфор из фосфорной и серу из серной кислот в лаборатории.
2Ca3(PO4)2 + 6SiO2 + 10C ---t→ 6CaSiO3 + P4 + 10CO↑ Фосфор растворяется в сероуглероде, выпарить.
Восстановить конц. серную к-ту металлом средней активности, сера в осадке.
-
KMnO2 + NO2 → KNO2 + MnO2KMnO2+NO2+H2O=
Какие здесь будут продукты реакции?? я так поняла, что KNO2 точно будет, а что еще??
-
Нитрат бария, размер аниона наибольший. Для получения более чистого осадка - уменьшения окклюзии/адсорбции.Какую соль: нитрат бария, хлорид бария, или бромид бария целесообразно использовать при осаждении сульфат-иона?и почему?

-
2NH3 + 2NO2 + H2O → NH4NO3 + NH4NO2Возможна ли реакция между оксидом азота (IV) и аммиаком?
8NH3 + 6NO2 --- t → 7N2 + 12H2O
-
По какому механизму протекает эта реакция?
PhNHNH2 + MeCHO → [PhNHNH2CH(O-)Me] → [PhNHNHCH(OH)Me] → PhNHN=CHMe↓оранж.+ H2O
По нуклеофильному.


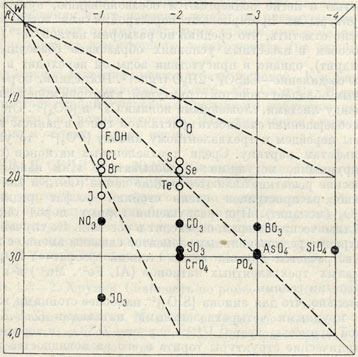
Нитрат же лучше
в Решение заданий
Опубликовано