-
Постов
29 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Chemram_
-
-
-
А можно ли в таком дикетоне, селективно восстановить одну кетогруппу с нормальными выходами?
-
http://chemister.ru/Database/search.php - тут еще можно чего нить нарыть
-
Видел где то, что используют ПМС 10000 и более
-
Миграция двойной связки ближе к кольцу наверное
-
Может вам вообще не сульфат калия продали, а аммония например...
-
Я тоже в свое время ее искал.
и как, успешно?
-
Добавьте оксида вольфрама(VI) и получите сильные борновольфрамовые гетерополикислоты.
Что ни будь органическое бы. На подобии углеводов или ТЭА.
-
-
Здравствуйте! Я впервые на этом форуме и если я что-то не туда написала/не так оформила, прошу палками не бить

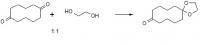
Я тут второй день думаю над этой задачей, но не уверена над своим ответом. Услышала, что тут могут люди помочь, подсказать какой правильный будет продукт G и почему
 (исходя из того что реакция ещё F там + Е. Очень сильно надеюсь на помощьььь и заранее спасибо!
(исходя из того что реакция ещё F там + Е. Очень сильно надеюсь на помощьььь и заранее спасибо! 
Думаю как то так будет..
-
Для борьбы с формальдегидом в воздухе, так же можно попробовать озонатор. Фенол тоже должен окислиться. и вся остальная органика. Только нужно помнить, что озон тоже не витамин и лучше обрабатывать помещение, когда ни кого нет, а потом проветрить.
-
i ! vchyom raznicca i chto oni saboy predstavlayut? Скорее всего полимер содержащий гидроксильные группы - hydroxy-containing polyme и полимер не содержащий гидроксогруппы - Hydroxy- terminted polymer
-
Какие есть у борной кислоты водорастворимые комплексы на подобии БК с глицерином, но более прочные?
-
Прикреплю статейку про комплексы меди c НТФ -- щелочной разлагается уже при 60оС с выделением оксида меди(II), может, и пойдёт.
Чтобы не плодить темы, спрошу здесь -- можно ли получить растворимый комплекс меди(I) с ацетонитрилом и его раствор в ацетонитриле или в воде или в их смеси?
Благодарствую.
В общем будем все смотреть на практике.
-
Не знаю. Даже предположить не могу. Может пиридин? ИМХО - тут метод научного тыка рулит

Да...надо пробовать.
Пиридин уж больно пахуч...)))
-
Если нужно, шоб разлагался при нагревании - тут надо подбирать амин. Этилендиамин стабилизирует медь(II), а, скажем, ацетонитрил - наоборот, медь(I). Значит должно быть шо-то среднее, слегка стабилизирующее, не так сильно, как ЭДА.
Триэтаноламин по сравнению с этилендиамином наверно сильнее будет образовывать комплекс?
-
А с какими конкретно солями меди идет эта реакция?
Вроде как в кислых растворах одновалентная медь окисляется. Исходя из этого,можно попробывать,использовать или летучую кислоту,улетающую при повышении температуры,или наоборот кислоту,с растворимостью сильно зависимой от температуры
Стандартно обычно используют сульфат меди. В этом варианте реакция проходит сразу.
Хотелось сделать систему, где раствор сульфата меди (2+) находится в смеси с NaI или KI, но что бы при при обычной температуре (20-30*С) реакция практически не шла.
А начиналась бы около 60*С.
НА ум приходит только комплексование меди(2+).
Этилендиамин стабилизирует медь(II). Комплексный иодид меди [Cu(en)2]I2 - вполне себе существует. Не знаю, как в твердом виде, а в растворе (даже кипящем) вполне устойчив.
Интересно, спасибо.
-
Возможно ли замедлить реакцию : 2Cu2+ + 4I- = 2CuI + I2 ?
ЧТо бы реакция при комнатной температуре была сведена к минимуму, и шла только при более высокой температуре (5-600С)
Будет ли медь в комплексном виде замедлять реакцию?
-
Получается, что образуется гексацианоферрат(II) железа(III)?
-
Кто знает, как идет реакция между гексацианоферратом(II) калия и тиосульфатом натрия.
K4[Fe(CN)6] + Na2S2O3 = ???
раствор из желтого переходит в прозрачный
-
У кого есть книжка в электронном виде?
Название: Успехи химии органических перекисных соединений и аутокисления
Автор: Эмануэль Н.М.
Год издания:1988
УДК: 547
Страниц: 496 -
Я вот тоже недавно пилил-пилил клапаны и ничего не напилил.Кстати от ЗИЛ-а были.
Наверно впускные клапана пилили
-
 2
2
-
-
А можно как-то защитить альфа-углерод от альдольной конденсации или наоборот или наоборот сделать так, что реакция Канниццаро сводилась бы к минимуму?
Если альфа-углерод не защищен, то Канниццаро будет идти незначительно, если конечно не будет каких либо других факторов, типа стерических препятствий и т.д.
Лучше смотреть каждый случай конкретно
-
Спасибо, а то пишут всякую ересь.
на самом деле, если есть водород у альфа атома, то будет идти и альдольная конденсация и реакция Канниццаро, просто последняя в меньшей степени.



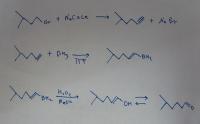
Этилбензол из ацетофенона.
в Органическая химия
Опубликовано
Спасибо!