-
Постов
17 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные GUY
-
-
Атомарный водород, по сравнению с молекулярным намного активнее, об этом можно судить даже по тому, какую температуру пламени выдает горелка на атомарном(около 3000C) и молекулярном водороде(еле-еле 2500)
-
Может я ошибаюсь, но тут таких нет
-
Если бы были более экономичные способы их бы сразу начали использовать, но увы.
-
Прочитай внимательно учебник по химии, там наверняка все разъяснено. Там же поищи примеры, которые уже разобраны, реши сначала сам, а потом проверь.
-
А что именно нужно, напиши по пунктамСпасибо. Почитал, но не то. А форумом то нет смысла пользоваться, а экзамене же не будет такой возможности. Так что выучить надо.
1
Определите координаты атома в таблице элементов.
Период 5-й, группа VIIA
2
Составьте валентную электронную формулу.
5s25p5
3
Допишите символы внутренних электронов в последовательности заполнения ими подуровней.
1s22s22p63s23p64s23d104p65s24d105p5
4
Учитывая уменьшение энергии полностью заполненных d- и f-подуровней, запишите полную электронную формулу.

5
Отметьте валентные электроны.
1s22s22p63s23p63d104s24p64d105s25p5
6
Выделите электронную конфигурацию предшествующего атома благородного газа.

7
Запишите сокращенную электронную формулу, объединив в квадратных скобках все невалентные электроны.
[Kr, 4d10]5s25p5
Вот вроде все по пунктам
-
http://www.xumuk.ru/esa/ Можешь воспользоваться этим сервисом, а вообще почитай здесь http://www.sxemotehnika.ru/elektronnoe-stroenie-atoma.html
-
-
В промышленности распространён пиролиз бензина в трубчатых печах: смесь бензина с водяным паром нагревают до 840-850°С, а затем быстро охлаждают в "закалочном" аппарате для предотвращения пиролитического уплотнения непредельных углеводородов. Парогазовую смесь отделяют от тяжёлой смолы,воды, разделяют газ и лёгкое масло пиролиза. После перегонки жидких продуктов на установке пиролиза получают 4 фракции с температурами кипения: до 70°С, 70-130°С (бензольно-толуольная), 130-190°С (С8-С9) и выше 190°С (тяжёлая смола).Подскажите как в малопромышленных масштабах получить бентол (бензольно-толуольную фракцию)
Можете посмотреть здесь http://www.ngpedia.ru/id255943p1.html
-
1. BaCl2 + 2H20= h2 +Cl2 + Ba(oh)2 (на аноде - хлор)
По этому уравнению легко все посчитать, кстати есть еще такой закон Фарадея m= kJt (k- электрохим. коэффициент).
2.4AgNO3 + 2H2O = 4Ag + О2 + 4HNO3
3. 4Au(NO3)3 + 6H2O = 4Au + 3O2 + 12HNO3
2Hg(NO3)2 + 2H2O = 2Hg + O2 + 4HNO3
-
1.CHCCH2CН3 + Br2 = CHBrCBrCH2СH3
2.CHCCH2CН3 + HCL = CH2CCLCH2CH3
3.CHCCH2CН3 + H2 = CH2CHCH2CH3
4.CHCCH2CН3 +[ Ag(NH3)2]OH = AgCCCH2CH3 + 2NH3 + h20
-
Могу сказать одно с документацией у этой компании все нормально, а что касается угля, то ничего сказать не могу,увы.Уважаемые специалисты!
Прошу Вас рассмотреть возможности определения физико-химических свойств активированного угля производства группы компаний "Норит".
Паспорт безопасности на активированный уголь - http://yadi.sk/d/RGvUWHLv7oD5J
Нашими технологами данный уголь предусматривается в технологических процессах обогащения руды.
Удельную теплоту сгорания технологи принимали как для углевородородного топливного угля 33МДж/кг (категория В1-В2).
В производстве помещения десорбции и реактивации угля это помещения свыше 1000 м.кв. Значение категории данного помещения является отпределяющим.
Однако по своей стуктуре этот активированный уголь схож с графитом (это 363кДж/кг - В4), это вещество с "углеродным скелетом".
Представительство Норит пообещало произвести испытание данного угля с целью определения удельной теплоты сгорания, но мне почему-то верится с трудом.
Удельную теплоту сгорания я бы мог обосновать зная химический состав данного угля, но этого у меня нет.
Помогите пожалуйста кто чем может!
-
Самое интересное, что пока еще не могут сделать, это термоядерные реакции, вот это был бы шик :ce:
-
http://forum.xumuk.r...howtopic=162058 посмотрите здесьВ токсилогическом анализе в случае отравления алкалоидами опия используют раздельное извлечение из анализируемого материала морфина и кодеина. Предложите химическую реакцию, с помощью которой можно отделить морфин от кодеина, и напишите схему этой реакции.
-
Юрий, очень сложно опровергать или подтверждать какой-либо диагноз, не обязательно ваш, имея только скудное его описание. Я не врач, но железодефицитная анемия происходит при нарушении синтеза гемоглобина, вследствие недостатка железа в организме. Если вам нужна более квалифицированная помощь, чем у вас сейчас, то можете обратиться в другое мед. учреждение, где вам окажут более качественную помощь. Я, конечно могу что-то вам посоветовать, если вы предоставите более подробное описание симптомов.Добрый день!
Есть основания полагать что у меня проблема с железом, на данном этапе латентный дефицит переходит в анемию. Помоему правильно это называется железоперераспределительная анемия - когда феритин в норме, а падает железо, на том же уровне ЖСС, в последнее время пополз вниз гемоглобин, другие показатели по крови.
Такое впечатление, что мой лечащий доктор в этом (железодефицитах) слабо ориентируется, поэтому очень хотелось бы общатся с кем то кто в теме.
Интересует 1.подтверждение/опровержение диагноза.
2. Пути выхода, какие лекарства существуют на отечественном/зарубежных рынках.
С уважением, Юрий.
P.S. Если немного не так выразился, сильно не пинайте, но я думаю смысел понятен.
-
Сульфид натрия имеет белый цвет, ну слегка бежевого, но никак не зеленые. Сейчас может поищу что- нибуть по вашей темеДобрый день!
Купил некоторое время назад сульфид натрия в химмаге с целью получения сероводорода.
Проблема в том что при добавлении кислоты (соляной или фосфорной) к данному реактиву выделяется газ по запаху напоминающий SO2.
Ни один опыт где нужен был сероводород не увенчался успехом.
Растворы этой соли - зеленые, сам реактив тоже зеленоватый.
Собственно вопрос - что это за реактив? Может и не сульфид вовсе?
-
Продукты существуют, сейчас очень часто в различные напитки добавляют, например, хинин, POPOP, флуоресцеин, эозинПрошу подсказать: существуют ли пищевые продукты, имеющие флуоресценцию? Как, например, производные хинина - напиток тоник светится в ультрафиолете.


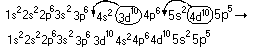
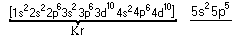
Кинетика
в Решение заданий
Опубликовано
Прошу помочь с задачкой.
Найти константу равновесия разложения 2HBr=H2 + Br2 , если Т=1400К, исходная концентрация HBr=0,0145атм, равновесная концентрация HBr=0,0136 атм.