Sany'OK
Пользователи-
Постов
94 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Sany'OK
-
Карбонат аммония при комнатной температуре устойчив (tразл.=60 °C). Кстати в дымовой состав (не на хлорате) можно попробовать ввести этот карбонат аммония (я думаю можно ещё и с сульфатом) и ПВХ (только нужно, чтоб КБ был отрицательным, чтоб не окислился аммиак в карбонате).
-
Ну, ещё так: CaCl2 + (NH4)2CO3 = CaCO3↓ + 2NH4Cl
-
Есть ещё мысля: в р-р образовавшегося H2[PbCl4] прилить р-р аммиака, получится (NH4)2[PbCl4], затем ещё раз прилить р-ра серной кислоты по уравнению: (NH4)2[PbCl4] + H2SO4 = PbSO4↓ + 2NH4Cl + 2HCl и ещё раз прибавить р-р аммиака. Но так, я думаю лучше не заморачиватся.
-
А если взять р-р серной кислоты, например електролита (или его разбавить), то тогда получится?
-
Я так понял аппарат для возгонки хлорида аммония? По этой р-ции удастся получить скорее всего не весь возможный хлорид аммония и нитрат калия, т. к. обе соли очень хорошо растворимы в воде (равновесие). Также следует учесть, что при возгонке нашатыря (tвозг.=337,6 оС) начнёт разлагатся нитрат калия (tразл.= больше 334,5 оС). По моему способу хоть и надо побольше реактивов (их легко достать или сделать самому), но зато не нужно строить всякие аппараты (хоть они и не сложные в конструкции) и выход будет лучше.
-
Можно ещё так попробовать: Pb(NO3)2 + 2NaCl = PbCl2↓ + 2NaNO3 или Pb(CH3COO)2 + 2NaCl = PbCl2↓ + 2CH3COONa PbCl2 + H2SO4 = PbSO4↓ + 2HCl
-
На аноде будет образовыватся надсерная кислота (кислота Каро). При концентрациях серной кислоты с плотностями меньше 1.2 или с концентрироваными её растворами выход надсерной кислоты будет мал (при плотности кислоты больше 1.4 выход также падает).
-
"Де-Нол" - это висмута трикалия дицитрат. Вот тут написано о нём. Также этот препарат может иметь названия "Биснол", "Тримо", "Пилоцид", "Вентрисол", "Трибимол", "Де-Нол гранулят".
-
Извеняюсь, перепутал с йодацетоном. Но продукт всеравно не очень хорошо пахнет. В руках не только держал, но и получал.
-
Смешиваете йод, р-р щелоч и этиловый спирт (или ацетон), йодоформ, как малорастворимое в холодной воде вещество выпадет в осадок. Для большего выхода р-р лучше охладить. ОСТОРОЖНО ЙОДОФОРМ ЯВЛЯЕТСЯ ЛАКРИМАТОРОМ (слезоточивым веществом)!
-
Так и называются "Адонис-бром". Вот ссылка.
-
Я думаю, что не бабахнет, да и массовая доля сурьмы и олова не очень большая. Но лучше для начала провести тест с небольшим количеством веществ. Также необходима будет перекристаллизация нитрата, возможна дополнительная очистка от вякой бяки.
-
Эта р-ция идёт в присутствии концентрированой серной кислоты. Цитата получения муравьиной кислоты с щавелевой (Л. А. Цветков "Эксперемент по органической химии в средней школе"):
-
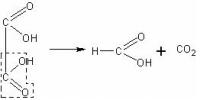
Ещё вода и угарный газ. H2C2O4 = H2O + CO2 + CO
-
Мой свинцовый сурик также ярко-оранжевого цвета и на сколько мне известно у него один состав 2PbO*PbO2. Для этой р-ции можно использовать любой оксид свинца, только селитры нужно брать в избытке от теоретического.
-
Согласен, получать таким образом йод дорого, но всё же можно.
-
Пакет гипотермический "СНЕЖОК" применяют для холодного компресса при первой помощи: при ушибах и растяжениях мышц (прикладывают на место травмы), перегревах, укусах насекомых, для остановки кровотечения. Вот цитата (с pirotek.info) получения бромида калия с таблеток: Лучше конечно ещё перекристаллизовать полученную соль. Щавелевая кислота скорее всего в чистом виде (сравнительно). Фото упаковки:
-
Прочитал я про цельозы, полились от смеха слёзы.
-
В аптеке можно ещё купить сорбит, фруктозу, аскорбиновую кислоту, глицин (таблетки сублингвальные, имеющие следующий состав: глицин — 0,1 г, вспомогательные вещества: магния стеарат, метилцеллюлоза водорастворимая) гидроперит, формидрон, аглитропин (состав: кислота уксусная, уротропин, глицерин, вода очищенная), димексид (ДМСО), вроде бы салициловую кислоту (или ацетилсалициловую, с которой можно получит салициловую), активированный уголь, снежок (аммиачная селитра), парацетамол (с него можно получить хлоранил, если кому надо), йодомарин (можно получить йод), хлористый калий (заменитель пищевой соли), борная кислота, адонис-бром (одна таблетка содержит 0,345 г массы "адонис-бром", содержащей 72,5% калия бромида, экстракта адониса сухого активностью 36,5 ЛЕД в 1 г). В ветеринарной аптеке - серу (кормовая добавка, применяется для улучшения шерстяного и перьяного покрова у домашних животных и птици), щавелевую кислоту (против варроатоза пчёл), раствор хлористого кальция (небольшой концентрации). Карбонат аммония можно купить в продуктовом магазине под названием аммоник (применяется как разрыхлитель теста).
-
В этом синтезе главное не перегреть смесь, а то нитрат начнёт разлогатся. Температуры должно хватить на плавление аммиачной селитры (tпл=169.6 оС), но она не должна превышать 200 оС. При нагревании часть селитры разложится, по этому её и взяли с избытком. Когда смесь побелеет (конец реакции), она не будет такой жидкой, как в начале, а станет на вид совершенно "сухой".
-
PbO (желтого цвета, свинцовый глет) растворяется в азотной кислоте, при этом получается нитрат свинца и вода, а вот PbO2 не растворяется в азотной кислоте, но у него коричневый цвет. Я думаю, что у Вас выпал сульфат свинца. Возьмите чистый свинец, тогда всё нормально получится. Вместо азотной к-ты можно взять нитрат аммония, для этого нужно в его расплав добавить свинец и греть смесь до растворения свинца (осторожно выделяется аммиак). Получит нитрат свинца можно путём сплавления свинцового сурика и нитрата аммония, при этом также выделяется аммиак. Вот цитата получения этого нитрата через сурик и аммиачную селитру (сайт не помню, вроде бы по пиротехнике был): Фото кристалликов нитрата свинца, сделанного по этому способу:
-
Вот комплексное соединение, которое образуется при взаимодействии FeCl3 с фенолом.
-
1. Одна σ-связь. π-связи не имеется, потому что в молекуле нет кратных связей. 2. Если форма молекулы симметрична, то молекула неполярна, а если асимметрична, молекула полярна. В даном случае форма молекулы асимметрична, тоесть молекула полярна. Полярность несимметричной по форме молекулы вытекает из полярности ковалентных связей между атомами элементов с разной электроотрицательностью.
-
Полученый таким образом фенол не будет загрязнён салициловой кислотой?