-
Постов
18 -
Зарегистрирован
-
Посещение
Информация о dr_alex
- День рождения 03/16/1977
Старые поля
-
Пол
Мужчина
-
Город
Минск
Достижения dr_alex
-
РАСТВОР СЛАБОГО ОСНОВАНИЯ Пусть В - слабое однокислотное основание, тогда в растворе существует следующее равновесие (автопротолиз воды мы пока учитывать не будем): B + H2O ↔ BH+ + OH- Kb = [bH+][OH-] / - константа основности Так как шкалу кислотности принято выражать в единицах pH, а в выражение константы основности равновесная концентрация протонов не входит в явном виде, то удобнее будет воспользоваться выражением константы кислотности сопряженной кислоты (KBH+ или Ka). BH+ + H2O ↔ B + H3O+ KBH+ = [H3O+] / [bH+] - константа кислотности сопряженной кислоты Так как в системе единственным источником OH- и ионов BH+ является молекула B, то уравнение электронейтральности принимает вид: [bH+] = [OH-] Запишем уравнение материального баланса СB = + [bH+] Из уравнения материального баланса видно, что равновесная концентрация молекулярной формы слабого основания равна разности между общей концентрацией растворенного основания CB и концентрацией катионной формы. Таким образом, = CB - [bH+] = CB - [OH-] = CB - Kw / [H3O+] Подставив эти выражения в уравнение константы кислотности сопряженной кислоты KBH+ = (CB - Kw / [H3O+])[H3O+] / (Kw / [H3O+]) и проведя соответствующее преобразование, получаем квадратное уравнение: CB[H3O+]2 - Kw[H3O+] - KwKBH+ = 0 Такой ход вычислений применим к любым растворам слабых однокислотных оснований, за исключением очень разбавленных растворов с концентрацией растворенного вещества ниже 10-6 моль/л. Однако во многих случаях эту формулу можно упростить. Если степень протолиза (α = [OH-] / CB = Kw / ([H3O+]CB)) основания меньше 5% *, можно считать, что ~ CB. А так как в данной системе единственным источником ионов OH- и BH+ является слабое основание B, то [OH-] = [bH+]. С учетом всех этих допущений KBH+ = [H3O+] / [bH+] = CB[H3O+]2 / Kw Решение этого уравнения относительно ионов H3O+ приводит к значению [H3O+] = (KwKBH+ / CB)1/2 или в логарифмической форме pH = 1/2 (pKw + pKBH+ + lgCB) * Как и в случае кислот, здесь также можно вывести приближенный критерий применимости упрощенной формулы. Если в уравнение Kb = [OH-]2 / CB подставить [OH-] ≤ 0,05 CB и помня, что Kw = KbKBH+, то получим (CBKBH+ / Kw) ≥ 400. В процессе вывода формул нами не были учтены ионы OH-, которые образуются в результате реакции автопротолиза воды. И в большинстве случаев это оправдано. Однако так можно поступать не всегда, особенно когда речь идет о растворах очень слабых оснований, даже если их общая концентрация выше 10-6 моль/л. Пусть B - очень слабое однокислотное основание, тогда в растворе существуют следующие равновесия: B + H2O ↔ BH+ + OH- 2H2O ↔ H3O+ + OH- Запишем уравнения электронейтральности и материального баланса для данной равновесной системы [OH-] = [bH+] + [H3O+] СB = + [bH+], так как основание очень слабое, то >> [bH+] и, следовательно, можно считать, что CB ~ Подставим величину [bH+] из выражения константы кислотности сопряженной кислоты в уравнение электронейтральности Kw / [H3O+] = CB[H3O+] / KBH+ + [H3O+] и выполнив несложные преобразования, получаем: [H3O+] = (KwKBH+ / (CB + KBH+))1/2 ОБЩИЙ СЛУЧАЙ ВЫЧИСЛЕНИЯ pH РАСТВОРА СЛАБОГО ОСНОВАНИЯ Запишем протолитические реакции, протекающие в растворе, а также выражения соответствующих констант: B + H2O ↔ BH+ + OH- KBH+ = [H3O+] / [bH+] (для расчетов будем использовать выражение константы кислотности сопряженной кислоты, а не константы основности по причине, указанной ранее) 2H2O ↔ H3O+ + OH- Kw = [H3O+][OH-] Составим уравнения электронейтральности и материального баланса: [OH-] = [bH+] + [H3O+] CB = + [bH+] Из этих данных выразим равновесные концентрации всех форм существования слабого основания в растворе: [bH+] = [OH-] - [H3O+] = CB - [bH+] = CB - [OH-] + [H3O+] Подставляем полученные значения и [bH+] в выражение константы кислотности сопряженной кислоты KBH+ = (CB - [OH-] + [H3O+])[H3O+] / ([OH-] - [H3O+]) После преобразования получаем кубическое уравнение: [H3O+]3 + (CB + KBH+)[H3O+]2 - Kw[H3O+] - KwKBH+ = 0 Как и в случае кислот, данное уравнение целесообразно использовать только когда речь идет об очень разбавленных растворах слабых оснований. Во всех остальных случаях допустим ряд упрощений, которые позволяют свести задачу к решению уравнения второй степени относительно [H3O+]. Рассчитать рН 0,10 М раствора ацетата натрия, константа кислотности уксусной кислоты составляет 1,75*10-5. Так как CBKa / Kw составляет 1,75*108, то можно применять упрощенную формулу. Таким образом, pH = 1/2 (14,0 + 4,76 + lg0,10 ) = 8,88 Рассчитать рН 2,0*10-4 М раствора пиперидина, если рKBH+ катиона пиперидиния составляет 11,12. Отношение CBKa / Kw составляет 0,15. Поэтому применять для расчета рH упрощенную формулу нельзя. CB[H3O+]2 - Kw[H3O+] - KwKBH+ = 0 2,0*10-4[H3O+]2 - 1,0*10-14[H3O+] - 7,6*10-26 = 0 [H3O+] = 5,67*10-11 моль/л; pH = 10,2 Рассчитать рН 0,10 М раствора иодата натрия, если Ka иодноватой кислоты составляет 0,17. Иодат натрия - очень слабое основание. Для расчета рН воспользуемся формулой: [H3O+] = (KwKBH+ / (CB + KBH+))1/2 [H3O+] = (1,0*10-14 * 0,17 / (0,10 + 0,17))1/2 [H3O+] = 7,93*10-8 моль/л; pH = 7,10 Если не учитывать автопротолиз воды, то рН раствора составит 6,88, а это неверно, так как в растворе присутствует основание, а среда получается кислой.
-
РАСТВОР СЛАБОЙ КИСЛОТЫ Пусть HA - слабая одноосновная кислота, тогда в растворе существует следующее равновесие (автопротолиз воды мы пока учитывать не будем): HA + H2O ↔ H3O+ + A- Ka = [H3O+][A-] / [HA] - константа кислотности Так как в данной системе единственным источником H3O+ и ионов A- является молекула HA, то уравнение электронейтральности принимает вид: [H3O+] = [A-] Запишем уравнение материального баланса СHA = [HA] + [A-] Из уравнения материального баланса видно, что равновесная концентрация молекулярной формы слабой кислоты равна разности между общей концентрацией растворенной кислоты CHA и концентрацией анионной формы. Таким образом, [HA] = CHA - [A-] = CHA - [H3O+] Подставив эти выражения в уравнение для константы кислотности Ka = [H3O+][A-] / [HA] = [H3O+]2 / (CHA - [H3O+]) и проведя соответствующее преобразование, получаем квадратное уравнение: [H3O+]2 + Ka[H3O+] - KaCHA = 0 Такой ход вычислений применим к любым растворам слабых кислот, за исключением очень разбавленных растворов с концентрацией растворенного вещества ниже 10-6 моль/л. Однако во многих случаях эту формулу можно упростить. Если степень протолиза (α = [H3O+] / CHA) кислоты меньше 5% *, можно считать, что [HA] ~ CHA. А так как в данной системе единственным источником ионов H3O+ и A- является слабая кислота HA, то [H3O+] = [A-]. С учетом всех этих допущений Ka = [H3O+][A-] / [HA] = [H3O+]2 / CHA Решение этого уравнения относительно ионов H3O+ приводит к значению [H3O+] = (KaCHA)1/2 или в логарифмической форме pH = 1/2 (pKa - lgCHA) * На основании этого утверждения можно вывести еще один приближенный критерий применимости упрощенной формулы. А именно если в уравнение Ka = [H3O+]2 / CHA подставить [H3O+] ≤ 0,05 CHA, то получим (CHA / Ka) ≥ 400. Следовательно, когда общая концентрация слабой кислоты по меньшей мере в 400 раз больше константы кислотности, можно пользоваться упрощенными формулами для расчета [H3O+] или рН. В процессе вывода формул нами не были учтены ионы H3O+, которые образуются в результате реакции автопротолиза воды. И в большинстве случаев это оправдано. Однако так можно поступать не всегда, особенно когда речь идет о растворах очень слабых кислот, даже если их общая концентрация выше 10-6 моль/л. Пусть HA - очень слабая одноосновная кислота, тогда в растворе существуют следующие равновесия: HA + H2O ↔ H3O+ + A- 2H2O ↔ H3O+ + OH- Запишем уравнения электронейтральности и материального баланса для данной равновесной системы [H3O+] = [A-] + [OH-] СHA = [HA] + [A-], так как кислота очень слабая, то [HA] >> [A-] и, следовательно, можно считать, что CHA ~ [HA] Подставим величину [A-] из выражения константы кислотности в уравнение электронейтральности [H3O+] = KaCHA / [H3O+] + Kw / [H3O+] и выполнив несложные преобразования, получаем [H3O+] = (KaCHA + Kw)1/2 ОБЩИЙ СЛУЧАЙ ВЫЧИСЛЕНИЯ pH РАСТВОРА СЛАБОЙ КИСЛОТЫ Запишем протолитические реакции, протекающие в растворе, а также выражения соответствующих констант: HA + H2O ↔ H3O+ + A- Ka = [H3O+][A-] / [HA] 2H2O ↔ H3O+ + OH- Kw = [H3O+][OH-] Составим уравнения электронейтральности и материального баланса: [H3O+] = [A-] + [OH-] CHA = [HA] + [A-] Из этих данных выразим равновесные концентрации всех форм существования слабой кислоты в растворе: [HA] = CHA - [H3O+] + [OH-] [A-] = [H3O+] - [OH-] Подставляем полученные значения [HA] и [A-] в выражение константы кислотности Ka = ([H3O+]2 - Kw) / (CHA - [H3O+] + Kw / [H3O+]) После преобразования получаем кубическое уравнение: [H3O+]3 + Ka[H3O+]2 - (Kw + KaCHA)[H3O+] - KaKw = 0 Данное уравнение целесообразно использовать только в том случае, когда константа кислотности близка к 10-7 и когда речь идет об очень разбавленных растворах. Во всех остальных случаях допустим ряд упрощений, которые позволяют свести задачу к решению уравнения второй степени относительно [H3O+]. Рассчитать рН 0,10 М раствора уксусной кислоты, константа кислотности которой составляет 1,75*10-5. Так как CHA / Ka составляет около 6*103, то можно применять упрощенную формулу. Таким образом, pH = 1/2 (4,76 - lg0,10 ) = 2,88 Рассчитать рН 0,10 М раствора дихлоруксусной кислоты, если константа кислотности равна 8,0*10-2. Так как CHA / Ka составляет всего 1,3, то для нахождения [H3O+] необходимо использовать квадратное уравнение: [H3O+]2 + Ka[H3O+] - KaCHA = 0 [H3O+]2 + 8,0*10-2[H3O+] - 8,0*10-3 = 0 [H3O+] = 5,8*10-2 моль/л; pH = 1,24 Рассчитать рН 1,0*10-4 М раствора фенола, если константа кислотности равна 1,0*10-10. Фенол - очень слабая кислота. Поэтому для расчета pH воспользуемся формулой [H3O+] = (KaCHA + Kw)1/2 [H3O+] = (1,0*10-10 * 1,0*10-4 + 1,0*10-14)1/2 [H3O+] = 1,4*10-7; pH = 6,85 Если не учитывать автопротолиз воды, то рН раствора составит 7,0, а это неверно!
-
РАСТВОР СИЛЬНОЙ КИСЛОТЫ Пусть HA - сильная одноосновная кислота, тогда в растворе существуют следующие равновесия: HA + H2O → H3O+ + A- 2H2O ↔ H3O+ + OH- Запишем уравнение электронейтральности для данной равновесной системы [H3O+] = [A-] + [OH-] Если молярная концентрация сильной одноосновной кислоты больше ~10-6 моль/л, то вкладом ионов H3O+, образующихся при автопротолизе воды, можно пренебречь. Так как концентрация последних равна концентрации OH--ионов, то уравнение электронейтральности принимает вид: [H3O+] = [A-] Запишем уравнение материального баланса CHA = [A-] + [HA] Так как одноосновная кислота HA является сильной, то равновесная концентрация [HA] ~ 0. Таким образом, уравнение материального баланса принимает вид: CHA = [A-] и,следовательно, [H3O+] = CHA; pH = -lgCHA Если молярная концентрация сильной одноосновной кислоты меньше ~10-6 моль/л, то вкладом ионов H3O+, образующихся при автопротолизе воды, пренебречь нельзя. Так как CHA = [A-] и [OH-] = Kw / [H3O+], то уравнение электронейтральности принимает вид: [H3O+] = CHA + Kw / [H3O+], отсюда [H3O+]2 - CHA[H3O+] - Kw = 0 Вычислить рН 5,0*10-2 М раствора HCl. pH = -lgCHCl pH = -lg(5,0*10-2) = 1,30 Вычислить, какое значение pH должен иметь 1,5*10-7 М раствор HClO4. [H3O+]2 - CH+[H3O+] - Kw = 0 [H3O+]2 - 1,5*10-7[H3O+] - 1,0*10-14 = 0 [H3O+] = 2,0*10-7 моль/л, что соответствует pH = 6,70 РАСТВОР СИЛЬНОГО ОСНОВАНИЯ Пусть B - сильное однокислотное основание, тогда в растворе существуют следующие равновесия: B + H2O → OH- + BH+ 2H2O ↔ H3O+ + OH- Запишем уравнение электронейтральности для данной равновесной системы [OH-] = [bH+] + [H3O+] Если молярная концентрация сильного однокислотного основания больше ~10-6 моль/л, то вкладом OH--ионов, образующихся при автопротолизе воды, можно пренебречь. Так как концентрация последних равна концентрации ионов H3O+, то уравнение электронейтральности принимает вид: [OH-] = [bH+] Запишем уравнение материального баланса CB = [bH+] + Так как однокислотное основание B является сильным, то равновесная концентрация ~ 0. Таким образом, уравнение материального баланса принимает вид: CB = [bH+] и,следовательно, [OH-] = CB Так как шкалу кислотности принято выражать в единицах pH, а [OH-] = Kw / [H3O+], то [H3O+] = Kw / CB; pH = pKw + lgCB Если молярная концентрация сильного однокислотного основания меньше ~10-6 моль/л, то вкладом OH--ионов, образующихся при автопротолизе воды, пренебречь нельзя. Так как CB = [bH+] и [OH-] = Kw / [H3O+], то уравнение электронейтральности принимает вид: Kw / [H3O+] = CB + [H3O+], отсюда [H3O+]2 + CB[H3O+] - Kw = 0 Вычислить pH раствора Ba(OH)2 с концентрацией растворенного вещества 2,0*10-4 моль/л. pH = pKw + lgCOH- COH- = 2 * 2,0*10-4 = 4,0*10-4 моль/л pH = 14,0 + lg(4,0*10-4) = 10,60 Вычислить, какое значение pH имел бы 2,0*10-7 М раствор Ba(OH)2. [H3O+]2 + COH-[H3O+] - Kw = 0 COH- = 2 * 2,0*10-7 = 4,0*10-7 моль/л [H3O+] = 2,4*10-8 моль/л, что соответствует pH = 7,62
- 2 ответа
-
- 1
-

-
Все это очень хорошо, но запись таким образом приведет к тому, что выражение получится слишком громоздким (если честно, не очень красиво это смотрится). Насчет стрелочек, последняя стрелочка обозначает наличие резонансных структур т.е. либо существует одна резонансная структура либо другая, вместе они существовать не могут. "Равновесная" стрелочка, которой я кстати так и не нашел, напротив предполагает, что в растворе могут находиться вместе несколько форм. Поправьте меня, если я что не так сказал.
-
Эх, вот это я уже давно понял. Хотя очень жаль. С LaTeX'ом немного знаком, так что можно было бы очень красиво, а главное профессионально все оформлять. А может все-таки можно приделать такой скрипт, который бы распознавал LaTeX'овский код, а?
-
Всем доброго времени суток! Скажите пожалуйста, а возможно сделать так, чтобы дроби записывались с использованием горизонтальной черты? Чесно слово, ну не очень удобно/красиво писать дроби в линейку. Заранее благодарен за ответ! Да, совсем забыл, было бы неплохо еще сделать стрелочки, обозначающие равновесие.
-
Тоже мне, бином Ньютона! COH- = (28,00 / 56,11 + 40,20 / 40,00) / 1,500 = 1,003 моль/л
-
Сразу же возникают несколько вопросов: 1. а каков предел обнаружения холина хлорида при помощи данной реакции? 2. а сколько этого вещества должно предположительно содержаться в этих отрубях? Хватает ли чувствительности? Попробуйте добавить известное количество холина хлорида в эти отруби (например, чтобы концентрация была как в средней точке ГГ), проделайте все операции, описанные в методике и посмотрите будет ли наблюдаться какой-либо аналитический сигнал. Если будет, то возможно просто не хватает чувствительности (очень мало холина хлорида содержится в отрубях).
-
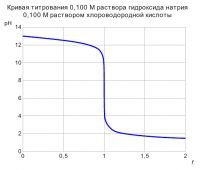
КРИВАЯ ТИТРОВАНИЯ СИЛЬНОГО ОСНОВАНИЯ СИЛЬНОЙ КИСЛОТОЙ f = CHClVHCl / (C0NaOHV0NaOH) где f - степень оттитрованности; CHCl - концентрация титранта, моль/л; VHCl - объем добавленного титранта, мл; C0NaOH - исходная концентрация гидроксида натрия в растворе, моль/л; V0NaOH - исходный объем раствора гидроксида натрия, мл. 1. f = 0 (Раствор сильного основания) pH = pKw + lgC0NaOH f = 0,000; pH = 13,00 2. 0 < f < 1 (Раствор сильного основания) [H3O+] = Kw(V0NaOH + VHCl) / ((1 - f)C0NaOHV0NaOH) f = 0,010; pH = 12,99 f = 0,050; pH = 12,96 f = 0,100; pH = 12,91 f = 0,200; pH = 12,82 f = 0,300; pH = 12,73 f = 0,400; pH = 12,63 f = 0,500; pH = 12,52 f = 0,600; pH = 12,40 f = 0,700; pH = 12,25 f = 0,800; pH = 12,04 f = 0,900; pH = 11,72 f = 0,950; pH = 11,41 f = 0,990; pH = 10,70 f = 0,999; pH = 9,70 3. f = 1 (Нейтральный раствор) [H3O+] = [OH-]; pH = pKw / 2 f = 1,000; pH = 7,00 4. f > 1 (Избыток сильной кислоты) [H3O+] = (f - 1)C0NaOHV0NaOH / (V0NaOH + VHCl) f = 1,001; pH = 4,30 f = 1,010; pH = 3,30 f = 1,100; pH = 2,32 f = 1,200; pH = 2,04 f = 1,500; pH = 1,70 f = 1,800; pH = 1,54 f = 2,000; pH = 1,48 Выводы: Для данных условий титрования подойдут все индикаторы, диапазон перехода окраски которых лежит в области рН от 4 до 10. К таким индикаторам могут быть отнесены: метиловый красный, бромтимоловый синий, феноловый красный, фенолфталеин, тимолфталеин и др.
-
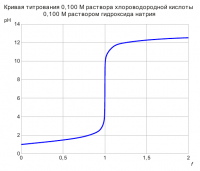
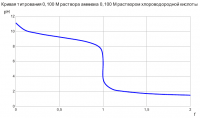
КРИВАЯ ТИТРОВАНИЯ СИЛЬНОЙ КИСЛОТЫ СИЛЬНЫМ ОСНОВАНИЕМ f = CNaOHVNaOH / (C0HClV0HCl) где f - степень оттитрованности; CNaOH - концентрация титранта, моль/л; VNaOH - объем добавленного титранта, мл; C0HCl - исходная концентрация хлороводородной кислоты в растворе, моль/л; V0HCl - исходный объем раствора хлороводородной кислоты, мл. 1. f = 0 (Раствор сильной кислоты) pH = -lgC0HCl f = 0,000; pH = 1,00 2. 0 < f < 1 (Раствор сильной кислоты) [H3O+] = (1 - f)C0HClV0HCl / (V0HCl + VNaOH) f = 0,010; pH = 1,01 f = 0,050; pH = 1,04 f = 0,100; pH = 1,09 f = 0,200; pH = 1,18 f = 0,300; pH = 1,27 f = 0,400; pH = 1,37 f = 0,500; pH = 1,48 f = 0,600; pH = 1,60 f = 0,700; pH = 1,75 f = 0,800; pH = 1,95 f = 0,900; pH = 2,28 f = 0,950; pH = 2,59 f = 0,990; pH = 3,30 f = 0,999; pH = 4,30 3. f = 1 (Нейтральный раствор) [H3O+] = [OH-]; pH = pKw / 2 f = 1,000; pH = 7,00 4. f > 1 (Избыток сильного основания) [H3O+] = Kw(V0HCl + VNaOH) / ((f - 1)C0HClV0HCl) f = 1,001; pH = 9,70 f = 1,010; pH = 10,70 f = 1,100; pH = 11,68 f = 1,200; pH = 11,96 f = 1,500; pH = 12,30 f = 1,800; pH = 12,46 f = 2,000; pH = 12,52 Выводы: Для данных условий титрования подойдут все индикаторы, диапазон перехода окраски которых лежит в области рН от 4 до 10. К таким индикаторам могут быть отнесены: метиловый оранжевый, метиловый красный, бромтимоловый синий, феноловый красный, фенолфталеин и др.
-
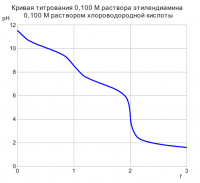
КРИВАЯ ТИТРОВАНИЯ МНОГОКИСЛОТНОГО ОСНОВАНИЯ СИЛЬНОЙ КИСЛОТОЙ Этилендиамин (Y) - слабое двухкислотное основание (Ka1 = 1,0*10-7, Ka2 = 8,3*10-11; pKa1 = 7,00, pKa2 = 10,08). f = CHClVHCl / (C0YV0Y) где f - степень оттитрованности; CHCl - концентрация титранта, моль/л; VHCl - объем добавленного титранта, мл; C0Y - исходная концентрация этилендиамина в растворе, моль/л; V0Y - исходный объем раствора этилендиамина, мл. 1. f = 0 (Раствор слабого основания) pH = 1/2 * (pKw + pKa2 + lgC0Y) f = 0,00; pH = 11,54 2. 0 < f < 1 (Буферный раствор: "слабая кислота - слабое основание") pH = pKa2 - lgf + lg(1 - f) f = 0,15; pH = 10,83 f = 0,20; pH = 10,68 f = 0,30; pH = 10,45 f = 0,40; pH = 10,26 f = 0,50; pH = 10,08 f = 0,60; pH = 9,90 f = 0,70; pH = 9,71 f = 0,80; pH = 9,48 f = 0,85; pH = 9,34 f = 0,90; pH = 9,13 3. f = 1 (Раствор амфолита) [H3O+] = (Ka1(Kw + Ka2CHY+) / (Ka1 + CHY+))1/2 CHY+ = C0YV0Y / (V0Y + VHCl) f = 1,00; pH = 8,54 4. 1 < f < 2 (Буферный раствор: "слабая кислота - слабое основание") pH = pKa1 - lg(f - 1) + lg(2 - f) f = 1,15; pH = 7,75 f = 1,20; pH = 7,60 f = 1,30; pH = 7,37 f = 1,40; pH = 7,18 f = 1,50; pH = 7,00 f = 1,60; pH = 6,82 f = 1,70; pH = 6,63 f = 1,80; pH = 6,40 f = 1,90; pH = 6,04 f = 1,95; pH = 5,72 f = 1,99; pH = 5,00 5. f = 2 (Раствор слабой кислоты) pH = 1/2 * (pKa1 - lgCH2Y2+) CH2Y2+ = C0YV0Y / (V0Y + VHCl) f = 2,00; pH = 4,24 6. f > 2 (Избыток сильной кислоты) [H3O+] = (f - 2)C0YV0Y / (V0Y + VHCl) f = 2,01; pH = 3,48 f = 2,10; pH = 2,49 f = 2,20; pH = 2,20 f = 2,50; pH = 1,84 f = 2,90; pH = 1,64 f = 3,00; pH = 1,60 Выводы: Хоть данная кривая титрования и имеет два скачка, но первый из них (f = 1) очень маленький. Поэтому фиксировать конечную точку титрования (особенно при использовании визуальных методов) лучше по второму скачку титрования (f = 2). Для этой цели подойдут индикаторы, изменяющие окраску в диапазоне рН от 3,5 до 5 (метиловый оранжевый, бромфеноловый синий, бромкрезоловый зеленый, конго красный и др.).
-
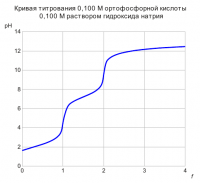
КРИВАЯ ТИТРОВАНИЯ МНОГООСНОВНОЙ КИСЛОТЫ СИЛЬНЫМ ОСНОВАНИЕМ f = CNaOHVNaOH / (C0H3PO4V0H3PO4) где f - степень оттитрованности; CNaOH - концентрация титранта, моль/л; VNaOH - объем добавленного титранта, мл; C0H3PO4 - исходная концентрация ортофосфорной кислоты в растворе, моль/л; V0H3PO4 - исходный объем раствора ортофосфорной кислоты, мл. 1. f = 0 (Раствор кислоты средней силы) Ka1 = 7,1*10-3, Ka2 = 6,2*10-8, Ka3 = 5,0*10-13; pKa1 = 2,15, pKa2 = 7,21, pKa3 = 12,30. [H3O+]2 + Ka1[H3O+] - Ka1C0H3PO4 = 0 f = 0,00; pH = 1,63 2. 0 < f < 1 (Буферный раствор: "кислота средней силы - очень слабое основание") [H3O+]2 + (CH2PO4- + Ka1)[H3O+] - Ka1CH3PO4 = 0 CH3PO4 = (1 - f)C0H3PO4V0H3PO4 /(V0H3PO4 + VNaOH) CH2PO4- = f C0H3PO4V0H3PO4 /(V0H3PO4 + VNaOH) f = 0,10; pH = 1,76 f = 0,20; pH = 1,89 f = 0,30; pH = 2,02 f = 0,40; pH = 2,15 f = 0,50; pH = 2,28 f = 0,60; pH = 2,43 f = 0,70; pH = 2,61 f = 0,80; pH = 2,83 f = 0,90; pH = 3,17 f = 0,95; pH = 3,49 f = 0,98; pH = 3,90 3. f = 1 (Раствор амфолита) [H3O+] = (Ka1(Kw + Ka2CH2PO4-) / (Ka1 + CH2PO4-))1/2 CH2PO4- = C0H3PO4V0H3PO4 / (V0H3PO4 + VNaOH) f = 1,00; pH = 4,71 4. 1 < f < 2 (Буферный раствор: "слабая кислота - слабое основание") pH = pKa2 + lg(f - 1) - lg(2 - f) f = 1,10; pH = 6,26 f = 1,20; pH = 6,60 f = 1,30; pH = 6,84 f = 1,40; pH = 7,03 f = 1,50; pH = 7,21 f = 1,60; pH = 7,39 f = 1,70; pH = 7,58 f = 1,80; pH = 7,81 f = 1,90; pH = 8,16 f = 1,95; pH = 8,49 f = 1,98; pH = 8,90 5. f = 2 (Раствор амфолита) [H3O+] = (Ka2(Kw + Ka3CHPO42-) / (Ka2 + CHPO42-))1/2 CHPO42- = C0H3PO4V0H3PO4 / (V0H3PO4 + VNaOH) f = 2,00; pH = 9,65 6. 2 < f < 3 (Буферный раствор: "очень слабая кислота - основание средней силы") CPO43-[H3O+]2 - (Kw + Ka3CHPO42-)[H3O+] - Ka3Kw = 0 CHPO42- = (3 - f)C0H3PO4V0H3PO4 /(V0H3PO4 + VNaOH) CPO43- = (f - 2)C0H3PO4V0H3PO4 /(V0H3PO4 + VNaOH) f = 2,05; pH = 10,80 f = 2,10; pH = 11,11 f = 2,20; pH = 11,42 f = 2,30; pH = 11,60 f = 2,40; pH = 11,74 f = 2,50; pH = 11,84 f = 2,60; pH = 11,92 f = 2,70; pH = 12,00 f = 2,80; pH = 12,06 f = 2,90; pH = 12,11 f = 2,95; pH = 12,14 f = 2,98; pH = 12,15 7. f = 3 (Раствор основания средней силы) CHPO42- = 0 CPO43-[H3O+]2 - Kw[H3O+] - Ka3Kw = 0 CPO43- = C0H3PO4V0H3PO4 /(V0H3PO4 + VNaOH) f = 3,00; pH = 12,16 8. f > 3 (Смесь сильного основания и основания средней силы) (COH- + CPO43-)[H3O+]2 + (COH-Ka3 - Kw)[H3O+] - KwKa3 = 0 COH- = (f - 3)C0H3PO4V0H3PO4 /(V0H3PO4 + VNaOH) CPO43- = C0H3PO4V0H3PO4 /(V0H3PO4 + VNaOH) f = 3,10; pH = 12,20 f = 3,30; pH = 12,28 f = 3,50; pH = 12,34 f = 4,00; pH = 12,45 Выводы: Несмотря на то что кислота трехосновная, на кривой титрования видны только два скачка. Для фиксации первого скачка титрования могут применяться индикаторы, изменяющие окраску в диапазоне рН от 4 до 5 (конго красный, бромкрезоловый зеленый, бромфеноловый синий), для фиксации второго скачка - от 9 до 10,5 (фенолфталеин, тимолфталеин).
-
КРИВАЯ ТИТРОВАНИЯ СЛАБОГО ОСНОВАНИЯ СИЛЬНОЙ КИСЛОТОЙ f = CHClVHCl / (C0NH3V0NH3) где f - степень оттитрованности; CHCl - концентрация титранта, моль/л; VHCl - объем добавленного титранта, мл; C0NH3 - исходная концентрация аммиака в растворе, моль/л; V0NH3 - исходный объем раствора аммиака, мл. 1. f = 0 (Раствор слабого основания) pKBH+ = 9,24 pH = 1/2 * (pKw + pKBH+ + lgC0NH3) f = 0,00; pH = 11,12 2. 0 < f < 1 (Буферный раствор) pH = pKBH+ - lgf + lg(1 - f) f = 0,10; pH = 10,19 f = 0,20; pH = 9,84 f = 0,30; pH = 9,61 f = 0,40; pH = 9,42 f = 0,50; pH = 9,24 f = 0,60; pH = 9,06 f = 0,70; pH = 8,87 f = 0,80; pH = 8,64 f = 0,90; pH = 8,28 f = 0,95; pH = 7,96 f = 0,99; pH = 7,24 3. f = 1 (Раствор слабой кислоты) pH = 1/2 * (pKBH+ - lgCNH4+) CNH4+ = C0NH3V0NH3 / (V0NH3 + VHCl) f = 1,00; pH = 5,27 4. f > 1 (Избыток сильной кислоты) [H3O+] = (f - 1)C0NH3V0NH3 / (V0NH3 + VHCl) f = 1,01; pH = 3,30 f = 1,10; pH = 2,32 f = 1,20; pH = 2,04 f = 1,50; pH = 1,70 f = 1,90; pH = 1,51 f = 2,00; pH = 1,48 Выводы: Для данных условий титрования подойдут все индикаторы, диапазон перехода окраски которых лежит в области рН от 4 до 6. К таким индикаторам относятся: конго красный, метиловый красный, резорциновый синий и др.
-
КРИВАЯ ТИТРОВАНИЯ СЛАБОЙ КИСЛОТЫ СИЛЬНЫМ ОСНОВАНИЕМ f = CNaOHVNaOH / (C0БКV0БК) где CNaOH - концентрация титранта, моль/л; VNaOH - объем добавленного титранта, мл; C0БК - исходная концентрация бензойной кислоты в растворе, моль/л; V0БК - исходный объем раствора бензойной кислоты, мл. 1. f = 0 (Раствор слабой кислоты) Ka = 6,3*10-5; pKa = 4,20 pH = 1/2 * (pKa - lgC0БК) f = 0,00; pH = 2,60 2. 0 < f < 1 (Буферный раствор) pH = pKa + lgf - lg(1 - f) f = 0,10; pH = 3,24 f = 0,20; pH = 3,60 f = 0,30; pH = 3,83 f = 0,40; pH = 4,02 f = 0,50; pH = 4,20 f = 0,60; pH = 4,38 f = 0,70; pH = 4,57 f = 0,80; pH = 4,80 f = 0,90; pH = 5,15 f = 0,95; pH = 5,48 f = 0,99; pH = 6,20 3. f = 1 (Раствор слабого основания) pH = 1/2 * (pKw + pKa + lgCБ) СБ = C0БКV0БК / (V0БК + VNaOH) f = 1,00; pH = 8,45 4. f > 1 (Избыток сильного основания) [H3O+] = Kw(V0БК + VNaOH) / ((f - 1)C0БКV0БК) f = 1,01; pH = 10,70 f = 1,10; pH = 11,68 f = 1,20; pH = 11,96 f = 1,50; pH = 12,30 f = 1,90; pH = 12,49 f = 2,00; pH = 12,52 Выводы: Для данных условий титрования подойдут все индикаторы, диапазон перехода окраски которых лежит в области рН от 7 до 10. К таким индикаторам относятся: феноловый красный, тимоловый синий, фенолфталеин и др.