
Fialka7
-
Постов
37 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Fialka7
-
-
Надо полагать, альдольная конденсация.
CH3-CH2-CH(CH3)-CH2-C(OH)(CH3)-CH2-CO-CH2-CH(CH3)-CH2-CH3
Получается молекула с тремя хиральными центрами. У двух конфигурация фиксирована, а вновь возникший (у гидроксила) представлен двумя изомерами. То есть получится два диастереомера с преобладанием одного из них.
Реакция обратима, равновесие сильно смещено в сторону продукта конденсации.
Спасибо.
-
Простите, Ваши предположения основаны на чём-то конкретном или же это просто, что называется, полёт фантазии.
. С уважением
Полет фантазии)) Спасибо!
-
-
Ну, как же?! Ассиметрическими после восстановления станут оба "бывших" карбонильных углеродных атома, превратившись в карбинольные. Отсюда и 4 энантиомера. Имеющийся изначально хиральный центр, как Вам уже указали ранее, каких-либо преобразований претерпеть не должен.
. С уважением
А почему 4 энантиомера образуется??? При востановлении CH3-C=O группы должная же быть рацемическая смесь, и при восстановлении циклогексанона ведь наверное какой-то из энантиомеров будет преобладать??
-
Довольно странно. Кетоны прекрасно гидрируются и боргидридом, и алюмогидридом до спиртов. Хиральный центр удалён от реакционного, и никак не активирован, поэтому его конфигурация меняться не должна.
А, ну да, в продукте будет уже три хиральных центра. Всего - четыре изомера. Но разницы-то между боргидридом и алюмогидридом не должно быть никакой.
А какие это будут изомеры, почему 4?
-
Здравствуйте.
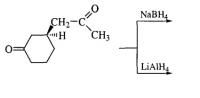
Прошу помочь с такой задачей:
Завершите следующие реакции восстановления:

Определите конфигурации хиральных центров в продуктах.В каком случае что будет восстанавливаться?
-
Может, вот так - [Cr(H2O)3Cl3], K2[Сr(H2O)(OH)5] -?
Спасибо!
-
Здравствуйте.
Составьте формулу комплексного соединения:
1) по эмпирической формуле - CrCl3 x 3H2O
2) по названию - аквапентагидроксохромат калия
Почему-то в первом [СrСl3(H2O)3] - не правильно, а во втором - K2[Сr(OH)5(H2O)] - тоже не правильно. Что не так? -
При сильном нагревании CCl4, HCl, H2O, N2
Спасибо
-
-
Метал, этил, пропил
Диметил, метилэтил, диэтил
Спасибо.
-
Добрый день.
Напишите структурные формулы первых трех представителей гомологического ряда циклопропанов, имеющих:а) одну боковую цепь,
б) две боковые цепи.
Не могу понять, что тут имелось ввиду. В а), например, подходят метилциклопропан, этилциклопропан и пропилциклопропан или метилциклопропан, метилциклобутан и метилциклопентан? -
Здравствуйте.
Для процесса синтеза аммиака рассчитать значение константы равновесия Kp, если в равновесном газе, выходящем из аппарата, содержится 13,9% аммиака. Процесс осуществляется под давлением 30 МПа, исходная смесь содержит реагенты в стехиометрическом количестве.
Не пойму, как решать(
Уравнение реакции N2 + 3H2 = 2NH3Kp = P2(NH3)/(P(N2) x P3(H2))
P(NH3) = P(общее) x φ(NH3) = 30 МПа x 0,139 = 4,17 МПа
Как дальше? -
Наиболее вероятна реакция с меньшим значением ΔG, т.е. с большим значением ЭДС
Реакции с одинаковым ЭДС могут иметь разные ΔG, т.к. число электронов может быть разным в соответствии с формулой ΔG = - nFE, т.е. число электронов тоже надо учесть?
-
Добрый день.
При взаимодействии платины с «царской водкой» азотная кислота восстанавливается до NO, а окисление платины возможно до ионов Рt2+, PtCl42– или PtCl62–. Написать уравнения реакций и выбрать из них наиболее вероятную, исходя из значений окислительно-восстановительных потенциалов.1) Рt – 2e– = Рt2+; j°= 1,20 В
2) Рt + 4Cl– – 2e– = PtCl42–; j°= 0,73 В
3) Рt + 6Cl– – 4e–= PtCl62–; j°= 0,68 В
4) NO3– + 4H+ + 3e– = NO + 2H2O; j°= 0,96 В
Раз потенциал окисления платины до Рt2+ больше чем потенциал восстановления азотной кислоты то реакция будет протекать в обратном направлении , т.е. Рt2+ будет окислять NO до NO3–? Потенциалы окисления платины до PtCl42– и PtCl62– меньше, чем потенциал восстановления азотной кислоты, то эти реакции будут протекать в направлении окисления платины? Как из них выбрать наиболее вероятную? Надо вычислять ΔG для каждой реакции?
-
Здравствуйте.
Чему будет равен pH раствора CH3COOH концентрацией 0,00000001 н.?
Закон разбавления Оствальда здесь применить нельзя, т.к. получается ерунда:α = кв. корень (Кд / С) = кв. корень (1,74 10-5 / 10-8) = кв. корень (1,74 103) = 41,7
Как тогда рассуждать?
-
ΔG (реакции) = ΔG (Ca(OH)2) + ΔG (С2H2) - ΔG (CaC2) - 2ΔG (H2O(г)) = -896,8 + 209,2 -(- 67,72) - 2∙(-228,6) = -162,68
Точно, спасибо!
-
Вы приведите табличные данные и расчёты, а то задаёте вопрос - "прилетала птичка, посидела, и улетела - что за птичка?"
Реакци
CaC2(к) + 2H2O(г) = Ca(OH)2(к) + С2H2(г)
ΔH (CaC2) = -62,7 кДж/моль, S (CaC2) = 70,22 Дж/(моль∙К), ΔG (CaC2) = -67,72 кДж/моль
ΔH (H2O(г)) = -241,8 кДж/моль, S (H2O(г)) = 188,7 Дж/(моль∙К), ΔG (H2O(г)) = -228,6 кДж/моль
ΔH (Ca(OH)2) = -986,6 кДж/моль, S (Ca(OH)2) = 76,1 Дж/(моль∙К), ΔG (Ca(OH)2) = -896,8 кДж/моль
ΔH (С2H2) = 226,8 кДж/моль, S (С2H2) = 200.8 Дж/(моль∙К), ΔG (С2H2) = 209,2 кДж/моль
ΔH (реакции) = ΔH (Ca(OH)2) + ΔH (С2H2) - ΔH (CaC2) - 2ΔH (H2O(г)) = -986,6 + 226,8 - (-62,7) - 2∙(-241,8) = -213,5 кДж/моль
ΔS (реакции) = S (Ca(OH)2) + S (С2H2) - S (CaC2) - 2S (H2O(г)) = 76,1 + 200,8 - 70,22 - 2∙188,7 = -170,72 Дж/(моль∙К)
ΔG (реакции) = ΔG (Ca(OH)2) + ΔG (С2H2) - ΔG (CaC2) - 2ΔG (H2O(г)) = -896,8 + 209,2 - 67,72 - 2∙(-228,6) = - 298,12 кДж/моль
ΔG реакции по формуле Гиббса при T = 298 K
ΔG (реакции) = ΔH (реакции) - T∙ΔS (реакции) = -213,5 - 298∙(-170,72∙10-3) = 162,63 кДж/моль
-
Здравствуйте.
Чем можно объяснить расхождение в величинах ΔG реакции, если вычислять двумя разными способами - через ΔG веществ (табличные данные) и по формуле ΔG = ΔH - TΔS, где ΔH и ΔS посчитаны через табличные данные ΔH и S веществ? Расхождение большое - по одному способу получается -213,5 кДж/моль, по другому -162,6 кДж/моль. Все проверяла, ошибки в вычислениях быть не может. Табличные данные тоже переписаны верно. -
830 см-1 это внеплоскостные колебания ароматических С-Н. Но зачем это тут - не ясно. Никакой информации, кроме того, что это - производное бензола из этого не извлечёшь, а это и так понятно.
Один изомер при монохлорировании даст пара-замещённый бензонитрил. Например п-этоксибензонитрил C2H5-O-C6H4-CN. Тогда исходником будет п-этоксианилин.
Но тут и более изысканный эфир подойдёт по составу: CH3-O-CH2-C6H4-NH2
Спасибо!
-
Здравствуйте.
Помогите решить такую задачу:
Вещество А состава С8H11NO образует соли с сильными кислотами, при диазотировании с последующим нагреванием раствора диазосоединения с цианидом меди(I) Cu2(CN)2 получается соединение, которое в ИК-спектре имеет полосу 830 см-1 и при монохлорировании в присутствии катализатора образует только один изомер. Установите строение соединения А и напишите схемы приведенных реакций.
Не пойму, к чему относится полоса 830 см-1? Вещество А будет замещенным анилином, т.к. оно образует соль диазония, которая потом вступает в реакцию Зандмейера с Cu2(CN)2 -
Здравствуйте.
Такой вопрос: расположите соединения в порядке уменьшения их реакционной способности в реакции нитрования: бензол, 1,3,5-триметилбензол, толуол, мета-ксилол, пара-ксилол. Наверное, будет вот так: мета-ксилол > пара-ксилол > толуол > бензол, только куда 1,3,5-триметилбензол вставить - не знаю. Где-то между мета-ксилолом и пара-ксилолом?
-
Вопрос действительно странный. Первый раз слышу про "группы восстановителей". А про агрегатное состояние - это-то вообще при чём тут?
Натрий в аммиаке - это твёрдое в жидком, водород тут вообще не при делах. Восстановитель - натрий, как он есть. То же самое относится и к натрию в бутаноле.
"Калийалюмогидрид" - это жесть! Никогда не слышал, шоб алюмогидрид в виде калиевой соли юзали. Только в виде ЛАГа - литийалюмогидрида. Но. по-любасу - это твёрдая штука.
Фенилгидразин - жидкость. Его, конечно, можно окислить, но в качестве именно восстановителя использовать - это новшество!
Спасибо!
-
еще надо учесть, что вода и этиленгликоль - доноры водородной связи, ацетон - не является донором водородной связи (биполярный, апротонный НДВС). и того вода и спирты - SN1, ацетон - SN2.
Спасибо!

Гидролиз SnCl4
в Решение заданий
Опубликовано
Здравствуйте
Помогите с задачей:
Какое соединение образует SnCl4 c продуктом его гидролиза? Написать уравнения реакций.
SnCl4 гидролизуется до SnO2 и HCl?