Zebra_007
Пользователи-
Постов
46 -
Зарегистрирован
-
Посещение
Весь контент Zebra_007
-
По реакции Чугаева - Церевитинова с 0,120 г спирта, молекулярная масса которого равна 60, выделилось 44,8 мл метана (н.у.). Сколько атомов активного водорода в молекуле спирта? Какое он может иметь строение? Я решил эту задачу, но не совсем понял: как узнать количество атомов активного водорода в молекуле спирта? Говоря о строении подрузамивается строение спирта, ведь так?
-
-
-
Правильно ли решил цепочку? Если есть какие-нибудь ошибки и недочёты то, пожалуйста, дополните с наглядным примером)
-
Изучаю элементорганические соединения, но ни в одной источнике не могу найти какие элементорганические соединения называют смешанными, а какие полными? Внести ясность, пожалуйста.
-
-
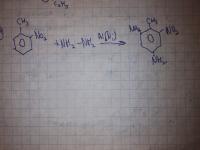
Соединение состава C8H11N (А) при действии азотистой кислоты дает наряду с олефином вещество Б, имеющее состав С8Н10О. При действии дихромата калия в разбавленной серной кислоте вещество Б превращается в вещество C8H8О (В), которое не дает реакции серебряного зеркала и при действии гидроксиламина превращается в C8H9NO (вещество Г). Последнее при действии натрия в спирте снова образует соединение А. Расшифруйте структуры веществ и схемы их превращений. Моё решение (поправьте, если есть ошибки, пожалуйста): CH3-C6H4-CH2-NH2 + HNO2 ---> CH3-C6H4-CH2-OH + N2 + H2O CH3-C6H4-CH2-OH + K2Cr2O7 + H2SO4 ---> Cr(SO4)3 + K2SO4 + 4H2O +C6H5-C(O)-CH3 дальше тупик... мб так: C6H5-C(O)-CH3 + NH2-OH ---> C6H5-CH(NO)-CH3 + H2O C6H5-CH(NO)-CH3 -(Na, спирт)-> CH3-C6H4-CH2-NH2
-
-
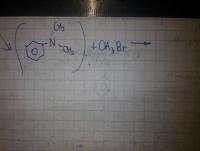
C6H5N(CH3)2 + CH3Br ---> комментарий: без вариантов CH3-CH2NH2 + NaNO2 + HCl ---> CH3CH2OH + N2 + NaCl + H2O комментарий: правильно ли?
-
Соединение состава C8H11N (А) при действии азотистой кислоты дает наряду с олефином вещество Б, имеющее состав С8Н10О. При действии дихромата калия в разбавленной серной кислоте вещество Б превращается в вещество C8H8О (В), которое не дает реакции серебряного зеркала и при действии гидроксиламина превращается в C8H9NO (вещество Г). Последнее при действии натрия в спирте снова образует соединение А. Расшифруйте структуры веществ и схемы их превращений. Моё решение (поправьте, если есть ошибки, пожалуйста): CH3-C6H4-CH2-NH2 + HNO2 ---> CH3-C6H4-CH2-OH + N2 + H2O CH3-C6H4-CH2-OH + K2Cr2O7 + H2SO4 ---> Cr(SO4)3 + K2SO4 + 4H2O +C6H5-C(O)-CH3 дальше тупик... мб так: C6H5-C(O)-CH3 + NH2-OH ---> C6H5-CH(NO)-CH3 + H2O C6H5-CH(NO)-CH3 -(Na, спирт)-> CH3-C6H4-CH2-NH2
-
А бензойный альдегид (c6h5cho) при взаимодействии с изобутиламином что даст?
-
Доброго времени суток. У меня тут затруднения с цепочкой, две реакции решил, а дальше - тупик. Есть мысли? p.s. для моего понимания с решением, если можно
-
Условия задачи: Для установления титра раствора HCl навеска безводной соды (х.ч.) массой 5,2060 г растворена в мерной колбе на 500 мл. На титрование 25 мл раствора расходуется 26,18 мл устанавливаемого раствора. Определите: а) молярную концентрацию эквивалента HCl, б) KHCl, в) ТHCl, г) ТHCl/Na2CO3
-
На титрование раствора, полученного растворением 0,5120 г Na2B4O7*10H2O (х.ч.), расходуется 2,32 мл раствора HCl. Определите: а) THCl, б) THCl/KOH, в) молярную концентрацию эквивалента HCl и г) KHCl
-
Я знаю, что изрядно вас достал, но мне нужна помощь. Условия: В мерную колбу на 500 мл помещено 25,00 HCl пл. 1,19. Объём доведен до метки. На титрование 20,00 мл полученного раствора а расходуется 25,13 мл раствора едкого натрия (Т=0,01976 г/мл). Какова молярная концентрация эквивалента исходного раствора кислоты?
-
Для установления титра раствора HCl взято 20 мл раствора NaOH (T=0,03982 г/мл). Раствор разбавлен водой в мерной колбе на 200 мл до метки. На титрование 20,00мл полученного раствора расходуется 18,95 мл раствора HCl. Определить: а) молярную концентрацию эквивалента HCl, б) KHCl, в) THCl, г) THCl/NaOH
-
Для установления концентрации и титра KMnO4 приготовлен раствор из 1,5020 г H2C2O4*2H2O (х.ч.) в мерной колбе на 250 мл. На титрование 25,00 мл этоо раствора расходуется в среднем 23,68 мл устанавливаемого раствора KMnO4. Определите: а) молярную концентрацию KMnO4, б) TKMnO4, в) TKMnO4/H2C2O4 , г) KKMnO4.
-
Помогите решить задачку по аналитике. Условия: Для установления титра раствора H2SO4 навеска Na2B4O7*10H2O (х.ч.) массой 2,4000 г растворена в мерной колбе на 200 мл. На титрование 20 мл приготовленного раствора буры расходуется 33,85 мл раствора H2SO4. Вычислите: а) молярную концентрацию эквивалента H2SO4, б) KH2SO4, В) ТH2SO4, Г) TH2SO4/Na2O
-
Помогите решить задачку, пожалуйста. Условия: Для установления титра раствора HCl навеска безводной соды (х.ч.) массой 5,2060 г растворена в мерной колбе на 500 мл. На титрование 25 мл раствора расходуется 26,18 мл устанавливаемого раствора. Определите: а) молярную концентрацию эквивалента HCl, б) KHCl, в) ТHCl, г) ТHCl/NaOН
-
скинул фотку ж
-
Задание: Сколько граммов буры Na2B4O7*10H2O (х.ч.) пойдёт на приготовление 500 мл раствора, необходимого для устновления титра - 0,1н HCl?