-
Постов
49 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные XummY
-
-
Ошибка в расчете конц. меди в комплексе. Концентрация лиганда у вас ведь не 0,4 М. Пересчитайте взяв за x - конц Cu2+, а за 4х - NH3.
В ответе у меня вышло примерно 65 мВ.
Как у вас вышло 65 мВ?? Не поделитесь решением?

-
 1
1
-
-
-
Тут лучше химики скажут. Было бы какое химически нейтральное к меди соединение , типа гидроксида меди, например, то было бы проще.
...А вы логарифмы точно правильно посчитали...?
логарифмы вроде посчитаны верно (хотя имеются какие-то сомнения)
-
 1
1
-
-
А вам не нужно учитывать реакцию меди с комплексом меди-2 и образованием комплекса меди-1 ?
Да и я о том же, понять до конца не могу что к чему. Буду благодарен Вам, если поможете примером (как это сделать).
-
 1
1
-
-
Здравствуйте!

Был проведён опыт, суть которого в следующем. В два стаканчика наливаются растворы сульфата меди CuSO4 и аммиачной комплексной соли [Cu(NH3)4]SO4 концентрацией 0,1 М каждый. В каждый раствор помещаются медные пластинки. Растворы соединены стеклянной трубкой, заполненной раствором электролита.
По заданию, необходимо привести условную запись концентрационного ГЭ, составить ионно-электронные уравнения процессов на электродах (оба медные). Определить ЭДС.
В общем получается откровенно говоря, фигня какая-то. Особенно в расчёте равновесных электродных потенциалов и концентрации ионов меди в растворе. Возникла проблема в определении потенциала на катоде.
Посмотрите пожалуйста. Кто что подскажет. Спасибо.
-
 1
1
-
-
В этой теме до сих пор ведутся жаркие обсуждения? Ничего себе
 В любом случае, всем спасибо!
В любом случае, всем спасибо! -
Надеюсь Вы правы, всем спасибо!

-
Как понимаю, ионно-молекулярное уравнение электролиза раствора CuCl2 будет таким:
Cu2+ + 2Cl- = Cu0 + Cl2
-
-
А как будет? Хлор что ли будет выделяться? Это фантастика.
А-а! Там что-то про бескислородные кислоты какая-то закорючка типа ClI2- ...
Но что это меняет? Йод как болтался там, так и будет болтаться.
Можно, конечно, предположить окисление йода в гипоиодит или дальше, тут надо таблицы потенциалов смотреть. Но что-то сомнительно, что потенциал окисления иода(0) окажется ниже потенциала окисления меди.
Хотя, возможно, что для корректного решения задачи надо представить преподу эти циферки.
Йод? Мы вроде с ним дел не имеем в этой задаче

-
 1
1
-
-
-
Здравствуйте, товарищи Химики!

Вопрос небольшой. Имеем раствор CuCl2 , катод и анод изготовлены из меди. Как понимаю, на катоде происходит восстановление меди, т.е. Cu2++ 2e = Cu0.
Подскажите пожалуйста, что будет с анодным процессом. При условии, что в растворе CuCl2 содержатся анионы бескислородных кислот Cl-2.
2Cl- - 2e = 2Cl0 или Cu0 - 2e = Cu2+
Подскажите пожалуйста. Спасибо!
-
 1
1
-
-
Всем спасибо, разобрался!

-
 1
1
-
-
Здравствуйте!
Задание следующее: Через раствор соли с концентрацией ионов металла [Mеn+] (моль/дм3) пропускают постоянный ток силой 1 А в течение 1 часа. Выполните следующие задания:
1. Составьте схему электролиза раствора, напишите уравнения процессов, протекающих на электродах. Катодный процесс подтвердите расчетом.2. Рассчитайте массы (для газов – объем при нормальных условиях) веществ, выделившихся на электродах.1 задание я выполнил (приложение).
 Помогите пожалуйста со 2 заданием. Не совсем понимаю как это выполнить.Спасибо.
Помогите пожалуйста со 2 заданием. Не совсем понимаю как это выполнить.Спасибо.-
 1
1
-
-
Непонятно, почему на схеме элемента на меди "-", если это положительный электрод?
А на кадмии "+", если потенциал -0,433В??
Вообще, такие задачи легко проверять здесь: http://www.xumuk.ru/galvanopara/
Как понял, анодом в электрохимии принято называть электрод, на котором идет процесс окисления. Анодом будет электрод, у которого более отрицательный электродный потенциал, а катодом – электрод с более положительным потенциалом.
И поскольку в схеме гальванического элемента слева записывается анод, а справа – катод, то получается что в данном гальваническом элементе анодом является кадмиевый электрод, а катодом – медный. Анодом становится металл, имеющий меньший электродный потенциал восстановления, а катодом – металл, имеющий больший потенциал восстановления.
+
Поскольку медь в электрохимическом ряду напряжений стоит правее, чем кадмий, то медь имеет большее значение электродного потенциала восстановления, чем кадмий. Поэтому в данном гальваническом элементе медный электрод будет катодом, а кадмиевый – анодом.
Получается логичнее всего (правильнее) на схеме элементов поменять местами медь и кадмий?
-
 1
1
-
-
объясните , пожалуйста, доступным языком. не понимаю. совсем

Приведите пример какой-нибудь реакции, разберёмся

-
Здравствуйте, товарищи Химики!Небольшая просьба к Вам. Имеем задачу следующего характера: в таблице указаны материалы электродов и концентрации ионов металла в растворе электролита [Mеn+] (моль/дм3). Используя эти данные, выполните следующие задания:1. Составьте схему гальванического элемента.2. Рассчитайте электродные потенциалы анодного и катодного процессов, вычислите ЭДС гальванического элемента.3. Напишите уравнения процессов, протекающих на электродах. Составьте суммарное уравнение реакции, лежащей в основе работы гальванического элемента.Работу выполнил, но есть сомнения, пожалуйста, проверьте решение.Спасибо!
-
 1
1
-
-
. 1) при нулевом изменении энтропии TdS обращается в нуль, т.е. пренебрегать изменением энтальпии не правильно (dG = dH), ибо знак этой величины и будет определять возможность/невозможность протекания реакции в прямом направлении;
. 2) если же изменение энергии Гиббса у Вас всё-таки получилось равным нулю, поздравляем, Ваша реакция в данных условиях находится в состоянии равновесия, т.е. скорости прямой и обратной реакций абсолютно равны по модулю.
. С уважением
Спасибо большое, понял

-
 1
1
-
-
Энтропия есть мера хаоса. Наиболее хаотичны газы и сложные вещества. У нас тут три газа с одной стороны и три с другой, если не вникать в термодинамические справочники изменение энтропии близко к нулю.
Тогда скажите пожалуйста, при условии если ∆S ≈ 0 что будет с энергией Гиббса? ∆G ≈ 0 ? Как такое может быть?

-
 1
1
-
-
Друзья, здравствуйте!

Условие задачи следующее: Качественно оцените знак изменения энтропии при протекании реакции (∆S > 0, ∆S < 0 или ∆S ≈ 0). Объясните полученный результат.
Реакция Fe2O3(к) + 3H2(г) = 2Fe(к) + 3H2O(г)
Подскажите пожалуйста, что происходит с энтропией. Увеличивается ли объём образуемого вещества/изменяется степень беспорядочности?
Спасибо!
-
 1
1
-
-
Ионная связь в кристалле MgJ2. В молекуле, существующей в парАх, связь будет ковалентная сильно полярная. Молекулы такого типа неполярны, поскольку дипольные моменты, возникающие от сдвига электронной плотности к крайним атомам или наоборот, компенсируют друг друга. Векторная сумма равна нулю. С AsCl3 все нормально.
Спасибо ОГРОМНОЕ! Разобрался

-
 1
1
-
-
Раз молекула MgJ2 линейная, то она неполярная. У линейных молекул дипольного момента нет. CO2, например, неполярен, а SO2 полярен.
Имеются в виду, конечно, центросимметричные трехатомные молекулы. У COS будет дипольный момент.
Получается ионная связь? Неполярная молекула? А с AsCl3?
-
 1
1
-
-
Товарищи, здравствуйте!
 Задача кажется не очень сложная, но есть сомнения (особенно с иодидом магния). Посмотрите пожалуйста решение, может чего заметите, может чего исправить нужно.
Условие задачи:Определите характер химической связи между атомами в молекулах AsCl3 и MgI2. Укажите возможный тип гибридизации орбиталей центрального атома, наличие σ- и π-связей. Покажите пространственную структуру молекул. Полярны ли связь в молекулах и молекулы в целом? Определить разность электроотрицательности.Спасибо!
Задача кажется не очень сложная, но есть сомнения (особенно с иодидом магния). Посмотрите пожалуйста решение, может чего заметите, может чего исправить нужно.
Условие задачи:Определите характер химической связи между атомами в молекулах AsCl3 и MgI2. Укажите возможный тип гибридизации орбиталей центрального атома, наличие σ- и π-связей. Покажите пространственную структуру молекул. Полярны ли связь в молекулах и молекулы в целом? Определить разность электроотрицательности.Спасибо!
-
 1
1
-







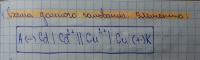





Разложение фенолята натрия
в Решение заданий
Опубликовано
Здравствуйте, уважаемые коллеги!
Подскажите пожалуйста причины разложения фенолята натрия в минеральной кислоте (HCl), буду вам признательно благодарен.
Спасибо.