
AdmiralHood
-
Постов
8 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные AdmiralHood
-
-
3 часа назад, yatcheh сказал:
"Сверхкритическое состояние" - это просто сильно сжатый реальный газ, со всеми вытекающими последствиями.
Споры о терминах — не моя стезя. Если хотите называть эту штуку газом — ничего не имею против, но сам предпочитаю пользоваться традиционной терминологией.
-
10 часов назад, yatcheh сказал:
Ежели рассуждать по-рабоче-крестьянски, то характерным признаком газа является его пропорциональная сжимаемость. Грубо говоря, если вы увеличиваете давление в газе в N раз, то объём при постоянной температуре уменьшается в N раз.
Характерный признак жидкости — практически полная несжимаемость при наличии текучести.
Так вот, когда вы исследуете вещество в разных точках закритической области фазовой диаграммы, то обнаруживаете, что не наблюдаются ни те, ни другие признаки. Сжимаемость перестаёт быть точно пропорциональной давлению, но и не снижается до величин, близких к нулю. За исключением, разумеется, пограничных областей с жидкостью и газом.
-
10 часов назад, Sovetnik сказал:
Линия затвердевания тоже неправильная, так как по ней следует, что азот будет иметь твердую фазу при температуре выше критической, что невозможно.
На вашей диаграмме та же ошибка - не будет кристаллического состояния при температуре выше критической ни при каком давлении.
Хотя, есть данные, что при очень высоких давлениях азот перестает быть двухатомной молекулой и может образовывать полимерные структуры, тогда возможны и жидкие и твердые фазы при плюсовых температурах.
http://dspace.nbuv.gov.ua/bitstream/handle/123456789/128443/01-Yakub.pdf?sequence=1
Нет таких ограничений на твёрдую фазу, давление рулит всегда. Посмотрите фазовую диаграмму любого вещества — закритическое состояние всегда граничит с твёрдой фазой.
-
В нижней и верхней частях диаграммы разные масштабы, поэтому линии раздела фаз претерпевают излом. Линии разного цвета взяты из разных источников.
Попутно нашёл забавную книжку с фазовыми диаграммами чистых элементов.
https://inis.iaea.org/collection/NCLCollectionStore/_Public/07/255/7255152.pdf
-
 1
1
-
-
В закритической области теряется различие между жидкостью и газом.
Если вы находитесь ниже критической точки и пересекаете линию конденсации, то у вас происходит явная смена фаз — газ превращается в жидкость или наоборот. Если же вы пройдёте тот же самый путь по фазовой диаграмме из начальной точки в конечную, обогнув сверху критическую точку, то вы перейдёте из жидкости в газ или обратно плавно, без явной смены фаз.
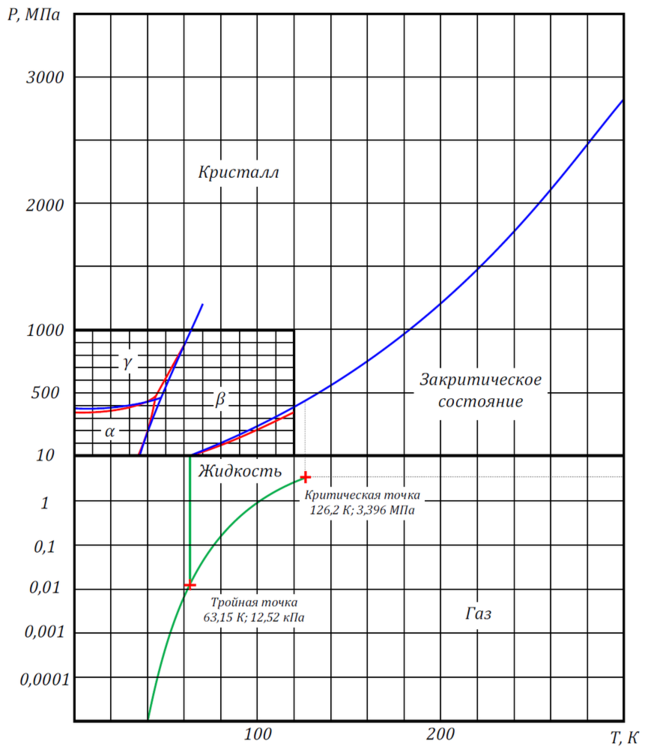
Сегодня разрисовал фазовую диаграмму азота по данным нескольких источников и залил в Википедию в статью «Азот». Наслаждайтесь!
На всякий случай помещаю сюда тоже.
-
 1
1
-
-
-
1. Диаграмма правильная.
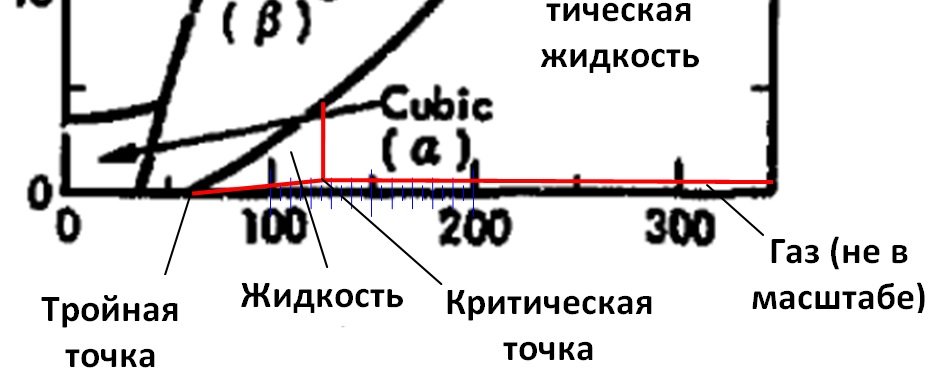
2. Но масштаб по оси давления такой большой, что критическое давление (34 атм) лежит практически на горизонтальной оси, то есть вся область газообразной фазы сливается с горизонтальной осью и на диаграмме не показывается.
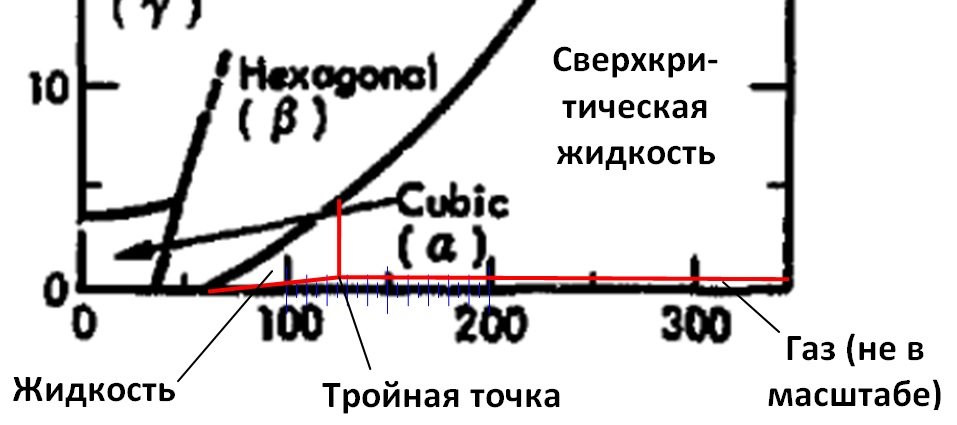
3. Есть нюанс. Область жидкости и сверхкритической фазы не разделена и называется «Liqiud». Если хотите исправить это досадное недоразумение, то проведите вертикальную линию из точки 127 К (критическая точка) до линии затвердевания. Треугольник слева будет жидкостью, справа — сверхкритическое состояние.
Ошибка: вместо «тройная точка» нужно «Критическая точка»
Азот - загадка
в Общий
Опубликовано
Да. Для воды, например, то же самое:
Синее и голубое слева и сверху — лёд различных модификаций.
Где-то при 28 000 атм при комнатной температуре азот должен затвердеть.