
colddawm
-
Постов
7 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные colddawm
-
-
-
4 минуты назад, FixMe сказал:
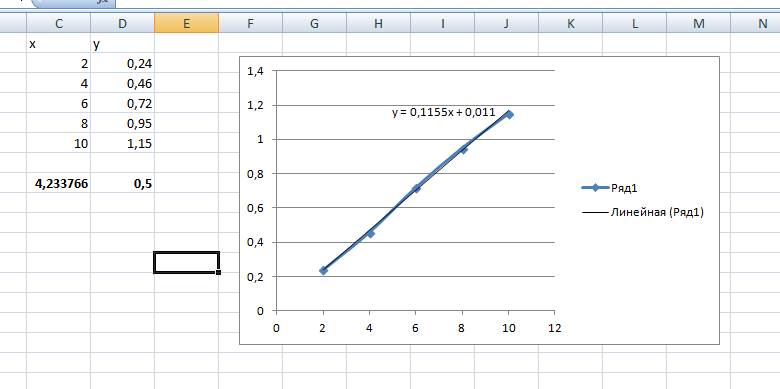
Каждой прямой соответствует определенное уравнение вида y = kx + b. Если в него подставить определенное значение y, можно узнать какому х оно соответствует.
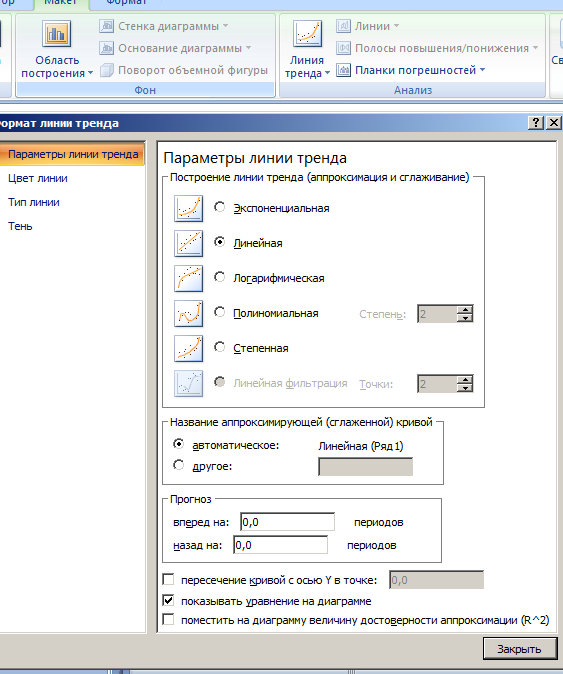
Для того, чтобы увидеть это уравнение в Excel нужно построить к вашему графику Линию тренда, а затем в настройках этой линии включить отображение уравнения на диаграмме.
Да,я пробовала это сделать. Значение получается x=2,1 . Но по графику вообще не логично, что 0,5 находится в этой точке...
-
Я с эксель вообще не дружу и понять не могу,как простейший график закончить делать.
Помогите пожалуйста(
Нужно поставить точку 0,5 на самом графике (на линии), а потом определить значение икса.
как это сделать?
Икс в данном случае будет массой металла в растворе.Нужно найти затем массовую долю металла.
Задача такая:Для определения металла навеску образца 0,1г растворили, перевели в мерную колбу на 100 мл, провели фотометрическую реакцию, довели до метки дистиллированной водой и измерили оптическую плотность: Ах=0,5 . Для построения градуировочного графика в 5 мерных колб на 100 мл поместили стандартный раствор, содержащий: 2,00; 4,00; 6,00; 8,00; 10 мг металла, провели фотометрическую реакцию, довели до метки дистиллированной водой и измерили оптическую плотность: А1 = 0,24; А2 = 0,46; А3 = 0,72; А4 = 0,95, А5 = 1,15.
Постройте градуировочный график в координатах А - масса металла m(Me),мг в растворе, по нему найдите массу металла в растворе, затем рассчитайте массовую долю металла в образце массой m г.
-
Для чего здесь дан рН? Как его нужно использовать? Вообще,я так поняла,что нужно найти молярные концентрации и подставить всё в формулу Нернста и всё. Правильно?
[H+]=1 моль/л? Это рН и есть конц.ионов водорода?
Сама задача:
Платиновый электрод помещен в раствор, содержащий КМnО4 массой m, г и MnSО4 массой m2, г в V, мл раствора и определенном pH. Температура стандартная – 298 К (25 0С). Вычислить разность потенциалов в электрохимической цепи (Электродвижущая сила, ЭДС), состоящей из данного электрода и электрода сравнения - стандартного водородного электрода (для которого температура – 298 К (250С); давление – 101325 Па (760 мм рт. ст.; 1 атм); активности всех компонентов в растворе – 1 моль/л.) по формуле ЭДС=Е2-Е1. Е2 - всегда больший потенциал.
Рассчитайте молярные концентрации КМnО4 и MnSО4, примите, что их концентрации равны соответствующим концентрациям [МnО4-] и [Mn2+].
Для расчета потенциала электрода, состоящего из платины, погруженной в раствор, содержащей окисленную форму MnO4- и восстановленную Mn2+ и число электронов n в уравнении полуреакции, используйте уравнение Нернста в форме:
(на картинке)
Потенциал стандартного водородного электрода в стандартных условиях равен Е1= Е10=0 В.
-
5 минут назад, aversun сказал:
Так вам что, градуировочный график построить. Сами ни как не можете, даже с карандашом и бумагой, не говоря уже об Excel?
0,1m, г -- это как понимать?
m=0,1г. Вот так
График да, не очень понятно как построить и как по нему значения массы и масс.доли искать.. -
Для определения металла навеску образца 0,1m, г растворили, перевели в мерную колбу на 100 мл, провели фотометрическую реакцию, довели до метки дистиллированной водой и измерили оптическую плотность: Ах . Для построения градуировочного графика в 5 мерных колб на 100 мл поместили стандартный раствор, содержащий: 2,00; 4,00; 6,00; 8,00; 10 мг металла, провели фотометрическую реакцию, довели до метки дистиллированной водой и измерили оптическую плотность: А1 = 0,24; А2 = 0,46; А3 = 0,72; А4 = 0,95, А5 = 1,15.
Постройте градуировочный график в координатах А - масса металла 0,1m (Me),мг в растворе, по нему найдите массу металла в растворе, затем рассчитайте массовую долю металла в образце массой 0,1m, г.


Вопрос по градуировочному графику в ЭКСЕЛЬ
в Аналитическая химия
Опубликовано
В итоге совсем другое уравнение...