
alex-s
-
Постов
22 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные alex-s
-
-
3 часа назад, Максим0 сказал:
Если на входе ЛАТР, то это - дурная идея, Латром запитайте трансформатор 230/12 В и через него вашу схему - тогда получите хоть какую-то мощность и электробезопасность. А для чего R1-R4?
Планировал ЛАТР после вашего сообщения уже задумался ....
Схема предварительная, пока работаю над ней...
-
-
2 часа назад, Максим0 сказал:
По блоку питания посоветую:
Спасибо большое очень ценные данные.
Можете фото скинуть ВГВ-1000/100 вообще нет в инете данных.
-
1 час назад, Хоббит+ сказал:
какой должен быть процесс, чтобы химическая переработка была выгодной и минимально затратнойипо труду, времени, расходным материалам и пр..
Вот как наши предки это делали в древние времена...

-
1 минуту назад, Хоббит+ сказал:
Я рассматривал и написал подробности по растворению латуней в кислоте. Это альтернатива электролитическому процессу. Дальше можно сульфат цинка подвергнуть электролизу и получить болееичистый продукт, чем за одну стадию. И вернуть кислоту в цикл.
Да, это именно то о чем я и хотел пообщатся ... супер!
У вас есть уже какой-то опыт в этом?
Я видел в старой ветки вы активно участвовали по этому вопросу (давно было).
-
-
Всем большое спасибо, за советы и предложения!
Данных теперь намного больше, будем принимать решение.
Ещё раз спасибо ВСЕМ!
-
-
8 минут назад, Техно сказал:
Это не объём... так, баловство.
Но, можно поискать того, кому эти обрезки трубочек будут нужны как материал.И да, "Трубочки 3 - 5 (есть и те и те) см, толщина 0,34 mm , диаметр 0,5 mm " несколько не корректно. Что такое "толщина"? Диаметр чего?
толщина 0,34 mm - латуни Диаметр трубочки диаметр 0,5 mm (неверно я описался) диаметр 0,5 см - (верно)
-
-
-
-
6 минут назад, mirs сказал:
Имеет, если цинк постоянно выводится из зоны реакции.
Например испаряется в вакууме.
Но получается очень дорогой цинк. И медный купорос дорогой.
Спасибо это отличный ответ. Все просто - это ДОРОГО.
А вот так будет дешевле?
Cu3Zn2 + H2SO4 = CuSO4 + ZnSO4 + H2
-
-
К сожалению я так и не понял из всех ответов опубликованных в теме почему это не сработает: 2 ZnSO4 + Cu2Zn → 3 Zn + 2 CuSO4
Выше я давал ссылку на источник откуда формула.
Не думаю что её отфонаря кто-то создал....
Наверняка не все так просто как в ней написано и нужны будут определенные условия.
Если кто знает напишите ваши мысли что требуется что бы это сработало.
-
8 минут назад, бродяга_ сказал:
а вот лить что то типа заготовок для ключей выглядит привлекательно.
особенно если применять древнею технологию касетного литья.
суть в том что делается сразу много отливок. китайцы от капали и внедрили.
Круто спасибо изучаю тему:
Кристаллизатором кассетной конструкции
Очень интересно!!!
-
9 минут назад, бродяга_ сказал:
тогда яснее надо ставить задачу. что за сырье? стружка опилка чистота? количество / время...
Трубочки 3 - 5 (есть и те и те) см, толщина 0,34 mm , диаметр 0,5 mm
Количество чуть более 100 кг в 1 месяц.
Достаточно чистые, но есть не очень...
Время есть..
9 минут назад, бродяга_ сказал:мож лить будет выгоднее что то на рынок...
В первую очередь именно этот вариант и смотрели. (Взяли на заметку)
Вариант разделения на Cu и Zn выглядит пока более привлекательным.
-
4 минуты назад, бродяга_ сказал:
Спасибо, что хотите помочь, и предупредить.
Целесообразность данной идеи просчитывали не одну неделю.
Окончательные выводы делать пока очень рано, так как данных не достаточно.
На данном этапе важно понимать КАК это сделать, и что для этого требуется...
-
-
10 минут назад, бродяга_ сказал:
так реакция не пойдет.
CuSO4 + Zn ==> ZnSO4 + Cu а так пойдет.
Данные взял на сайте https://chemequations.com/ Химические Уравнения онлаин
Могут ошибатся? (или есть смысл проверить на практике, подскажите) и у меня исходный продукт (Латунь Cu2Zn)
Есть ещё такая формула:
Cu3Zn2 + H2SO4 = CuSO4 + ZnSO4 + H2
Но тут вообще хаос как из этого коктейля выделять что либо?
-
Создал новую тему, так как старая ветка закрыта и нет возможности публикаций.
Цель: выделить из латуни Cu и Zn (с минимальными потерями, а также получить максимально очищенные Cu и Zn).
На просторах интернет нашёл такое решение
2 ZnSO4 + Cu2Zn → 3 Zn + 2 CuSO4
Потрясающе, был несказанно рад и уже почти перешел к практике, но тут подвернулась другая формула, которая сбила меня с толку.
Помогите разобраться в этой теме.
Привожу пример, в котором и есть непонимание:
В результате растворения навески цинка в водном растворе сульфата меди (II) (CuSO4 + Zn = ?) происходит образование сульфата цинка и выделение меди в чистом виде (замещение).
Молекулярное уравнение реакции имеет вид:
CuSO4 + Zn ==> ZnSO4 + Cu
Вопрос: здесь 2 ZnSO4 + Cu2Zn → 3 Zn + 2 CuSO4
мы получили Zn и CuSO4, а во втором уравнении это исходные данные для реакции, почему тогда в первом случае реакция останавливается и не продолжается по сценарию второй формулы
CuSO4 + Zn ==> ZnSO4 + Cu
заранее большое спасибо
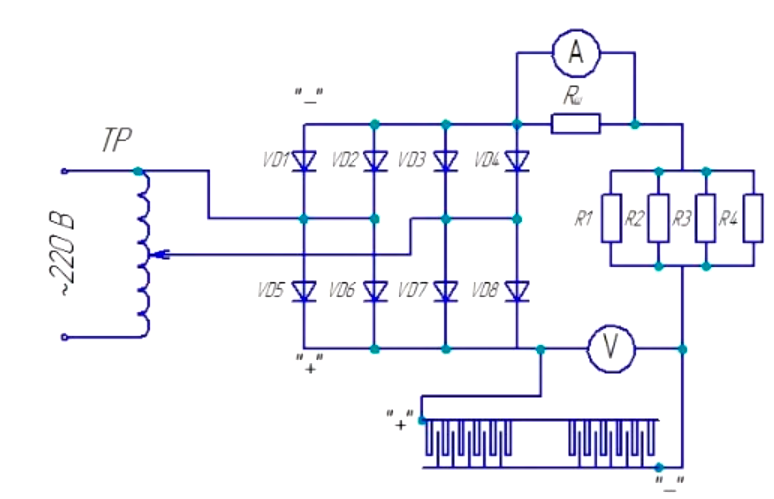

Как разложить латунь на Cu и Zn?
в Неорганическая химия
Опубликовано · Изменено пользователем alex-s
Предложили 10 штук диодов ДЧ151-100х-12 (говорит продавец не Б/У - [неверю]).
Цена с торгом 5$ штука - думаю брать.