
Анна Березовская
-
Постов
15 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Анна Березовская
-
-
Нужно получить нитрат свинца: в тетраоксид трисвинца добавить разбавленную азотную кислоту (Pb3O4+4HNO3→2Pb(NO3)2+PbO2+2H2O).
Эту смесь нужно довести до кипения в лабораторном стакане, поставив в него стеклянную палочку. После охлаждения раствор профильтровать и полученный фильтрат выпарить, поставив в ёмкость с фильтратом стеклянную палочку.
В связи с этим два вопроса: Нужно ли фильтрование для того, чтобы избавиться от PbO2 и зачем смесь нужно доводить до кипения обязательно со стеклянной палочкой (есть ли какая-то особенная причина для этого)?
-
Спасибо большое Вам ещё раз, теперь до меня дошло.
-
К сожалению, не указано, нужно вычислить теоретический выход продукта.
-
А можно вопрос?
Как вы к этому пришли? Для вычисления выхода продукта нужно продукт разделить на то вещество, которое в меньшем количестве. SnCl2*2H2O в меньшем количестве? и если посмотреть на последнее уравнение, то получается что SnCl2*2H2O и продукт SnO в равном количестве, как тогда вычислить выход продукта, если в условии даны SnCl2*2H2O (n=4,49 ммоль) и Na2CO3 (n=28,31 ммоль).
-
Спасибо Вам большое
-
Нужно вычислить выход продукта SnO. Уравнения реакций для получения этого продукта:
1) SnCl2*2H2O + 2HCl→Sn2++2H3O+4Cl-
2) Na2CO3 + H2O→2Na++HCO3-+OH-
3)Sn2+ + 2OH-→Sn(OH)2
4)Sn(OH)2→SnO+H2O
Общее уравнение реакции: SnCl2*2H2O + Na2CO3→SnO+2NaCl+CO2+ 2H2O; известна масса SnCl2*2H2O (m=1,012 г)
Какие исходные вещества нужны для вычисления выхода продукта? Нужно рассматривать SnCl2*2H2O как источник Sn2+ для SnO, а откуда взялся кислород, из воды?
-
Реакции получения Ag2HgI4:
3Ag+4HNO3→3AgNO3+2H2O+NO
Hg(NO3)2+2KI→HgI2+2KNO3
HgI2+2KI→K2HgI4
K2HgI4+2AgNO3→Ag2HgI4+2KNO3
Количество исходных веществ: n(Ag)=1,92 ммоль; n(KI)=3,71 ммоль; n(Hg(NO3)2*H2O)=0,943 ммоль
Количество продукта: n(Ag2HgI4) = 0,582 ммоль
Как рассчитать выход продукта реакции, какое исходное вещество здесь в меньшем количестве и как понять это по коэффициентам?
-
Хорошо, спасибо большое.
-
Так ведь KI здесь в большем количестве
-
Продукт = тетраиодомеркурат(II)серебра(I). Его получение показано уравнениями реакции. Нужно вычислить выход продукта реакции. Известное количество веществ: Продукт (Ag2HgI4) = 0,582 ммоль, серебро=1,92 ммоль, иодид калия=3,71 ммоль, моногидрат нитрата ртути (II) = 0,943 ммоль.
Мое решение:
выход продукта реакции=(количество продукта/количество моногидрата нитрата ртути(II))*100=(0,582 ммоль/0,943 ммоль)*100
Мой вопрос: почему это не правильно? При получения продукта моногидрат нитрата ртути(II) растворяется в воде. Значит ли это, что нужно испрользовать при вычислении не гидрат, а просто нитрат ртути(II)? В этом моя ошибка?
-
1 минуту назад, Paul_S сказал:
Знаете, именно из-за того, что там все-таки есть редокс-процесс, эта реакция гладко уравнивается с выделением хлора
4 C8H4O3 + 4 H4N2CO + CuH4O2Cl2 = C32H16N8Cu + 10 H2O + 4 CO2 + Cl2
Но в реальности там хлор, конечно, выделяться не будет, поскольку ему есть что окислить. Допустим, он окисляет мочевину
H4N2CO + H2O + 3 Cl2 = N2 + CO2 + 6 HCl
Складывая эти ур-ния, получим
12C8H4O3 + 13H4N2CO + 3CuH4O2Cl2 = 3C32H16N8Cu + 9H2O + 5CO2 + N2 + 6HCl
Последнее уравнение, думаю, наиболее вменяемое, без громадных коэффициентов.
Спасибо Вам большое еще раз! Теперь я гораздо лучше поняла этот эксперимент, потому что буквально вчера пришлось его выполнять, но а с теоретической частью как- то не сразу все получилось, запуталась в коэффициентах?
Огромное спасибо
-
26 минут назад, Paul_S сказал:
61 C8H4O3 + 75 H4N2CO + 15 CuH4O2Cl2 = 15 C32H16N8Cu + 122 H2O + 83 CO2 + 30 NH4Cl
или так
61 C8H4O3 + 60 H4N2CO + 15 CuH4O2Cl2 = 15 C32H16N8Cu + 137 H2O + 68 CO2 + 30 HCl
Разница в том, что в первом случае считаем, что HCl переводит мочевину в хлорид аммония и СО2.
Огромное Вам спасибо, вы меня спасли
-
12 минут назад, Paul_S сказал:
А с чего там хлор должен выделяться? Образующийся фталоцианин реагирует с хлоридом меди как кислота, хлорид-ион уходит в виде хлорида аммония. Это не редокс-процесс.
Спасибо большое за ответ, но проблема остается, потому что соотношение атомов водорода и кислорода исходных веществ и продуктов не правильное. Не могли бы вы мне помочь? Мое уравнение: 4C8H4O3 + 8CH4N2O + CuCl2*2H2O→C32H16CuN8 + 8CO2 + 4H2O + HCl + 8NH4Cl
-
Нужно составить уравнение химической реакции. Получение фталоцианина меди из мочевины, фталевого ангидрида, дигидрата хлорида меди(II) и гептамолибдата аммония в качестве катализатора. Не получается записать уравнение с нужными коэффициентами. В чем моя ошибка?(прикреплена фотография)
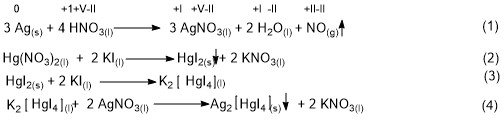
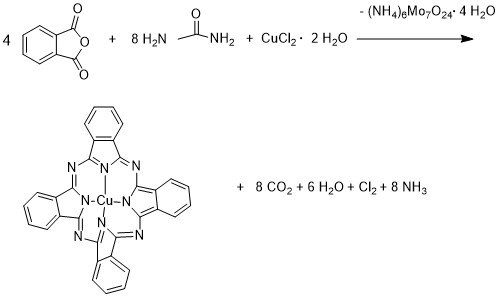
Получение нитрата свинца
в Решение заданий
Опубликовано
Ну приходится делать так, как сказал преподаватель?
Спасибо большое