
Ksenon_uni
-
Постов
4 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Ksenon_uni
-
-
Нейронная сеть была обучена определять количество серебряных микрокластеров по изображениям, полученным на электронном микроскопе. В качестве теста были представлены пять снимков. Предсказания нейронной сети отмечены в таблице в столбце NN, реальное количество серебряных кластеров представлено в таблице в столбце YY.
Коэффициент детерминации (R2R2) используется для определения качества обученной модели. Он рассчитывается по следующей формуле:
R2=1−RSSTSS,R2=1−RSSTSS,где TSSTSS – отклонение реальной величины от среднего значения:
TSS=∑n=15(Yn−Yсред)2,TSS=∑n=15(Yn−Yсред)2,и RSSRSS – вариация в наборе данных, которые не предсказаны моделью:
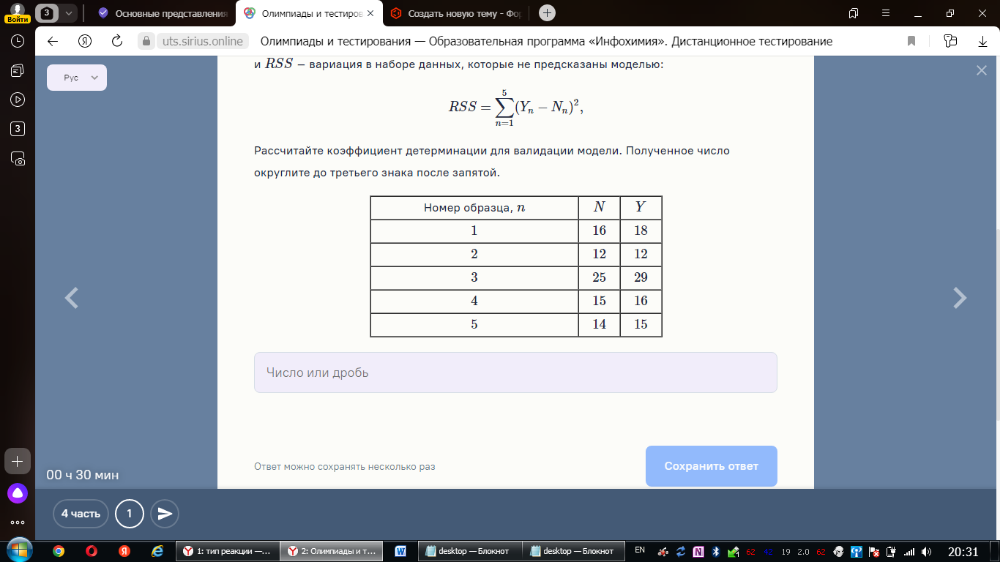
RSS=∑n=15(Yn−Nn)2,RSS=∑n=15(Yn−Nn)2,Рассчитайте коэффициент детерминации для валидации модели. Полученное число округлите до третьего знака после запятой.

-
Fe(NH4)3(C6H5O7)2
помогите в разложением под светом и получением этого вещества.
-
Добрый день, меня смущает то, что многие источники пишут,что степень окисления у кремния -4 в формуле силана.
Например
Хомченко Г. П., Цитович И.К. Неорганическая химия: Учебник для С/х ВУЗов (М.:Высш. школа, 1987), стр. 329: "В соединениях с кислородом (и другими неметаллами) он (кремний) проявляет степень окисления +2 и +4, а в соединениях с водородом -4."
или
Химия. Пособие-репетитор под ред. проф. В. Н. Чернышова и доц. А.С. Егорова (Феникс.:Ростов-на-Дону, 1996), стр. 418: "...кремний..степени окисления, наиболее характерными из которых являются следующие: -4 (силан, силициды металлов Mg2Si, Ca2Si и др.)..."хотелось бы узнать, какой источник более правдив.
НО
в огэ задание 10748
 , потому что водород в гидридах имеет степень окисления − 1
, потому что водород в гидридах имеет степень окисления − 1
хотелось бы узнать, какой источник более правдив и какого стоит придерживаться.
Заранее спасибо!
Спойлер
Навеска из 123 г сплава щелочных металлов сгорела в кислороде, при этом образовалось 156 г перокс...
в Решение заданий
Опубликовано
Навеска из 123 г сплава щелочных металлов сгорела в кислороде, при этом образовалось 156 г пероксида, 30 г надпероксида и 96 г нестехиометричного оксида. Какая масса кислорода (г) была израсходована?