
lanochka
-
Постов
32 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные lanochka
-
-
Проверьте пожалуйста мои рассуждения в задаче:
Рассчитайте число степеней свободы в системах.
Разбавленный водный раствор хлорида натрия в присутствии паров воды.
С=К-Ф+n
K=2( тк присутствуют ионы натрия и хлора)
ф=2 жидкая и парообразная фазы
n=2,тк система зависит от температуры и давления
С=2-2+2=2?????
-
подскажите пожалуйста,как решить задачу
в присутствии какого индикатора(ph=4,ph=5, ph=9, ph=11) можно титровать 0,1 м раствор уксусной кислоты раствором щелочи, ,чтобы погрешность титрования не превышала 0,1 %
-
Друзья, подскажите пожалуйста решение данной задачи: никак не могу найти формулу, для Пр при комплексообразовании(
рассчитать растворимость AgCSN в 0.01 м растворе аммиака , если для аммиачных комплексов серебра логарифмы ступенчатых констант образования равны lg K1=3.32 lgK2=3.92 ПрAgCSN = 1,1 * 10 -11
-
Здравствуйте. никак не могу понять как рассчитать растворимость соли, если пробавляться сильную кислоту, понимаю, что растворимость увеличивается по сравнению с водой.
Подскажите пожалуйста на примере такой задачи:
Вычислить растворимость CaF2 в 0.02 м растворе HCl.ПР( caf2)= 3,7 на 10 в -11, Кд кислоты = 7, 4на 10 в -4
-
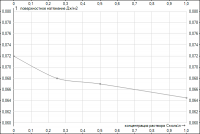
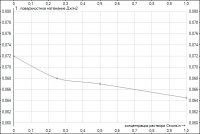
Здравствуйте,решая лабораторную работу столкнулаcь с проблемой определения равновесной концентрации ,которая требуется мне для нахождения адсорбцию ПАВ из раствора по уравнению: Г=С0-Ср/M*V я имею 2 графика изотермы натяжения до и после адсорбции,как мне ,пользуясь ими найти С0
прошу прощения вот график
почему то прикрепляется один и тот же файл((
вваепар
-
здравствуйте,подскажите пожалуйста следущее: на лаб. раб мы готовили 25% раствор бутанола,для этого мы брали 4,57 мл спирта,доводили до 100мл добавлением воды,плотность первоначального спирта была известнв,0,8 г\см3,мне требуется это процентное содержание перевести с молярную концентрацию,подскажите пожалуйста,каак это сделать?
тогда может быть можно как то рассчитать молярную концентрацию 50%раствора(плотность тоже не дана)
-
здравствуйте,подскажите пожалуйста следущее: на лаб. раб мы готовили 25% раствор бутанола,для этого мы брали 4,57 мл спирта,доводили до 100мл добавлением воды,плотность первоначального спирта была известнв,0,8 г\см3,мне требуется это процентное содержание перевести с молярную концентрацию,подскажите пожалуйста,каак это сделать?
-
.Уважаемые форумчане, подскажите пожалуйста решение задачек
1
Вычислите площадь, приходящуюся на молекулу стеариновой кислоты и толщину пленки, покрывающей поверхность воды, если известно, что 0,1*10-6 кг стеариновой кислоты покрывает поверхность воды, равную 5*10-2 м2. Молярная масса стеариновой кислоты равна 284 г/моль, плотность 0,85*103кг/м3.
2.
. Какой объем нитрата серебра с концентрацией 1*10-3 моль/л надо добавить к 10 мл раствора хлорида калия с концентрацией 2* 10-3 моль/л, чтобы получить золь с положительно заряженными частицами? Приведите схему строения мицеллы золя.
3. Гидрозоль иодида серебра получен путем смешения равных объемов 0,008 М раствора КI и 0,01 М раствора AgNO3. Какой из электролитов MgSO4 или K3[Fe(CN)6] будет иметь наибольший порог коагуляции для данного золя?
4 Установлено, что связь между характеристической вязкостью и молекулярной массой растворов полиизобутилена при 20°С описывается уравнение [η] = 3,6*10-4*М 0,64. Определите молекулярную массу фракции полиизобутилена в растворе с характеристической вязкостью [η] = 1,8 м3/кг.
-
здравствуйте,возник вопрос при решении задачи
. Константа химического равновесия реакции С2Н6(г)↔С2Н4(г) + Н2(г) при 1500К равна 40. Определите направление реакции, если в начале реакции парциальные давления компонентов имеют следующие значения : С2Н6=0,05 МПа, С2Н4=0,01 МПа, Н2= 0,02 МПа.
dG = -RTlnk
k =pH2pC2H2\pC2H6
подставим и найдём знак эн гиббса
Вопрос,для чего в задаче уже указана константа равновесия и почему она не сходится с полученной константой из парциальных давлений?
-
Тут проблема не в термодинамике (которая выражается в равновесных потенциалах), вся проблема в кинетике. Восстановление нитрата крайне затруднено кинетически. Если где-то в задачниках считают, что раньше нитрата будет восстанавливаться водород, то они правы с практической точки зрения. Нитрат раскочегарить на электрохимическое восстановление весьма сложно. Но реально. Некоторые ионы металов (имеющие разновалентные состояния, вроде вольфрама и ванадия) весьма успешно катализируют восстановление нитрата. Одним из таких катализаторов (но очень плохих) является железо. Железо всегда есть в растворах, в виде прмеси, только оно катализатор фиговый. Восстановление нитрата с ним проблематично.
Ну, не важно. Мы имеем нитрат с обычным уровнем (в воде типа дистиллированной) примесей солей железа. Не прокатит: нитрат не восстановится. Железо - слабый катализатор. А других вроде по условию не дано. Стало быть, мы должны считать нитрат в данных условиях электрохимически инертным. Пусть там термодинамика говорит, что нитрат в данных условиях может восстановиться. Все равно кинетика будет против.
ничего себе)))спасибо,а то давно мучила себя этим вопросом)
-
ну вот и я пр то же....короче странная реакция
А ещё вопросик можно.Если берём водный раствор нитрата калия,то на катоде могут протекать 3 процесса
К++1е=К Е=-2.95
2H2O+2e=H2+2Oh- Е=-0.82 рн=14
NO3- + H2O + 2e = NO2- + 2OH- Е=0,01 В этом случае потенциал последней реакции наибольший,почему тогда считается что идёт реакция восстановления водя?
-
-
-
-
???здравствуйте,подскажите плз как написать электролиз расплава КNO3 на инертных электродах?На сколько мне известно это вещество при нагревании разлагается....а в кр требуют именно электролиз расплава
-
здравствуйте,подскажите плз как написать электролиз расплава КNO3 на инертных электродах?На сколько мне известно это вещество при нагревании разлагается....а в кр требуют именно электролиз расплава
-
здравствуйте,подскажитепож-та решение задачи ::константа равновесия химической реакции протекающей в гальваническом элементе Pt\Fe3+Fe2+\\Sn4+Sn2+\Pt равна 10 в ст 23 найти E sn4+\Sn2+ еслиEFe3+\Fe2+=0,77 в
я нашла,что конст равновесия для овр вычисляется по форм lgK=(Eок- Евос)n\0,059,хотелось бы уточнить как будет выглядеть ОВР и кто окислитель и восстановитель?
-
-
-
да,все верно. Если олово в ряду напряжений левее какого либо из перечисленных катионов,то оно вытесняет этот катион.
а вытесняет,можно приравнять к тому что оно растворяется?
-
уважаемые, форумчане помогите пожалуйста с задачкой
В 1 М растворы HCL , Cu(NO3)2 , Pb(NO3)2, AL2 (SO4)3, KNO3, NiSO4 опускают по кусочку олова. В каком растворе олово будет растворяться
вообще 1м раствор можно считать концентрированным.Если олова в ряду напряжения активнее,то оно будет вытеснять металл из раствора,я права?
-
Здравствуйте подскажите пожалуйста
ИЭТ альбумина равна 4,8. Белок помещен в буферный раствор с рН=5,5. Как будут заряжены частицы альбумина
Я понимаю,что в кислой среде, когда в результате избытка водородных ио-
нов подавлена ионизация карбоксильных групп, молекула белка
ведет себя как основание, приобретая положительный заряд,а как это записать?
-
ну учитывая то,что в графите сп2 гибридизация,а в карбине сп,то получается,что в карбине больше связей,хотя фиг знает ведь число тройных и двойных связей может уравниваться)),если я так рассуждаю,то получается что карбин более устойчив,а зачем нам даны теплоты сгорания?
-
ребята,здравствуйте,помргите пожалуйста с задачей
Теплота сгорания карбина 356,1кДж/моль, а для графита теплота сгорания 396,3кДж/моль. Сравните термическую устойчивость графита и карбина
мне понятно,что чем меньше теплота образования веществ,тем оно более устойчиво,поэтому я на этот вопрос ответила,через теплоту образования углекислого газа(она же равна тепл сгорания веществ) и типа там где меньше,то вещество и устойчивей,но мне не зачли ответ,подскажите пожалуйста как надо на него ответить
гальванический элемент
в Решение заданий
Опубликовано · Изменено пользователем lanochka
Ребята,помогите пожалуйста разобраться в задачке E5:дан гальванический элемент,под букв а приведены все реакции на электродах(не понятно почему их 3); под б написано уравнение реакции токообразующей(вообще не пронятно от куда что берётся(((