
bumblebee
-
Постов
89 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные bumblebee
-
-
я решила вот эту задачу (но):
В каком объеме воды следует растворить 2 г оксида серы (VI), чтобы получить раствор серной кислоты с массовой долей 1%?
НО у меня объём воды получился 88038 мл!!!!!!! такое может быть???!!?подскажите пожалуйста?
-
-
-
помогите разобраться с задачей,пожалуйста.
при обработке некоторого количества одноатомного спирта неизвестного состава натрием выделилось 2,24 л газа(н.у) а при взаимодействии образовавшегося органического вещества с избытком бромистого алила было получено 20,4 г симметричного кислородосодержащего соединения. какая мсасса спирта была взята в реакцию, и каково его строение?
2CxHyO+2Na=2CxHy-1ONa + H2
N(H2)=2.24/22.4=0,1 моль
а дальше я не знаю что такое бромистый алкил. как его можно выразить через формулу неизвестного спирта, предполагаю, что в алкиле будет столько же атомов углерода как в спирте( ведь кислородосодержащие соединение симметрично). я правильно рассуждаю? помогите с решением?
-
Ацетат-ион связывает находящиеся в растворе ионы H+ в молекулы слабодиссоциирующей уксусной кислоты:
CH3COO- + H+ --> CH3COOH
Вследствие уменьшения концентрации ионов H+ реакция растворения цинка замедляется:
Zn + 2H+ --> Zn2+ + H2↑
спасибо!
-
Вот задача на которую я пытаюсь найти ответ:как известно цинк активно реагирует с раствором серной кислоты. однако придобавлении к этому раствору ацетата натрия выделение пузырьков газа резко замедляется. как можно объяснить это явление?
я правильно предполагаю, что ацетат натрия даёт гидролиз в данном растворе, образуя слабый электролит-уксусную кислоту, на образование катиона которой и тратиться водород при реакции цинка с H2SO4???
-
помогите решить, пожалуйста!
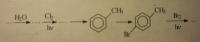
В результате реакции 27.6 г толуола с бромом в присутствии бромида алюминия выделился газ в количестве, достаточном для взаимодействия с 100 мл 0.5 M раствора перманганата калия. Установите качественный и количественный состав органических соединений, полученных в результате бромирования толуола.
-
-
Подскажите, какие вещества должны быть на месте первого и второго многоточий?

-
HC≡C-C≡C-C≡CH - триацетилен
CH2=CH-CH=CH-CH=CH2 - гексатриен-1,3,5
спасибо))))))))))))
-
Подскажите, кто знает как выглядят формулы триацетилен и гексатриен-1,3,5?
-
-
Решение очень простое.
Запишите реакцию толуола с перманганатом и определите, сколько MnO2 образуется в реакции с 18,4 г. толуола.
А можете сказать, что входит в органический слой данной задачи? мне стало непонятен именно этот момент. при окислении образуется органическая соль, по массе которая больше толуола, израсходованного на её образование,---> С6H5-CH3+ 2KMnO4=C6H5-COOK+2MnO2+KOH+H20 ну тоесть как же масса могла уменьшиться???!
-
Помогите,пожалуйста решить задачу!
Смесь бензола и его ближайшего гомолога обработали горячим нейтральным раствором перманганата калия. Органический слой и осадок отделили от раствора. Масса органического слоя уменьшилась по сравнению с исходной смесью на 18,4г. Чему равна масса осадка??
-
Из уравнения C2H2 + H2O = C2H4O следует, что n(C2H2) = n(C2H4O) = 1; n - число молей.
1 моль (22,4 л) C2H2 --> 1 моль (44 г) C2H4O
По моему мы не можем брать 22,4л/моль. нет нормальных условий..
-
Ацетальдегид - легко кипящая жидкость (20,2°С).
22,4 л С2Н2 - 44 г С2Н4О
11,8 л С2Н2 - х г С2Н4О ===> х = 23,2
m(С2Н4О) = 23,2*(100-5)/100 = ...
Можно узнать почему вы решили что
?22,4 л С2Н2 - 44 г С2Н4О -
Помогите с задачей, пожалуйста....
Какова масса (в г) образовавшегося ацетальдегида в реакции гидратации ацетилена объёмом 11,8 л содержащего 5% примесей.
Моя часть решения:
C2H2+H2O=C2H4O. понятно что объём ацетальдегида равен тоже 11,8, но как же найти массу, если нет данных для уравнения Менделеева Клайперона, и даже не указаны н.у?
-
-
Смесь трёх солей натрия, в которой количество вещества гидрофосфат- ионов в 2 раза больше количества вещества фосфат-ионов, но в 3 раза меньше количества вещества дигидрофосфат- ионов, растворили в воде. При обработке раствора избытком разбавленного раствора хлорида бария образовалось 50 г осадка. Вычислите суммарную массу исходных солей?
Помогите решить задачу,пожалуйста! особенную трудность вызывает уравнение реакций гидролиза:(
-
У вас кислоты очень мало, по сравнению с раствором карбоната натрия, поэтому вторая реакция вам не понадобится
хм...тогда какие 3 вещества будут в растворе?( в ответе именно 3 указано)
хм...тогда какие 3 вещества будут в растворе?( в ответе именно 3 указано)
ой пардон! всё) поняла
-
Na2CO3 + HCl = NaHCO3 + NaCl
NaHCO3 + HCl = NaCl + CO2↑ + H2O
спасибо огромное!
-
какие здесь будут уравнения реакций? не подскажите?
К 10,0 мл 5,00%-ного раствора карбоната натрия (пл.1,05 г/мл) добавили по каплям 1,00 мл 5,00%-ного раствора хлороводорода (пл. 1,03 г/мл). Вычислите массовые доли веществ в полученном растворе.
-
Да ^_^ , всё логично, поэтому мне понятно, спасибо за помощь! вот только можно выразить в процентах концентрацию водородов?
Будем пытаться "запустить" собственную "думалку". Итак, кислота одноосновная, т.е. каждая молекула ее при диссоциации может бать один ион водорода. Но - кислота она слабая, поэтому только часть молекул таким образом будет диссоциировать, а какая часть - это показывает степень диссоциации. Поэтому умножаете исходную концентрацию кислоты на число протонов, образующихся при диссоциации каждой молекулы и на степень диссоциации. Три числа сами умножите?..
ЗЫ: коллега FilIgor, даже методика объяснения решения задач у нас похожая...

да, 3 числа умножу! спасибо за объяснение!!!!

-
Если степень диссоциации муравьиной кислоты в растворе с концентрацией 0,1 моль/л равна 0,03, то концентрация ионов водорода ...
Варианты ответа:1. 0,4 моль/л. 2. 0,1 моль/л. 3. 0,012 моль/л. 4. 0,003 моль/л. 5. 0,3 %. 6. 3 %?
Как решать подобного рода задачи? Помогите,пожауйста!
Нахождение состава раствора через массовую долю
в Решение заданий
Опубликовано
SO3+H2O-->H2SO4 взяла всё по X моль,получила
0,01=98х/2+18x
x=4891моль
вот что у меня здесь неправильно??подскажите