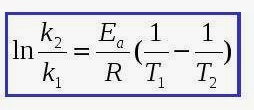lika89
Пользователи-
Постов
27 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент lika89
-
Определить константу скорости (k2), если k1=0,69 (моль/л*мин), энергия активации 150 кДж/моль, Т1=473 К, Т2=493 К. Я так понимаю, что нужно вычислить по уравнению Аррениуса: У меня не получается преобразовать уравнение и вычислить. Помогите пожалуйста!
-
2СН3OH = CH3OСH3+ H2O 1) напишите выражение для констант химического равновесия, выраженных через равновес- ные концентрации и парциальные давления 2) приведите факторы, влияющие на положение равновесия 3) на основании принципа Ле - Шателье установите влияние изменения температуры, давле- ния, концентрации сырья и продуктов на выход продукта 4) определите, при каких условиях необходимо проводить реакцию для получения продуктов с высоким выходом.
-
Для реакции с начальными концентрациями реагирующих веществ, равными С, протекающей при температуре t1, известна константа скорости реакции k1 и энергия активации Еа. Вычислить: 1) начальную скорость реакции 2) скорость реакции в момент времени, к которому концентрация вещества А (вещество выделено жирным шрифтом) 3) время от начала реакции, за которое концентрация вещества А уменьшится на Р% 4) концентрации всех веществ к этому моменту времени 5) константу скорости реакции при температуре t2 6) температурный коэффициент скорости реакции. № Химическая реакция С, моль/л t1, °C t2, °C k1, л/(моль·мин) Р % Е, кДж/моль 23 2СН3OH = CH3OСH3+ H2O 0,2 200 220 0,69 40 150
-
спасибо!
-
Для приведенной реакции: 1) вычислить стандартный тепловой эффект реакции при постоянном давлении 2) привести термодинамическую характеристику реакции 3) вычислить теплоту реакции получения продукта массой m (продукт выделен жирным шрифтом) при постоянном давлении 4) вычислить стандартный тепловой эффект реакции при постоянном объеме. СН3OH = CH2O + H2 m=1,5 кг
-
Я честно не понимаю, я уже с 13:30 до сих пор пытаюсь разобраться. Даже выражения не напишу - не соображу
-
Не понимаю потом что, кучу примеров пересмотрела, вот и не знаю уже что куда откуда
-
Простите за ошибки) ΔG0 =-92,3-1000*186,6= -186508? В общем не разобралась ΔH0=-92,3 S0=186,6 , такие данные используются?
-
просто у меня цыфры получаюся в сотнях тысечах...
-
А можно с цифрами, формулы я нашла, а вот с вычислением плохо...
-
Я понимаю, что на энергию Гиббса много примеров, есть и в примерах решения. Но из всех заданий по физ химии мне именно это не понять. Найти ΔG0, Кр, Кс в реакции 2HCl=Cl2+H2, при Температуре 1000 К, Кр сравните с Экспериментальными данными lg Кр -5,258. Не понимаю просто
-
что делать с этой задачей?
-
а ее ввиде лаборторки чисто методом описывать тогда? спаибо без вас бы мы не справились сейчас хоть в чем то разобралась нет я и правда ошиблась, там 300
-
Это условие писал человек, находящийся в расстроенных чувствах. Оно абсолютно алогично. Если уже задана концентрация (0,1 н.), то зачем остальные данные? Вдобавок, растворением 1, 68 г. гидроксида калия в 30 мл воды не получится 0,1 н. раствор. Это чушь. Или Вы неверно переписали. да, тут не 30, а 300
-
а затем? Спасибо за подсказки)
-
Условия не я придумывала. Мне безупречноть не к чему. мне нужен просто зачет
-
это точная формулировка задачи, котоая была задана нам на заочном отделении
-
Как так? дайте хоть подзказку в каком направлении думать