-
Постов
464 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные ОргХим.
-
-
а) C2H5OH + HBr ==+ Mg==> C2H5MgBr + H2O
2CH3OH + O2 ==> 2CH2O + 2H2O
CH2O + C2H5MgBr ==> C3H7OMgBr
C3H7OMgBr + H2O ==> C3H7OH + Mg(OH)Br
б) С2Н5ОН ==кат.(ZnO|CeO2), t~450*С==> CH3-C(O)-CH3
CH3C(O)CH3 + H2 ==кат.(Ni|Cu), t~210*C==> CH3CH(OH)CH3
В водном растворе кислотность спиртов снижается с увеличением разветвлённости углеводородной цепи.
-
 1
1
-
-
Есть
..хотя крайне взрывчатый (N5+1)P(N3-1)6 = PN23...
http://www.nanometer.ru/2011/11/21/obshaa_i_neorganicheskaa_himia_264531.html
-
Задачи простые.
Прошу помощьььи в решении нескольких задач;
Закончить уравнения реакций:
1) CH3-CH=CH2+HBr
2) CH3-CH=CH2+H2O
3) CH3-CH=CH2+Br2
4) CH3-CH2-CHOH t/H+
5) CH3-CH2-CH3 t/kam
6) CH2=CH-CH3+O2
1) - гидрогалогенирование (по Марковникову).
2) - гидратация, получится СН3-СН(ОН)-СН3
3) - галогенирование алкенов
4) - гидрирование, получится С3Н7ОН
5) - вообще можно привести массу реакций, например дегидрирование: СН3-СН2-СН3 =кат./темп.=> СH3-CH=CH2 + H2
6) - реакция горения(полного окисления)
1) СH3-CH=CH-CH2-CH3 и СН2=CH-CH2-CH2-CH3 и др.
2) СH3-CH=СН-СН2-СН2-СН3 и СH3-CH2-CH=CH-CH2-CH3 и др.
3) СН2=СН-СН2-СН3 и СН3-СН=СН-СН3
1) M=21*2=42 (2-средняя молекулярная масса водорода)
42- это углерод. (42/Mr(С )=42/14=3 - количество атомов углерода)42 - (85,7% * 42) = 6 - количество атомов водорода
формула: C3H6Точно так же остальные (средняя молекулярная масса по воздуху равна 29)
-
а при кипячении кислота становится концентрированной как например из электролита получают концентрированную серную кислоту.При температуре выше 213 °C ортофосфорная кислота превращается в пирофосфорную кислоту H4P2O7 вода испарится кислота станет конц.
В задаче сказано "кипячение". Думается под этим словом не имелось ввиду выпаривание. Если бы было выпаривание, тогда бы написали "выпаривание".
-
Во-первых, нужно составить уравнение: P2O5 + 3H2O ==> 2H3PO4
Дальше n(P2O5) = m/Mr = 2,84/142 = 0,02 моль
Согласно уравнению реакции выше n(H3PO4)=2n(P2O5)=0,04 моль
Найдём общее количество n(H3PO4) в получившемся растворе: n + m/Mr = 0,04 + (60*0,18)/98 = 0,15 моль
3NaOH + H3PO4 ==> Na3PO4 + 3H2O
n(NaOH) =3n(H3PO4) = 0,45 моль
Так как n(H3PO4)=n(Na3PO4) то: m(Na3PO4)=0,15*164=24,6 г.
как я её решил описываю ход решения на счёт правильности решенной задачи не уверен и поэтому обращаюсь за помощьььььььью
mН3РО4=10,8г
3Н2О+Р2О5=2Н3РО4
nР2О5=0,02моль
mН3РО4=3,92г масса образовавшейся кислоты
mН3РО4=14.72г общая масса кислоты
nН3РО4=0,15моль
раствор прокипятили
2Н3РО4=Н4Р2О7+Н2О
nН4Р2О7=0.075моль
nNaOH=0,75моль
Н4Р2О7+4NaOH=Na4Р2О7+4Н2О
nNa4Р2О7=0,075моль
mNa4Р2О7=16,35г
при нагревании фосфорная переходит в дифосфорную
Такая реакция возможна только с Концентрированной кислотой
-
А почему нет:? Уравнивается нормально. Тем более амфотерный гидроксид.
Ну вы сами посмотрите. Никогда, при такой реакции, при такой кислой среде, не получится гидроксид.
-
Это точно? А что в первых трех уравнениях? Коэффициенты не так стоят, а сами вещества те образуются?
Да
...
А почему Al2(SO4)3, а не гидроксид алюминия (|||)
А с чего вдруг гидроксиду там образовываться?
-
3)1)4)2)
- В вашем случае реакционная способность зависит от степени поляризации С=О. У кетонов (ацетона) наименьшая поляризация(в вашем случае).
- У альдегидов (ацетальдегида и формальдегида) - чуть побольше. С увеличением числа атомов углерода у альдегидов, их реакционоспособность уменьшается, поэтому ацетальдегид будет мение реакционоспособен, чем формальдегид.
- Хлораль, за счёт трихлорметильной группы, является наиболее реакционоспособной.
-
 1
1
-
-
Теоретически можно, но не в домашних условиях.
Можно из жирных кислот арахисового масла попробовать, но нужна лаборатория.
-
на первой картинке 1,2-дигидро-1,5-диметил-2-этил-3Н-пиразол-3-oн
(1,2-dihydro- 1,5-dimethyl- 2-ethyl- 3H-pyrazol-3-one)
на второй - Стрептоцид (сульфаниламид)
-
В литературе по органическому синтезу встретилась такая фраза: "Лигноцериновая кислота СНз ( СН2) 22СООН находится в арахидном масле, в гниющей дубовой древесине, в буковом дегте и др. Кристаллизуется из горячего спирта в виде шелковистых хлопьев." Т.е. это значит, что её можно кристализовать из горячего спирта? Если да, то сразу возникает вопрос из какого именно?
Что тут может быть непонятного?
Сначало растворили лигноцериновую кислоту в горячем спирте; при охлаждении выпали шелковистые хлопья лигноцериновой кислоты, т.е. кристаллизовались из спирта.
кристаллизация это не сам процесс синтеза нового вещества.
-
Спасибо Дмитрий, не знаком с этими трудами, будет свободное время просмотрю, но вторая часть этого видео что я скинул еще интересней, на мой взгляд, мы же обсуждали добычу энергии из пространства, которая не вредит экологии, а так же безгранична:
Это тоже одна из теорий, на мой взгляд крайне маловероятная, хотя и заманчивая.
-
Задача очень простая.
Мr(металла) - молярная масса металла. Можно составить пропорцию:
3,31г = Мr(металла) + Мr(NO3).
------ -------------------------------
2,78г = Mr(металла) + Mr(Cl).
Отсюда: 3,31 * (Мr(металла) + 35,5) = 2,78 * (Мr(металла) + 62)
Мr(металла) = 103,5
-
 1
1
-
-
Верхний - бензокаин
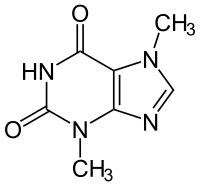
Нижний - теофиллин
P.S. А вообще у каждого химика есть хим проги, я пользуюсь ACD. В данном случае, что делал я: нарисовал, перевел в название и нашел по названию на ChemSpider, затем и на вики нашлось.
P.S.S. Как я понял, это все психоактивные вещества, с какой целью интересуетесь? ))
Структурные форулы сравни. 2 - это НЕ теофиллин , а Теобромин - http://ru.wikipedia.org/wiki/Теобромин
-
.......
2. как выходя з 1,6-димбромгексану можно получить цыклогексанон?
2. Сначало прибавляем металлический натрий, получается циклогексан. Затем окисление кислородом при 150°С, давлении 1,2-1,6 мПа с катализатором.
-
 реакция написана то правильно, а вот в написании самого вещества запутались.
реакция написана то правильно, а вот в написании самого вещества запутались.Во-первых, никогда не пишите вот так ( (СH3)2-CH-)
Из-за этого пошла ошибка: (после изомеризации) вместо (СH3)2-CH- вы написали (СН3)2-СН2-
Будте внимательны!
-
Фуран относят к ароматическим, так как он представляет собой сопряженую циклическую систему, в состав которой входит 6p электронов – 4 электрона диеновой системы – и пара электронов гетероатома.
Понятие "ароматичность" - http://ru.wikipedia.org/wiki/Ароматичность
Гидрирование: C4H4O + 2Н2 ==Ni(кат.),120*C==> C4H8O (тетрагидрофуран).
С4Н4О + Н2 ==кат.==> С4Н6О (дигидрофуран). t=~100*C.
-
CH3COOC2H5 + H2O + H2SO4 =/= (гидролиза нет, кислая среда)
CH3COOC2H5 + H2O + NaOH ==> CH3COONa + C2H5OH
-
а) при гидролизе вообще не нужны электроды.
б) в расплавах гидролиза нет!
Гидролиз - http://ru.wikipedia.org/wiki/Гидролиз
Описаные вами задания к гидролизу не имеют никакого отношения. Это немного другой процесс.
-
-
По-моему, 6,6-диметилгептандиол-2,5, так как нумеровать цепь следует с того края, к которму ближе функциональная группа ОН. Таким образом, основой структуры является гептандиол-2,5 (в этом легко убедиться, если заменить оба метила на водороды и дать название получившемуся диолу).
Да, конечно же вы правы, правильно будет 6,6-диметилгептандиол-2,5.
-
Какой помощи? Я
так понял вам структурная формула нужна.
СH3
|
CH2
|
CH-CH3
|
CH-CH3
|
CH-CH2-CH(-CH3)-CH(-CH3)-CH3
|
CH2
|
CH-C2H5
|
CH2
|
CH2
|
CH3
-
1.сера - оксид серы(4) - сернистая кислота - сульфит натрия - сульфит серебра
1) S + O2 ==> SO2
2) SO2 + H2O ==> H2SO3
3) H2SO3 + 2NaOH ==> Na2SO3 + 2H2O
4) Na2SO3 + 2AgNO3 ==> Ag2SO3(осадок) + 2NaNO3
2. гидроксид меди (2) - сульфат меди (2) - медь - оксид меди (2) - нитрат меди(2)
1) Cu(OH)2 + H2SO4 ==> CuSO4 + 2H2O
2) 3CuSO4 + 2Al ==> 3Cu + Al2(SO4)3
3) 2Сu + O2 ==> 2CuO
4) CuO + 2HNO3 ==> Cu(NO3)2 + H2O


где можно взять рефрактометрические таблицы
в Решение заданий
Опубликовано
http://yojik21.com/publ/3-1-0-71