Поиск
Показаны результаты для тегов 'атмосферные процессы'.
Найдено 1 результат
-
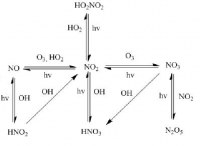
Предмет физико-химические процессы в техносфере, задание дали на всю группу, но никто ничего не понимает, хоть и изучали химию 2 семестра. Прошу помощьи, подсказок, советов по отдельным заданиям. Выполните задание: 1. Пользуясь схемой, составьте уравнения реакций, происходящих в атмосфере вблизи источника выбросов оксидов азота (например, котельной) в солнечную безветренную погоду. В атмосфере постоянно присутствуют: озон, радикалы ОН· и НО2. 2. Составьте схемы реакций превращения первичных продуктов: NO, N2O3, N2O5, HNO2, HO2NO2, NO3(реакции, которые идут при λ < 290 нм отбрасываются). 3. Пользуясь справочными данными определите константы скоростей реакций при соответствующих температурах (ориентируясь на температурный градиент атмосферы). 4. Из основных циклов превращений поллютантов выберите самые быстрые реакции, отвечающие за трансформацию основной массы атмосферной примеси. 5. Сделайте вывод, ответив на вопрос: какие продукты цикла оксида азота являются основными компонентами смога? Общая схема химических превращений оксидов азота в атмосфере: (рис в прил) Решите расчётные задачи: 1 Сравните скорости выведения из атмосферы молекул метана при их взаимодействии с гидроксидным радикалом в приземном слое и на высоте верхней границы стандартной тропосферы. Концентрация метана на этих высотах равна 1,7 млн-1. Энергия активации и предэкспоненциальный множитель для реакции взаимодействия метана с ОН-радикалом равны 14,1 кДж/моль и 2,3 см3 • с-1 соответственно. Концентрации гидроксидных радикалов на этих высотах принять равными: [ОН]1 = 5 • 105 см-3, [ОН]2 = 2 • 106 см-3. 2. Определите, каким будет соотношение скоростей процессов газофазного и жидкофазного окисления SО2, если принять, что основной вклад вносят следующие реакции: SО2{г) + ОН(г) ? HSO3(г) (1) SО2{р-р) + Н2О2(р-р) ? Н2SO4(р-р) (2) Константы скоростей реакций окисления: k1 = 9∙10-13 см3 ∙ с-1; k2 = 1 ∙ 103 л ∙ моль-1 ∙ с-1. Концентрации примесей в газовой фазе составляют: [ОН] = 5 ∙106 см-3, [sO2] = 10-4 % (об.); [Н2О2] = 10-7 % (об.). Расчеты провести для атмосферного воздуха, имеющего температуру 25о С и содержащего 0,00001 г свободной воды в каждом литре воздуха, Считать, что при растворении в воде концентрация SО2 в газовой фазе не меняется. Газы считать идеальными и подчиняющимися закону Генри. Давление принять равным 1 атм. 3. Какое было бы отношение концентраций NO и NO2 в равновесной системе на высоте 11 км, если их взаимную трансформацию можно было бы ограничить следующими реакциями: М + NO + О = NO2 + М* , если М — молекулы кислорода NO2 + О = + NO + О2? Константы скорости реакций на этой высоте равны соответственно: k1 = 8 ∙ 10-32 см6 ∙ с-1,; k2 = 1∙10-12 см3∙с-1.
-
- атмосферные процессы
- органика
- (и ещё 3 )