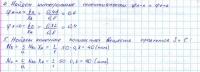Поиск
Показаны результаты для тегов 'охт'.
Найдено 11 результатов
-
Этилен получают путем пиролиза пропана: C3H8=C2H4+CH4 В продуктах реакции содержится 0,5%об пропана. Рассчитать степень превращения пропана, выход этилена и расходный коэффициент по сырью кг и м^3. Рассвет провести на 2т этилена.
-
-
- охт
- охт мат.баланс
-
(и ещё 1 )
C тегом:
-
Саму задачу и ее решение Вы можете видеть внизу на фото. Смущает последнее действие, а именно, количество вещества получившихся продуктов S и C - по 40 моль. Наверное, количества получившихся веществ в реакции должно быть равно количеству вещества исходного реагента, у меня так не получается. Может такое быть? Как решить по-другому, чтобы было правильно? Может ошибка где - то в предыдущих действиях? Спасибо за внимание к моему вопросу и Вашим ответам!
-
-
- охт
- химические реакторы
- (и ещё 1 )
-
помогите решить!!! При термоокислительном крекинге метана (с целью получения ацетилена) смесь газов имеет состав [% (об.)]: С2Н2 -- 8,5; Н2--57,0; СО -- 25,3; С02 --3,7; С2Н4--0,5; СН4 -- 4,0; Аг -- 1,0. Определить количество метана, которое нужно подвергнуть крекингу, чтобы из отходов крекинга после отделения ацетилена получить 1 т метанола: СО + 2Н2 = СН3ОН. По практическим данным из 1 т исходного метана получается после выделения С2Н2 1160 кг смеси газов.
- 2 ответа
-
- мб
- материальный баланс
-
(и ещё 2 )
C тегом:
-
Рассчитать мат-й баланс в процессе горения газовой смеси состава: объемная доля Н2=50%, объемная доля СН4=50%. На горение подается сухой воздух при температуре 45С и Р=90кПа с относительной влажностью 0,6. поток горючего газа Wгг=5000 м3/час. Реакции горения идет со степенью превращения : Н2=0,75, СН4=0,9. Смесь газа и кислорода стехиометрическая. Определить состав продуктов горения во всех единицах измерения, полагая что Z=1. 2Н2+О2=2Н2О СН4+О0=2Н2О+СО
- 2 ответа
-
- ОХТ
- материальный баланс
-
(и ещё 1 )
C тегом:
-
Критические тепловые явления в гетерогенном процессе
Igor57 опубликовал тема в Химическая технология
Господа, нужно расписать ответ на поставленную тему:"Критические тепловые явления в гетерогенном процессе: неодносзначность стационарных режимов;обратная связь." и "Критические тепловые явления в гетерогенном процессе: гистерезис стационарных режимов." Подскажите что написать можно, или литературу в которой можно прочесть об этом. Заранее благодарен. -
1. В реакторе идеального вытеснения проводят реакцию А+В ----> R+S Определите производительность по продукту R, если СА.О = С В.О. = 2кмоль/м3, объем реактора V=1,4м3 , объемный расход υ = 28м3/ч, константа скорости k=18 м3 /кмоль*ч/
-
Будьте добры решите кто разбирается , уже трижды сходил к преподавателю с различными версиями решения , листочек выглядит так словно прошел все круги ада :О З.ы. могу выложить неверный вариант решения и указать , где единственная верная мысль , а могу просто сформулировать : скорость хим.реакций будет постепенно уменьшать при увелечение степени превращения
-
Этилен получают путем пиролиза пропана С3H8 ----> C2H4+ CH4 В продуктах реакции содержится 0,6 объемных % пропана. Рассчитать степень превращения пропана, выход этилена и расходный коэффициент по сырью в кг и м3. Расчет произвести на 1 тонну этилена. Не могу сдвинуться с мертвой точки. Помогите кто чем может.
-
Уважаемые форумчане! Помогите, пожалуйста, с решением задачки по дисциплине "общая химическая технология". Рассчитать зависимость содержания кислорода в газах обжига от концентрации SO2 при воздушном дутье: а) для обжига колчедана FeS2 б) для обжига серы; в) для обжига сернистого цинка ZnS.