sergium
Участник-
Постов
229 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Весь контент sergium
-
Марганец от 2+ до +7 азотная кислота вряд ли окислит. Нужны более сильные окислители. Если нетрудно, скиньте источник Так правдоподобнее MnSO4 + PbO2 + HNO3 → HMnO4 + Pb(NO3)2 + PbSO4 + H2O
-
1) Получить можно по схеме R-MgBr + СО2 → R-COO-MgBr → R-COOH + Mg(OH)Br Это получение с помощью реактива Гриньяра 2) Наберите в гугле сульфохлорирование карбоновых кислот, получение амидов карбоновых кислот 3) Формулы можно найти опять же. Например тут http://www.chemistry.ssu.samara.ru/chem4/pic/o4602.gif Писать довольно много. Просто поищите по этим рекомендациям в инете, тут стандартные реакции и вопросы. А потом покажите проделанную работу
-
Это ОВР. Обычно в программах школ не составляют правую часть в данном типе реакций, а только делают баланс. По-крайней мере в украинских. Это детальнее проходят в институтах на первых курсах. Тут свойства перманганата калия. В зависимости от среды, он восстанавливается в разные продукты. Почитайте тут http://himik.pro/okislitelno-vosstanovitelnyie-reaktsii-2/vliyanie-faktorov-na-ovr/reaktsii-permanganat-kaliya
-
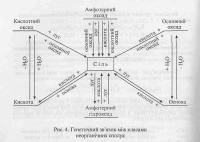
Вот генетическая схема в общем виде, правда на украинском, т.к. понятнее не нашел. В правой части хим. реакции должно обязательно образовываться либо соль, либо кислота, либо основание, иногда и оксид (при реакции разложения) Т.о. даже если вы не знаете, что в правой части, то можно составить её как пазл по имеющимся частям в левой части. В общем-то этих знаний вполне достаточно для школы.
-
Как объянить, почему ртуть реагирует с серой легче, чем цинк, хотя активность первой меньше?
-
Т.е. типа такого H[Au(NO3)4] + N2O5 --> Au(NO3)3 + HNO3*N2O5 Как понять связывает азотную кислоту? В виде чего? Что-то первый раз слышу. Обычно N2O5 связывает воду
-
Я делал по книге Третьякова, как предложил aversun. Просто с N2O4 надо выделить сначала чистое золото из комплекса "при взаимодействии соединения (H3O)[Au(NO3)4] с азотным ангидридом и последующем нагревании в вакууме при 80 °С возгоняются золотисто-желтые кристаллы нитрата Au(NO3)3." Вот я эту реакцию и написал
-
Думаю, как вариант тогда может так сойти Na[Au(OH)4] + HNO3 (t)--> NaNO3 + (H[Au(NO3)4] + H2O) H[Au(NO3)4] + H2O + N2O5 --> Au(NO3)3 + 3HNO3
-
тогда собственно в этом и вопрос. Как осуществить такое превращение Na[Au(OH)4] --> Au(NO3)3 может взять другой растворитель...
-
Mo+NaNO3+NaOH Делаете слои сендвичем и прокаливаете
-
Стоит ли упоминать про сулему
-
Просто я подумал, что соль Au(NO3)3 не может существовать в водном растворе. Честно говоря, не видел нигде про неё упоминания. Только в википедии
-
Встретилось задание: надо получить нитрат золота из комплекса. Реакция впрочем-то стандартная Na[Au(OH)4] + HNO3 --> NaNO3 + Au(NO3)3 + H2O Но известно, что Au(OH)3 + 4HNO3 = H[Au(NO3)4] + 3H2O т.е. в водном растворе в одной книге говорится, что не существует гидратированных ионов Au3+. Собственно в этом и вопрос. Может ли протекать реакция выше по такой схеме?
-
разумеется. Все карбонаты растворяются в сильных кислотах
-
набухать-набухает, как и все полимеры в растворителях.Но мне кажется, что второй раз его нельзя использовать
-
Уважаемые форумчане, Кто знает, можно ли восстановить силиконовый герметик засохший, залив его растворителем или ещё как-то?
-
Формула гидроксида бария Ba(OH)2 Эта химическая формула отображает структуру молекулы. Видно, что она состоит из 1 атома бария, 2 атомов кислорода и 2 атомов водорода. Если атом обозначить кружочком, то можете нарисовать молекулу эту. Количество молекул Ba(OH)2 вычисляете по формуле N = m*6.02*1023/ M M - молярная (молекулярная) масса Ba(OH)2 . Найдите её сами
-
Преогромнейшее спасибо Только кажется ошибочка. Или я туплю K1 = [H+]1*[H2PO4-]/ [H3PO4] [H+]1 = (K1C)0,5 K2 = [H+]2*[HPO42-]/ [H2PO4-] Но, учитывая, что [H2PO4-] = [H+]1 K2 = [H+]22/ (K1C)0,5 [H+]2= (K2*(K1C)0,5)0,5 Просто [H+]2 = [H2PO4-] такого не может быть, ведь H2PO4- диссоциирует не полностью
-
Вычислил, получилось K1 = [H+]*[PO43-]^4 / [H3PO4]*K3^2*K2 [PO43-] как можно выразить?
-
Помогите плиз, H3PO4 надо вычислить рН, учитывая вторую и третью степени диссоциации. Перечитал литературу, но везде учитывают только первую степень. Как рассчитывается рН многоосновных кислоты, если учитывать 2-ю и даже 3-ю степени
-
в приступе бодуна и отравляются всегда
-
Да и обычно их перемешивают экструдером с добавлением стабилизаторов. Так есть риск, что они окислятся воздухом
-
нет, не получится. Если у вас пластики близкие по составу, то их можно совместить: например, каучук и полиэтилен. Полиэтилен и полипропилен. Но если полистирол с ПВХ или с полиэтиленом, то ерунда будет. Важно подобрать температурный режим
-
Супер, спасибо. Все сошлось. Хотя теоретически там могут любые реакции идти. Например: Na3PO4 + H2SO4 --> NaH2PO4 + Na2SO4 Na2SO4 + H3PO4 Да и Cu3(PO4)2 может реагировать с фосфорной кислотой