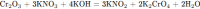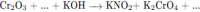-
Постов
84 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Lilian96
-
fe3(so4)2+k2s+h2o=fe(oh)3+k2so4+h2s-почему так неправильно?? а должно быть так fe3(so4)2+k2s=k2so4+s+fes помогите,пожалуйста=)
-
нет)Я отредактировала,в нормальный вид вопрос привела)посмотрите,пожалуйста) то есть ошибка,если я напишу в электронном балансе 1 Сr? просто я слышала,что можно сокращать(делить на 2),но не знаю,правильно так или нет... :bh: :bh: :bh: :bh: :bh:
-
Можно по-другому записать?Помогите,пожалуйста! Cr2O3+KNO3+KOH=KNO2+K2CrO4+H2O Обязательно так писать электронный баланс?? N(+5)+2e=N(+3) 2Cr(+3)-6e=2Cr(+6) нельзя вместо второй строчки записать: Cr(+3)-3e=Cr(+6)??то есть разделить все на 2"??
-
Спасибо!!!!но почему 2 неверно?,ведь образуется соль..
-
спасибо! вот в этом вопросе встретила Верны ли следующие суждения о получении серной кислоты в промышленности? А. Для поглощения оксида серы(VI) используют концентрированную серную кислоту. Б. Для осушения оксида серы(IV) используют гидроксид калия. 1.верно только А 2.верно только Б 3.верны оба суждения 4.оба суждения неверны
-
осушение самого so3
-
Как понимать осушение so3?
-
Почему термин "молекула"не применяется к веществам,имеющим ионное строение?Долго беспокоит этот вопрос...Помогите,пожалуйста)
-
то есть останется непрореагировавшая к-та,которая тоже будет с гидроксидом взаимодействовать.Спасибо!!я поняла
-
Медь массой 6,4 г обработали 100 мл 30%-ной азотной кислоты (ρ = 1,153 г/мл). Для полного связывания продуктов к полученному раствору добавили 200 г раствора гидроксида натрия. Определите массовую долю щелочи в использованном растворе. я составила уравнение реакции.так как азотная к-та разбавленная(30%),то: 6Cu+14HNO3=6CU(NO3)2+2NO+7H20 m(HNO3р-ра)=100*1,153=115,3 m(HNO3)=115,3*0,3=34,59 n(HNO3)=34,59\98=0,353 n(Cu)=6.4\64=0,1,значитбазотная кислота в избытке. Cu(NO3)2+2NaOH=2NaNO3+Cu(OH)2 2n(NAOH)=n(Cu(No3)2)=0,05 m(NaOH)=0,05*40=2 w(NaOH)=2\115,3+6,4-m(NO)+200=0,62%-мой ответ почему ответ мой ответ не правилен?
-
то есть фенол при высокой температуре обесцвечивает перманганат?
-
да..странный.бензол не обесцечиает.а фенол же тоже обесцвечивает перманганат????
-
В какой массе раствора с массовой долей Na2SO4 10 % нужно растворить 200 г Na2SO4 × 10H2O, чтобы получить раствор с массовой долей сульфата натрия 16 %? Какую среду будет иметь полученный раствор. Помогите понять задачу,пожалуйста!
-
Водный раствор перманганата калия изменяет свою окраску под действием : 1.бензола 2.гексана 3.фенола 4.гексена почему ответ только 1?.фенол же тоже реагирует с перманганатом калия.
-
спасибо большое!это не школьное задание.я сама этот список составила,просто интересно=))
-
это из открытого банка ФИПИ взял?я там эти вопросы встретила.
-
В порядке увеличения основных свойств вещества расположены в ряду: 1)СН3NH2, C2H5NH2, C6H5NH2 2)C2H5NH2, СН3NH2, C6H5NH2 3)C6H5NH2, СН3NH2, C2H5NH2 4)C6H5NH2, C2H5NH2, СН3NH2 я думаю,что 3.так ли?помогите,пожалуйста...(
-
Помогите,пожалуйста,расположить в ряд эти соединения в порядке увеличения основных свойств: гидроксид натрия,спирты,метиламин,1-аминопропан,анилин,аммиак,уксусная кислота,глицин,фенол,соляная кислота,