-
Постов
1831 -
Зарегистрирован
-
Посещение
-
Победитель дней
19
Тип контента
Профили
Форумы
События
Сообщения, опубликованные NLVN
-
-
-
Для кротонового чего только там не будет
-
10 баксов
-
CH3-CH=CH-CHO + CH3-CH=CH-CHO ----> CH3-CH=C(-CHO)-CH(OH)-CH=CH-CH3
Сомневаюсь. Скорее так
CH3-CH=CH-CHO + CH3-CH=CH-CHO ----> [ CH3-CH=CН-CH(OH)-СН2-CH=CH-CОH ] ----> CH3-CH=CН-CH=СН-CH=CH-CОH
-
-
Да не может такая смесь уменьшится в объеме. Что то вы путаете или в условии опечатка.
И обратите внимание: плотностей по водороду
А вы что считаете?
А сама задача может быть решена элементарно. Раз объем смеси уменьшился на 25%, значит ее плотность соответственно возросла на 25%. Закон сохранения массы.
Истчо как может. За счет расходования водорода, который присоединяется к изобутилену. В условии, естессно, очепятка. Метилпропен там должен быть.
В этой задаче нет необходимости считать плотность. Достаточно рассчитать отношение средних молярных масс исходной и полученной смеси.
-
-
Есть четвёртое начало - его точную строгую формулировку не помню, но есть и такая: "Вечный двигатель четвёртого рода невозможен"
-
А у вас какие идеи?Теплота образования метана из простых веществ при 25°С равна ∆H=-74,85 Дж/моль. Определите ∆U этой же реакции при той же температуре.
Ответ написан 72,37 кДж/моль
Помогите с решением, потому что никак не могу получить этот ответ. То ли ответ неправильный, то ли условие. Какие у вас идеи?
-
молодой человек, вам понятен термин "обратить"?Есть поговорка: если нельзя, но очень хочется, то можно. Металлический натрий плавится при 98°C. Погружаем в него полиэтилентерефталат и начинаем греть без доступа кислорода. При какой-то температуре ПЭТФ разложится. Но как это будет происходить? Куда уйдёт кислород? Разве тугоплавкий оксид натрия не есть энергетически наиболее выгодное положение для кислорода в таких условиях?
-
Просто щелочи - это хорошо растворимые в воде основания. Помимо щелочных металлов щелочи образуют и щелочноземельные - кальций, стронций, барий, радий.Тут намекают, шо - семантика рулит. Всякая щёлочь - основание, но не всякое основание - щёлочь.
Ну, просто же - щелочами называют гидроксиды щелочных металлов (пардон за каламбурчик)
-
Это было утверждение, а не вопрос.Также как и на любом тюркском наречии-Ёк))
-
Как по-узбекски коротко ответить "Нет".http://www.xumuk.ru/encyklopedia/2/5451.html
Пиролиз эфиров сложных жирных к-т в присут. нек-рых металлов (Mg, Zn) или их оксидов приводит к кетонам:
6046-23.jpg
Бензоаты и оксалаты разлагаются при более низких т-рах в жидкой фазе.
Эфиры сложные устойчивы к действию окислителей. Восстановление эфиров сложных (Na в этаноле, LiAlH4, A1H3 и др.) приводит к альдегидам, но обычно восстановление идет дальше - до первичного спирта:6046-24.jpg Каталитич. гидрирование эфиров сложных в присут. хромата (III) меди при т-ре 200-300 °С и давлении 10-30 МПа - пром. способ получения спиртов. При восстановлении эфиров алифатич. моно- и дикарбоновых к-т Na в кипящем ксилоле образуются ацилоины (см. Ацилоиновая конденсация).
-
О как!!! Не наоборот, случайно?Основания это щелочи.
-
Фотоэлектроколориметр - это частный случай спектрофотометра.
-
-
Реакцию проводят в сильных минусах, там идёт присоединение,кажется, это именная реакция даже. Так что ацетон.
-
Если только подразумевается гидролиз этилацетата. А так ЭА практически не растворим воде, что прочем не мешает воде растворяться в этилацетате.
P.S. Я вот думаю о капельной печи. Проблема в том, что у меня нет навыков слесарных работ.
Не сурово. В наличии металлический натрий, но жаба душит его переводить.
ЭА прекрасно растворим в воде - до 7 % по массе. Если у вас там примесь - хватит 1 раза, проценты - смените воду и еще раз поболтайте
-
Такие задачи, если в задании не заданы дополнительные реактивы, решаются через составление шахматки - каждый приливается к каждому и смотрят эффект. Затем заносят в таблицу и сравнивают с теоретической. Совпадение визуальных эффектов говорит о присутствии в нумерованной пробирке того или иного вещества.
-
Потрясти с водой - уйдет ЭА, уксусная кислота, спирты, если есть. Подсушить солью, а затем ПЭ и тяжелые УВ разгонятся на раз, даже без колонки, просто на дефлегматоре, сантиметров 30, лучше 40.
-
Коллега, константа кислотности сильно зависит от растворителя, поэтому она ни как не может остаться той же.
Кислотность в неводных растворителях - вопрос довольно сложный, люди книжки про это пишут.
Диэлектрическая проницаемость муравьиной кислоты меньше, чем у воды, уже поэтому уксусная кислота в муравьиной будет слабее, а если учесть, что муравьинка - сама нехилый донор протона, то можно предсказать, что уксусная кислота в муравьиной будет очень слабой кислотой.
А какая будет константа - я сомневаюсь, что её можно вот так - взять, и рассчитать, без заморочек.
Полностью согласен. По прочтении вопроса показалось, что речь идет о водном растворе уксусной и муравьиной кислот.
-
Там [Cu(NH3)4]2+ , а не [Cu(NH3)4(H2O)2]2+

КЧ = 4, а не 6

КЧ все-таки 6. Просто из-за эффекта Яна-Теллера у меди наблюдается тетрагональное искажение, из-за чего две из шести связей более длинные, поэтому считают, что КЧ = 4 и комплекс плоскоквадратный. А воду в координационной сфере часто пропускают, например, как в комплекс Na[Al(H2O)2(OH)4] записывают как Na[Al(OH)4].
-
Константы кислотности останутся те же, диссоциация будет протекать тоже без особенностей. Единственный момент - мурашкина кислота сильнее уксусной, поэтому равновесие диссоциации уксусной кислоты будет смещено влево, и степень диссоциации уксусной будет несколько меньше, чем в отсутствие мурашкиной кислоты.
-
Да, ацетон.
Механизм - нуклеофильное присоединение метильного аниона по тройной связи с последующим гидролизом образовавшегося кетимина

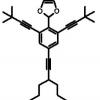
Декарбоксилирование.
в Решение заданий
Опубликовано
Не знаю, как получал его ТС, но можно пропускать сухой HCl через ИПС на холоду. Если вы намекаете на возможную реакцию, то без катализатора типа хлорида цинка и на холоду она будет идти до второго пришествия.