
neutron
-
Постов
105 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные neutron
-
-
какие реакции в водном растворе не идут? и как это объяснить?
1) 16HCl(k)+2KMnO4=5Cl2+2MnCl2+2KCl+8H2O
2) HF+NaI = NaF + HI
3) 2HF + Na2CO3 = 2NaF + CO2 + H2O
-
Реакция пойдет, но... среду укажите для начала!
это был опыт в лабораторной работе: в одну пробирку добавили к осадку гидроксида хрома 3 гидроксид натрия (конц) и перекись(конц), во вторую добавили только перекись. в результате в первой пробирке образовался темно-коричневый раствор и шла бурная реакция, во второй - темно - охристый и реакция шла не очень бурно. что там могло образоваться я не знаю(
-
что получится?
-
правильно ли составлена реакция и как ее уравнять методом полуреакций?спасибо
-
общие константы устойчивости:
[Cd(CN)4]2- = 1.3*10^17
[Ni(CN)4]2- = 1 *10^31
Во сколько раз различается концентрация ионов CN- d 0.1M растворах солей K2[Cd(CN)4 и K2[Ni(CN)4]?
По идее, концентрация ионов [CN-] будет больше у [Ni(CN)4]2- , // По какой это идее у [Ni(CN)4]2- - должно быть больше, если этот комплекс устойчивее?
ну да, я уже просто запуталась, а посчитано все верно?
-
ПР сильно отличаются
Это да, но я не совсем понимаю, какие ПР сравнивать. В первой реакции, например, я должна сравнить ПР(CuS) и ПР([Cu(NH3)4]S), а во второй ПР(Cu(OH)2) и ПР([Cu(NH3)4](OH)2)?
-
общие константы устойчивости:
[Cd(CN)4]2- = 1.3*10^17
[Ni(CN)4]2- = 1 *10^31
Во сколько раз различается концентрация ионов CN- d 0.1M растворах солей K2[Cd(CN)4 и K2[Ni(CN)4]?
По идее, концентрация ионов [CN-] будет больше у [Ni(CN)4]2- , по моим расчетам получается, что у [Cd(CN)4]. Может, я не так считаю?
-
K = Kнест/ПР
как Вы это определили, ее как-то выводят, я не понимаю, как.
-
[Cu(NH3)4]SO4 + Na2S = CuS + NH3 + Na2SO4
[Cu(NH3)4]SO4+KOH=[Cu(NH3)4](OH)2 + K2SO4
Почему в первом случае выпадает осадок, а во втором нет?
-
Тзам=См*Ккр
См=(0,63/106)/150=3,93*10^-5
Тзам=3,93*10^-5*1,86=7,3*10^-5 а куда девать кажущуюся диссоциацию?
Кажущаяся степень диссоциации = 0,69
-
-
Не так, вы ее не уровняли и у меди КЧ=4.
а так, реакция так будет проходить? Только уравнять и координационное число изменить,да?
-
-
какая реакция получится? наверное, медь растворится,да?
-
=> AgCl + NH4NO3
а так не может получиться: AgNO3+NH4Cl+NH3?
И еще я хотела бы спросить, что получится, если смешать NiSO4 + NH4OH(конц)? там должен сначала образовываться какой-то осадок, а потом он растворяется в избытке раствора аммиака, какой осадок здесь должен получиться?
а так не может получиться: AgNO3+NH4Cl+NH3?
И еще я хотела бы спросить, что получится, если смешать NiSO4 + NH4OH(конц)? там должен сначала образовываться какой-то осадок, а потом он растворяется в избытке раствора аммиака, какой осадок здесь должен получиться?
может быть Ni(OH)2?
-
спасибо
-
Я буду указывать все в следующем порядке: Комплексообразователь, его степень окисления, координационное число в комплексном соединении.
1) [Ag(NH3)2]Cl - Ag, +1, 2
2) Na[Co(H2O)2(CN)4)] - Co, +3, 6
3) K2[PtCl4] - Pt, +2, 4
4) [Ni(en)3]Cl2 - Ni, +2, 4 или 3 - не знаю точно
5) [Co(NH3)5(H2O)]Cl3 - Co, +3, 6
6) [Ni(CO)4] - Ni, степень окисления не знаю, как определить, по правилу, получается, что ноль, но че-т падазрительна, координационное число скорее всего = 4.
Укажите на все ошибки, какие найдете и объясните, пункты 4 и 6.Так ли определены заряды комплексных ионов (железо (II), никель(II))?
[Fe(NH3)(CN)5] - +2
[Fe(CN)6] - -4
[Ni(CN)4] - -2
Правильно ли названы следующие координационные соединения?
[Cr(NH3)3(H2O)Br2]NO3 - нитрат дибромоакватриамминохрома(II)
[Pt(NH3)3Cl]Cl - хлорид хлоротриамминоплатины(II)
[Cr(NH3)3(NO2)3] - тринитритотриамминосрома(III)
[Co(NH3)5SO4]NO2 - нитрит сульфатопентаамминокобальта(III)
K4[Fe(CN)6] - гексационоферрат(II) калия
[Pt(NH3)2Cl2] - дихлородиамминоплатины(II)
[Co(NH3)6]Br3 трибром гексаамминокобальта(III)
K[Co(NH3)2(NO2)4] - тетранитритодиамминокобальта(III)
[Co(NH3)3Cl2] - дихлоротриамминокобальта(III)
Правильно ли написаны формулы соединений:
иодид бромопантаамминокобальта(III) - [Co(NH3)5Br]I2дихлоротетранитритоиридат(III) калия - K3[ir(NO2)4Cl2]
Спасибо!
-
-
-
C(FeCl3)=0.1моль/л
Fe3+ + HOH = [FeOH]2+ + H+ - Iстадия
[FeOH]2+ + HOH = [Fe(OH)2]+ +H+ IIстадия
общее уравнение: Fe3+ + 2HOH = [Fe(OH)2]+ + 2H+
Kг=([[Fe(OH)2]+]*[HOH]^2)/([Fe3+]*[HOH]^2)=Kw^2/K([Fe(OH)2]+)
x^3/0.1=10^-28/6.8*10^11
x^3=1,47*10^-41
x=2.45*10^-14
pH=-lg(2.45*10^-14)=13.6
Объясните,пожалуйста,что не так. Спасибо.
-
Да, это я где-то неправильно насоветовал.
Надо
Кг1 = Kw/ Ka2
как определить,когда какую константу брать?
-
-
А какой смысл определять то, что заранее уже написано на этикетке?
Так что это вопрос к преподавателю и лаборантам
спасибо
-
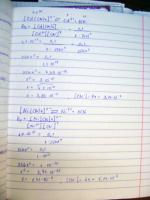
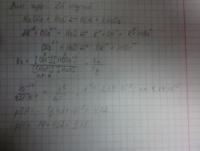
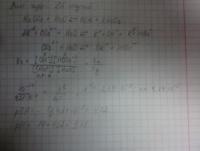
объяснить,какие реакции в водном растворе не идут
в Решение заданий
Опубликовано
поэтому реакция не идет в водном растворе?