amandra
Пользователи-
Постов
14 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент amandra
-
параллельно тема обсуждается на другом форуме
-
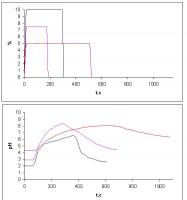
это начальные условия...сначала в баке только кислота присутствует реакция идет когда в бак подется известь подача извести моделируется с помощью блока Repeating Sequance на втором рисунке, то есть мгновенное значение объема, при моделировании задание подаваемого объема представлен на третьем рисунке сверху, там же снизу результирующий pH проблема в том, что результаты моделирования не совпадают с активным экспериментом, рисунок 3 - моделирование. 4 - активный эксперимент
-
на первом рисунке представлена схема нейтрализации на втором - мат модель, что я построил блок 1 - реализцет численное решение ДУ в частных проихводных (см выше), вход - задание концентрации щелочи и кислоты на границе, на выходе - значение концентрации в той же точке блок 2 - он реализует расчет в статике концентрации щелочи, которая получается при перемешивании концентрации, что приходит из бака и той что добавляется через задвижку с учетом объемов, то есть С=(С1*V1+С2*V2)/(V1+V2) блок 5 - задает положение задвкижки, тем самым моделирует подаваемый объем щелочи после второго блока берется разница концентрации щелочи и кислоты и поступает на два блоке - на 3 и 4 блок 3 расчитывает pH по указанной схеме блок 4 анализирует знак концентрации, если >0 то это щелочь и соответсвенно формирует матрицу выхода, если кислота - тож самое на третьем рисунке представлены результаты численного моделирования, подаваемый объем щелочи и pH на выходе насоса на четвертом рисунке приведены результаты численного эксперимента: три раза открывалась задвижка в разные положения, ну и сама реакиция pH в результате моделирования получается неадекватный результат...оссобенно вблизи pH=7...графики расходятся с реальными...динамика другая где может быть ошибка? что я не учел с точки зрения химии?
-
стоит задача построения мат модели процесса нейтрализации, пытался частные вопросы этой задачи на форумах задавать, на какие-то получил ответа, на какие-то нет... в баке объемом 200 м куб (H=6м) собираеются сточные воды, которые содержат H2SO4, CaSO4, MgSO4 (соли кальция и магния в малой концентрации), нейтрализация проводится известковой водой (концентрацию не знаю), pH исходной воды примерно 2-3 бак оснащен трубой рециркуляции длиной примерно 35 метров, на ней установлен рециркуляционный насос, pH-метр pH-011, до насоса врезана труба для подачи известковой воды, подается через поворотную заслонку данные есть только по положению задвижки и показания pH-метра модель бака описал системой ДУ в частных производных, они учитывают распределение концетраций по длине с учетом хим реакции Ca(OH)2 + H2SO4 = CaSO4 + 2 H2O C1(x,t) - концентрация щелочи C2(x,t) - концентрация кислоты dC1(x,t)/dt = D* d^2C1(x,t)/dx^2 - k*C1(x,t)C2(x,t) dC2(x,t)/dt = D* d^2C2(x,t)/dx^2 - k*C1(x,t)C2(x,t) с начальными условиями С1(x,0)=0, С2(x,0)=0.01 с граничными условиями С1(0,t)=f1(t), dС1(x,L)/dx=0 С2(0,t)=f2(t), dС2(x,L)/dx=0 граничные условия слева первого рода, так как непосредственно задается концентрация, справа 2-ого рода - изолирование(потерь нет) в уравнениях D - коэф диффузии k - константа скорости хим реакции pH расчитывается вот как... берется разница концентраций кислоты и щелочи если разница меньше 10^-14 то pH=7 если разница положительна, то преобладает щелоч, то pH = 14+log10(2*C) если разница положительна, то преобладает кислота, то pH = -log10(abs(2*C))
-
спасибо, если предположить, что дойдя до pH-метра не всё прореагировало, то как будет мерить датчик?
-
ошибся, основной электрод - стеклянный, а электрод сравнения - хлорсеребрыный
-
в итоге хочется обобщить для определения pH используется pH-метр фирмы Техноприбор http://www.tehnopribor.ru/pH-meters.htm, для определения используются рН стеклянный электрод и электрод сравнения (каломельный) наобходимо получить зависимости ЭДС от концентраций и pH от ЭДС 1)зависимость ЭДС от концентраций а) исследуемый расствор Ca(OH)2 с концентрацией 0.001М б) исследуемый расствор H2SO4 с концентрацией 0.0003М 2) как влияют малые концентрации солей CaSO4 и MgSO4
-
явно об этом нигде не написано...
-
мне нужно вывести уравнение, ЭДС от концентраций кислоты и/или щелочи, а потом найти зависимость pH от ЭДС
-
я не имел в виду, что что-то влияет на реакцию, мне надо знать как мериит pH сам датчик, если я знаю химический состав жидкости, либо кислая среда, либо щелочная
-
там два элетрода и как же он фиксирует? как вывести эту зависимость?
-
в том и вопрос у меня изменяются во времени концентрации кислоты и щелочи, как мне расчитать ЭДС, если я знаю концентрации? используется pH-011 фирмы "техноприбор"
-
за протеканием процесса нейтрализации следят по показаниям pH-метра
-
здравствуйте процесс нейтрализации кислой среды известковой водой H2SO4 + Ca(OH)2 = CaSO4 + 2 H2O Уравнение Нернста для меня вот что непонятно... под знаком логарифма отношение произведений концентраций продуктов к произведениею концентраций исходных реагентов получается что, в кислой (С(H2SO4) = 0.1 и С(Ca(OH)2) =0.0001) или щелочной (С(H2SO4) = 0.0001 и С(Ca(OH)2) =0.1) среде потенциал будет одинаков как так? что я не учел? спасибо