-
Постов
5859 -
Зарегистрирован
-
Посещение
-
Победитель дней
6
Тип контента
Профили
Форумы
События
Сообщения, опубликованные antabu
-
-
А вот ещё черный юмор от Задорнова, может и не в тему: в цивилизованных странах люди, пока живут, потребляют столько консервантов, что после смерти не разлагаются в гробу десятки лет, а как бы мумифицируются.
-
На форуме зарегистрированы две Ромашки - кириллическая женского полу и латиницей - мужеского.
-
В своё время делал электролизер для получения гремучего газа из молочной бутылки, каковых теперь нет, но вопрос не об этом. Для увеличения проводимости применяют раствор кислоты или щелочи с (близкой к) оптимальной концентрацией как в аккумуляторе. В случае серной кислоты электроды используют свинцовые, ИМХО со щёлочью работать удобнее, электроды можно сделать из никеля, но обычно применяют нержавейку, и никакой пайки, подводящие провода внутри электролизёра из того же материала, что и электроды. Вентильные металлы: титан, цирконий, гафний, ниобий, тантал на постоянном токе не работают - анод пассивируется и тока не пропускает. Вольфрамовый анод в щелочи будет растворяться, а в кислоте пассивируется. Если делать проточный водонагреватель для водопроводной воды на переменном токе, титановые электроды, вроде, допустимы, но не могу сказать, сколько они прослужат.
-
Действительно, из четырёх моих ящиков определился только один.
-
-
http://www.2ip.ru/mail.php показал, что адрес murad139@rambler.ru не существует.
-
Если взять тиосульфат натрия (пятиводный) в запаянной ампуле (я брал фиксанал) и нагреть горячей водой примерно до 50 градусов, соль расплавится в своей кристаллизационной воде. Если при этом не останется ни одного кристаллика, то после охлаждения в ампуле будет вязкая жидкость, сохраняемая в таком виде сколько угодно. Если ампулу вскрыть, начинается кристаллизация с выделением тепла, температура повышается примерно до 50 градусов и довольно долго держится, пока вся соль не закристаллизуется, можно даже греть руки на морозе.
-
В старые добрые времена из технического йода получали реактивный просто: в моногидрат серной кислоты кидали йод, некоторое время перемешивали и возгоняли
ИМХО таким способом от примеси брома не избавиться.
-
Скорее прибор для определения точки Кюри.
-
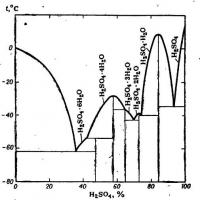
Диаграмму температуры замерзания в зависимости от концентрации можно посмотреть, например, в книжке:
Киргинцев А.Н., Трушникова Л.Н., Лаврентьева В.Г. Растворимость неорганических веществ в воде. Справочник [Химия, 1972] Скачать: http://ihtika.net/?qwe=loginfromfile&z...p;filein=279769 (требуется регистрация).
-
Да, это чьё-то гениальное изобретение.
-
Старят не ртуть, а стекло термометров, а если ртуть размазывается по стеклу - значит туда попал воздух и от такого термометра пора избавляться. Не знаю, была ли тема о демеркуризации.
-
У меня сухой винной кислоте лет 10, а растворимость как у оптически активной формы из сообщения Ромашки, может, это мезоформа?
-
С эмоциональной точки зрения сгорание имени в данной ситуации как-то нелогично. Тут лучше подошла бы какая-нибудь электронная иллюминация.
-
Насыщенный при 25 градусах раствор битартрата калия используют для калибровки pH-метров. Если его растворимость зависит о изомерии, то не всякий изомер на то годится. А если ещё и константы диссоциации различаются, то вообще ерунда получается.
-
Наверное, имя длинное, раз надо читать полторы минуты :D
-
Сушить надо мне, и раньше я это делал в эксикаторе над ангидроном, которого у меня мало. Самое практичное, наверное, над серной к-той, может, кто предложет лучше, только не над основными оксидами/гидроксидами.
А Termoyad, видимо, придётся пожертвовать либо качеством, либо количеством (обычная дилемма при синтезах).
С потерей качества можно предложить такой способ: залить в свободный объём банки раствор едкого натра, выдержать при перемешивании. Образуется раствор иодида и иодата натрия, слить его и добавить к нему раствор серной кислоты - иод выпадет в осадок, отмыть его декантацией. Концентрация щёлочи расчитывается таким образом, чтобы весь иодат был в растворе. Способ основан на диспропорционировании иода.
-
с 50% H2SO4 так и есть.
Примерно в этой области концентрации окислительные потенциалы перекиси водорода и персульфата становятся равными, персульфат аммония в растворе в 50% серной довольно быстро разлагается, при этом ощущается запах озона.
-
У вина бывает осадок, основной компонент которого - битартрат калия.
Винная кислота может быть лево- или правовращающим изомером, или смесью. У меня есть реактив, родная этикетка утрачена, растворимость его значительно выше, чем по справочнику. Отличается ли растворимость у оптических изомеров?
-
-
Иод плавится только под давлением или при резком нагреве. В любом случае он быстро испарится.
Посмотрите в любом справочнике температуры плавления и кипения.
Насчёт "Нахватал воды" - глупость, иод не гигроскопичен, она может попасть, если её туда налить.
Слежался он из-за перекристаллизации.
Есть такая лабораторная работа - регенерация иода из лабораторных остатков, я обычно это делаю обработкой нитритом натрия в кислой среде, при этом иодид окисляется до иода, а если это был иодат - то он восстанавливается нитритом. После отмывки получается порошок иода под слоем воды, так он у меня хранится и не слёживаетя. Так я его и отмеряю - взвешиваю в цилиндре под слоем воды и считаю по Архимеду. А если вдруг понадобится сухой - посоветуйте, как его сушить - в литературе не нашёл.
-
-
А там в капилляре есть стеклянный волосок, действует по системе ниппель... Короче, происходит разрыв столба ртути в заданном месте.
-
Обычные электролиты дают плохую адгезию по нержавейке, для этого существует специальный. Состав есть в любом справочнике по гальванике, кажется такой: соляная кислота 200мл/л хлорид никеля шестиводный 200г/л.
Последовательность такая: обезжиривание - прокипятить деталь в растворе стирального порошка, промыть водой (руками не прикасаться), опустить в электролит и выдержать там час без тока, затем включить ток 10А/дм2 ещё на час, анод - Ni температура - комн. Цифры постараюсь завтра уточнить. Это называется предварительное никелирование, выход потоку мал, и соответственно мала толщина, если надо больше, по этому слою наращивают металл по ссылке из сообщения 3.


Электроды для Электролиза воды.
в Курилка
Опубликовано
Последнее время модным стало использовать блоки питания от старых компов с разной степенью переделки, в Инете по этому вопросу должно быть масса информации.