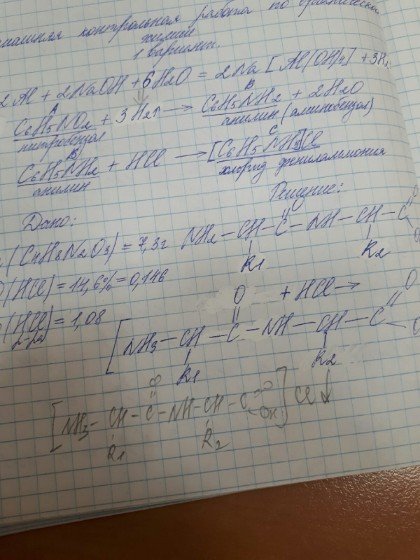themadiz
Пользователи-
Постов
17 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент themadiz
-
Понял, спасибо.
-
Внимание вопрос тем, кто работал в лабах с минеральными удобрениями. У меня методика "определение массовой доли аммонийного азота в минеральных удобрениях хлораминовым методом". Так вышло, что на практику я не попал ( спасибо нашему местному заводу за дистанционную практику ). Вопрос такой, там есть формула массовой доли аммонийного азота: X=((v-v1)*250*0.000467*K*100)/(m*V2) v среднее значение объёма раствора тиосульфата натрия израсходованного на контрольный опыт v1 объём раствора тиосульфата натрия, израсходованный на титрование анализируемого раствора K - поправочный коэффициент. Т.к. делаю фактически мысленный эксперимент, то возьму 1 m - масса навески. По методичке 1-1.5г. Я взял 1.5г V2 объём аликвоты. По методичке 5-10 см3, я взял 10. Такой вопрос: если кто-то выполнял данную работу, не мог бы он поделиться своими расчётами ( ну или хотя бы получившиеся объёмы ). Потому что я хз, если взять объём раствора тиосульфата натрия на КО 20 см3, то на титрование анализируемой пробы потребуется 7.1 см3. Это чтобы массовая доля аммонийного азота вышла 20%. И по мне должно быть наоборот ( ведь в КА нет анализируемой пробы ). В принципе результат не важен и можно взять значения от балды, главное правильно посчитать, но хотелось бы знать, что и как.
-
Текст задачи: некоторое количество серебра растворили в 122,5 мл азотной кислоты с массовой долей кислоты 50% и плотностью 1,44 г/мл. При этом выделилось 8,96 л смеси двух газов с плотностью 1,875 г/л ( н.у. ). Определить массу растворившегося серебра и массовую долю веществ в конечном растворе. Я так понимаю, что в плане газов речь идет о NO2 и NO. Но они выделяются в зависимости от концентрации кислоты. Если конц., то NO2, если разб., то NO. И вот тут я в тупике, т.к. не идет речи о снижении концентрации как в 1 задаче из списка на фото. Первая была решена, во второй я плохо понимаю что делать после нахождения массы кислоты и ее количества вещества. Скажу сразу, мне не нужно полное решение, мне нужно понять, куда двигаться и что и где использовать.
-
Скрин не мой, одногруппница прислала.
-
то есть, я правильно понимаю, что здесь неполный гидролиз в любом случае? Просто у меня в условии сказано, что гидролиз полный, но вы похоже утверждаете обратное. Препод сказала что формула булет такой ( см.скрин, это для гидрохлорида, та, что карандашом сделана ).
-
Я пока мылся увидел ошибку. Про то, что не весь аланин перешёл в гидрохлорид уже догадался. Всё-таки свежая голова лучше работает) Спасибо)
-
В данном случае да, аланин подходит. Но тогда встаёт вопрос, а не должна ли масса аланилаланина быть меньше? Ибо если найти его количество вещества через гидрохлорид, то его молярная масса выходит куда выше, чем по факту. Т.е. если M(гидрохлорид)=111,5 г/моль, то n=6,3г/111,5 г/моль = 0,0565 моль, по реакции 2n(гидрохлорид)=1n(дипептид)=> n(дипептид)=n(гидрохлорид)/2 = > n(дипептид) = 0,0565/2= 0,02825 моль. Однако, M ( дипептид ) = 7,3 г/ 0,02825 моль = 258,4 г/моль, однако молярная масса аланилаланина 160 г/моль. Это я ошибся в расчётах или, возможно, некорректное условие задачи?
-
Я тупой и ещё тупее. Невнимателен. Спасибо. Спасибо. Я просто действительно туповат и невнимателен.
-
Туплю, бывает иногда подобное. Я понял вас и услышал. Однако, у меня появился новый вопрос. Если исходный дипептид - аланин-аланин, то получается формула как на скриншоте, добавляем 1 молекулу воды и 2 молекулы соляной кислоты. Но в таком случае, куда уходит оставшийся водород? Потому что водорода однозначно получается больше, чем в 2 молекулах получившийся соли
-
Азот четырёхвалентен, у него по факту не может быть валентности 5 ( как вы пишете ). Т.е. будет NH3, если я правильно понимаю и знаю химию. Впрочем, ответ от этого не сильно меняется. Спасибо, я кажется понял как это решить.
-
Правильно ли я понимаю, что аланилаланин будет наиболее вероятным дипептидом? И как вы определили это?
-
Небольшой апдейт: мне нужно понять с чего начать, только и всего. Остальное решу сам.
-
Всем здравствуйте. Столкнулся с задачей, а т.к. с дипептидами мы почти не работали, то прошу помощи: При полном гидролизе 7,3 г природного дипептида соляной кислотой ( массовая доля кислоты 14,6%, плотность раствора 1,08 г/см3 ) было получено 6,3 г соли, массовая доля хлора в котором 28,28%. Установите возможную формулу структурную дипептида и вычислите объем кислоты, прореагировавшей с исходным дипептидом. Единственное, что я понял, это то, что дипептид будет состоять из остатков одной и той же аминокислоты, т.к. соль образуется одна, а не две.
-
Добрый день, товарищи химики. Решал я тут лабораторную на то, с чем будет реагировать разбавленная серная кислота. И одним из веществ был Sr(NO3)2 Подумал я и пришел к выводу: реакции в н.у. не будет, т.к. соль, образованная достаточно сильным основанием и кислотой, реагирует с сильной кислотой. Поинтересовался у препода: да, именно так. Перед этим задавая вопрос в комменты в группе ВК получаю ответ: что за бред, реакция будет, т.к. SrSO4 почти аналогичен сульфату бария. Вопрос к действительно знающим людям: будет ли все же реакция, или нет? Верить рандому с группы, преподу или вам? Думаю будет нужным указать, что лабораторная для 1 курса и теоретическая, т.к. мы еще На ДО.