-
Постов
35 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Yung Pull
-
Вот же решал задачу про хлорид серебра. Эта обратная той. BaCO3 -> Ba(2+) + CO3(2-) [Ba(2+)] = [CO3(2-)] = S [Ba(2+)] = S, [CO3(2-)] = S ПР = [Ba(2+)][CO3(2-)] = S2 S = √ПР = 0,0002191 моль/л Р = S * Mr(BaCO3) = 0,0002191 моль/л * 197,34 г/моль = 0,0432 г/л V = 5 л => m(BaCO3) = 0,0432 г/л * 5 л = 0,2162 г
-
а) при рН 12,4 гидроксид магния полностью осаждается, поэтому масса осадка увеличивается б) из-за нейтрализации осадок растворяется, т.е. масса уменьшается
-
12,24,36,48,60,72,84,96 -, Mg, -, Ti, -, -, -, - Э(MgO) = 20 Э(TiO2) = 20 Всегда 20)
- 1 ответ
-
- 1
-

-
Оцените скорость полимеризации винилового мономера при его концентрации 2 М, если Wuнициирования= 3 ∙ 10-8 моль/л∙с. Отношение константы роста цепи на квадратный корень константы обрыва цепи kp/k00,5= 0,2 (л/моль∙с)0.5, если концентрация ингибитора [I] = 0,01 M, а константа переноса цепи на инициатор Cz = 0,1. Ответ должен быть 3,3 ∙ 10-5 моль/л. Решение: Wu = 2∙f∙k1∙[I], откуда k1 = 3∙10-8/2/0,01/f = 1,5∙10-6/f c-1 (вообще принял, что f = 1, т.е. все радикалы образовывались в этой стадии пошли на реакцию роста) Скорость роста цепи Wp = kp∙[M•]∙[M] Скорость обрыва цепи Wo = ko[M•]2 Допустим, что скорость обрыва и инициированя равны, тогда выражаем [M•] и подставляем в уравнение роста. Wр = kp/k00,5 ∙ (2f∙[I]∙k1)0.5∙ [M] И если подставить f = 1 и другие значения то выражение 6,9∙10-5 моль/л, что не совпадает с ответом)
-
Осаждаем соединение гидроксидом натрия. Прокаливаем осадок. Образуется Cr2O3. Его и взвешиваем. m(Cr) = w*m(Cr2O3) w = 2Ar(Cr)/Mr(Cr2O3)
- 4 ответа
-
- 1
-

-
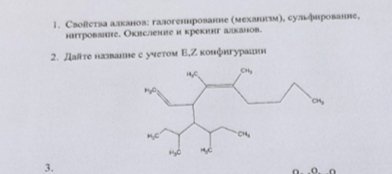
4Z-3-(дивтор-бутилметан)-нонадиен-1,4?
-
Вот, ПР надо сравнить с Кд(H2S) из соображения: сколько и каких ионов нужно для связывания каждого из вещества, можно прийти к этому ПР(CuS) < ПР(H2S) < ПР(FeS) Поэтому образование CuS предпочтительнее образования H2S, а образование FeS менее предпочтительнее образования H2S, поэтому реакция обмена идёт.
-
Чем больше ЭДС, тем предпочтительнее/быстрее реакция.
-
Кг= Kw/KHF/KNH4OH pKг = pKw - pKHF - pKNH4OH pKг = 14 - 3,18 - 4,75 = 6,07 K(1-h) = h2C pK + p(1-h)=2ph + pC pC = -lg0,1 = 1 p(1-h)-2ph = 1 - 6,07 p(1-h)-2ph = -5,07 p(1-h)-ph^2 = -5,07 p[(1-h)/h^2] = -5,07 (1-h)/h^2 = 10^5,07 (1-h)/h^2 = 117489 1-h = 117489h^2 117489h^2 + h - 1 = 0 D = 469 957 h = (-1 + 685,5)/ 2*117489 = 0,00292, 0,292% --------------------------------- Пользуясь упрощённой формулой: Кг= Kw/KHF/KNH4OH pKг = pKw - pKHF - pKNH4OH pKг = 14 - 3,18 - 4,75 = 6,07 Кг = 10^-6,07 = 8,5*10^-7 h = √(Кг/С) = 0,00292, или 0,292%
-
Для газов из соображения уравнения Менделеева-Клапейрона концентрация прямопропорциональна давлению. 2NO + O2 --> 2NO2 v1 = k [NO]^2[O2] v2 = k [NO]^2[O2] v2/v1 = [xNO]^2[xO2]/[NO]^2[O2] = x^2*x = 1000 x^3=1000 x = 10 Т.е. в 10 раз надо давление увеличить.
-
FeS2 + 8H2O - 15e = Fe3++ 2SO42- + 16H+ | 1 NO3-+ 4H+ +3e = NO + 2H2O | 5 FeS2 + 8H2O + 5NO3-+ 20H+ = Fe3++ 2SO42- + 16H+ + 5NO + 10H2O По идее, если поставить эти коэффициенты уравнять не получится. У нас с железом III связано 3 нитрат группы, который получаются из дополнительной реакции. Прибавляем 3 моль HNO3 слева и справа. FeS2 + 8NO3-+ 23H+ = Fe3++ 3NO3- + 2SO42- + 19H+ + 5NO + 2H2O Справа отдаём часть Н+ для 2SO42-, чтобы сделать её нейтральной, т.е. 4Н+, остальные Н(+) вычитаем и слева, и справа, т.е. 15Н(+) FeS2 + 8NO3-+ 8H+ = Fe3++ 3NO3- + 2SO42- + 4H+ + 5NO + 2H2O Отсюда, реакция: FeS2 + 8НNO3 = Fe(NO3)3 + 2Н2SO4 + 5NO + 2H2O

.thumb.png.89d100f6529b6692c4eb9410a3762ef9.png)

.thumb.jpg.de7d1f469aae9abe64344cba14af0a6a.jpg)