Darina001
Пользователи-
Постов
57 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Darina001
-
Написать уравнения реакций по опыту и ответить на вопросы
Darina001 опубликовал тема в Решение заданий
Написать уравнения реакций по данному опыту и ответить на вопросы: поместите в цилиндрическую пробирку небольшое количество оксида марганца(4), добавьте туда же 5-6 капель разбавленной серной кислоты и затем прилейте 2-3 мл раствора пероксида водорода. В отверстие пробирки внесите тлеющую лучинку. Опишите наблюдения. Напишите уравнение реакции. Сделайте вывод о свойствах пероксида водорода. -
Написать уравнения реакций по опыту и ответить на вопросы
Darina001 опубликовал тема в Решение заданий
Кусочек серы поместите в тигель с концентрированной азотной кислотой. Содержимое тигля кипятите в течение 5—7 мин, добавляя новые порции азотной кислоты по мере ее разложения. По охлаждении тигля его содержимое разбавьте водой и, перелив часть его в пробирку, добавьте к нему раствор хлорида бария. Опишите наблюдения. Подействуйте на образовавшийся осадок разбавленной соляной кислотой. Растворяется ли осадок? Дайте объяснение. Напишите уравнения реакций. Используя значения стандартных окислительно-восстановительных потенциалов, дайте обоснование реакции серы с азотной кислотой. -
Написать уравнения реакций по опыту и ответить на вопросы
Darina001 опубликовал тема в Решение заданий
Написать уравнения реакций по данному опыту и ответить на вопросы: поместите в цилиндрическую пробирку небольшое количество оксида марганца(4), добавьте туда же 5-6 капель разбавленной серной кислоты и затем прилейте 2-3 мл раствора пероксида водорода. В отверстие пробирки внесите тлеющую лучинку. Опишите наблюдения. Напишите уравнение реакции. Сделайте вывод о свойствах пероксида водорода. -
Написать уравнения реакций по опыту и ответить на вопросы
Darina001 опубликовал тема в Решение заданий
В две пробирки внесите по 4-5 капель концентрированной серной кислоты. В одну пробирку бросьте 1 кусочек цинка, во вторую-медную стружку и осторожно нагрейте. Исследуйте выделяющийся газ по запаху(осторожно). Напишите уравнения реакций. -
Написать уравнения реакций по опыту и ответить на вопросы
Darina001 опубликовал тема в Решение заданий
Внесите в пробирку 3-4 капли раствора хлорида железа(3), столько же раствора йодида натрия или калия и 1 каплю раствора крахмала. Что наблюдаете? Добавляйте по каплям при перемешивании раствор тиосульфата натрия до обесцвечивания раствора в пробирке. Объясните изменения. Напишите уравнения реакций. Какую роль во второй реакции играет Na2SO3S? -
Написать уравнения реакций по опыту и ответить на вопросы
Darina001 опубликовал тема в Решение заданий
К 3-4 каплям раствора соли алюминия( AlCl3 или Al2(SO4)3) добавьте 3-4 капли раствора сульфида натрия или аммония. Опишите наблюдения. Определите, сульфид или гидроксид алюминия образуется в виде осадка. (Для этого, отделив раствор и промыв осадок водой, подействуйте на него серной или соляной кислотой и испытайте продукты реакции на запах). Напишите уравнение реакции в молекулярной и ионной форме. Дайте термодинамическое обоснование результатов опыта на основе вычисления дельтаG реакций взаимодействия L3+(р) и S2-(р) в водном растворе с возможным образованием Al2S3(к) или Al(OH)3(к). -
Кусочек серы поместите в тигель с концентрированной азотной кислотой. Содержимое тигля кипятите в течение 5—7 мин, добавляя новые порции азотной кислоты по мере ее разложения. По охлаждении тигля его содержимое разбавьте водой и, перелив часть его в пробирку, добавьте к нему раствор хлорида бария. Опишите наблюдения. Подействуйте на образовавшийся осадок разбавленной соляной кислотой. Растворяется ли осадок? Дайте объяснение. Напишите уравнения реакций. Используя значения стандартных окислительно-восстановительных потенциалов, дайте обоснование реакции серы с азотной кислотой.
-
Написать уравнения реакций по данному опыту и ответить на вопросы: поместите в цилиндрическую пробирку небольшое количество оксида марганца(4), добавьте туда же 5-6 капель разбавленной серной кислоты и затем прилейте 2-3 мл раствора пероксида водорода. В отверстие пробирки внесите тлеющую лучинку. Опишите наблюдения. Напишите уравнение реакции. Сделайте вывод о свойствах пероксида водорода.
-
Составьте молекулярное и ионное уравнение: Ca(ClO)2+ CaCl2+ H2SO4->…?
-
Необходимо приготовить 700г раствора H3PO4 с моляльной концентрацией 0,5моль/кгН2О. Какой объем раствора H3PO4 с w(H3PO4)=10,32% и Рр-ра=1,055г/мл и какой объем воды необходимо взять для приготовления раствора?
-
Что будет, при взаимодействии [Ni(NH3)6]SO4 c пикриновой кислотой, помогите, пожалуйста?
-
Почему вы берёте Н3PO4, а не PO4? Только же мое вроде? Ион*
-
Помогите, пожалуйста, составить полуреакции для уравнений: 1)P+ HNO3+ H2O=H3PO4 + NO 2)KMnO4 + K2SO3+H2O=MnO2+ K2SO4+KOH 3)KMnO4+KOH+KCN=K2MnO4+KOCN+H2O
-
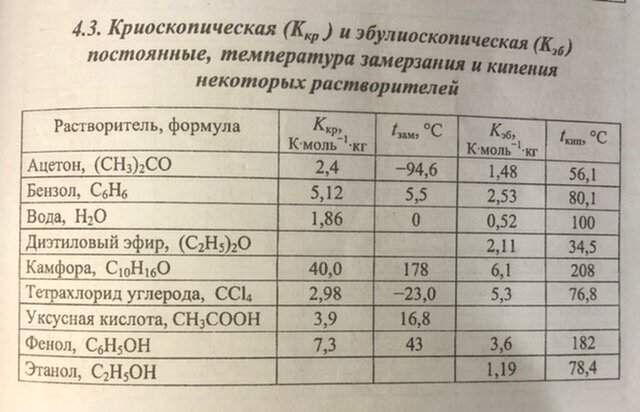
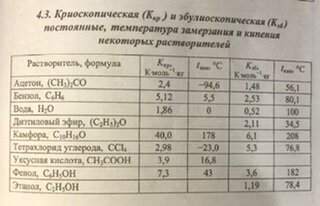
Вычислить молекулярную массу растворенного вещества
Darina001 опубликовал тема в Неорганическая химия
-
Вычислить молекулярную массу растворенного вещества
Darina001 опубликовал тема в Неорганическая химия