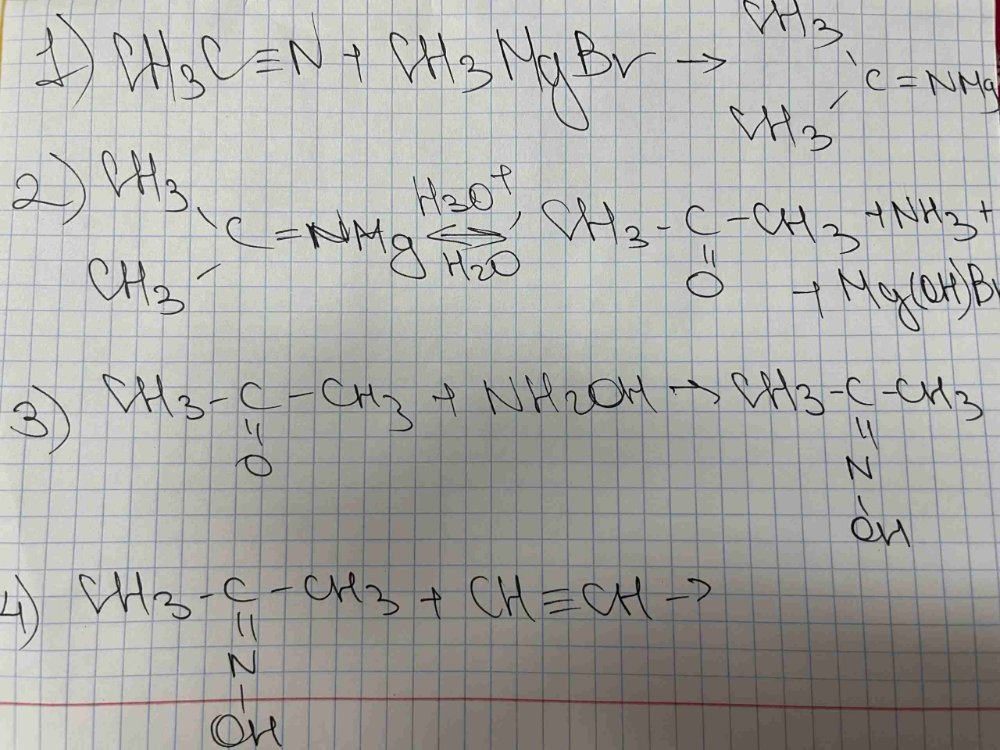katik
Пользователи-
Постов
34 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент katik
-
Всем огромное спасибо!!
-
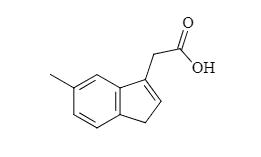
Подскажите, пожалуйста, как можно назвать данное соединение? В каком порядке осуществлять нумерацию атомов? Подразумеваю, что правую часть соединения можно обозвать, как циклопентен-1-ил-этановаякислота, а всё вместе 3-метилбензоциклопентен-1-ил-этановая кислота?
-
Почему растворимость м-фенилендиамина в воде больше, чем у м-нитроанилина? Как эта же растворимость будет увеличиваться/уменьшаться, если у нас будет, допустим, м-фенилендиамин и о-фенилендиамин?
-
Спасибо! Условий действительно не было указано ?
-
Пожалуйста, подскажите, правильно ли осуществлены следующие реакции на фото (интересует в основном 3 стадия). Если да, то какой продукт может получиться в 4 стадии? Никак не могу найти ни в книжках, ни в Интернете взаимодействие оксима пропанона с ацетиленом....
-
Даны исходные вещества, как трихлорметилбензол, который взаимодействует с водным раствором гидроксида калия, получается какое-то вещество А, которое в дальнейшем будет взаимодействовать с гидроксидом кальция. Аналогично с кумолом, который подвергается окислению с получением вещества А. 1) трихлорметилбензол + 3KOH + H2O --> A, 2) кумол + [O] --> A, 3) A + Ca(OH)2 --> B. Вопрос: что же это за вещество А? Сначала думала на бензоат калия, но он вроде как не взаимодействует с гидроксидом кальция, да и получается он путём взаимодействия 4 молей KOH, а не 3, как описано в условии. Может ли тогда на место 3 хлоров в реакции 1) встать 3 гидроксильные группы? Тогда что же за окислители будут в реакции 2)? Помогите, пожалуйста.
-
Всем большое спасибо за помощь!
-
Возможно, там опечатка и подразумевалось 0,025 моль сульфата магния. В этом случае у меня вышел ответ 2,5 мМ, правильно ли?
-
Чему равна жёсткость воды в 10 л которой содержится 0,025 моль/л сульфата магния. Ответ: 5 ммоль/л Ж=(m/Mэкв)*V Молярная масса эквивалентов сульфата магния известна - 0,5*120г/моль=60 г/моль, масса воды = 10л. А как тогда перейти к массе соли? Подумала, что через молярную концентрацию Cм=m/(M*V), но тогда неизвестен объём
-
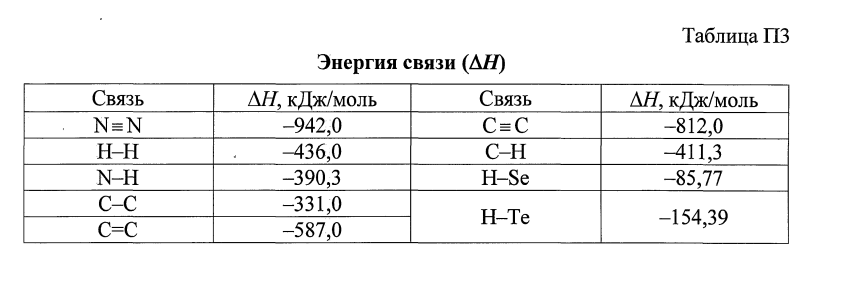
А в таком случае как их правильно рассчитать? Правильно ли я понимаю, что нужно из энергии связей, что легче всего рвутся, вычесть энергию связи, задействованную образовании новой? Тогда как это понять на примере того же ацетилена?
-
Да, меня это тоже смутило. А могло ли подразумеваться, что просили рассчитать энергию связи молекулы ацетилена. В таком случае я тоже не могу прийти к вышенаписанному ответу.
-
Нужно рассчитать энергию сигма-связи молекулы ацетилена, используя справочные данные. В учебнике приведён ответ -245 кДж/моль, но всё никак не могу к нему прийти, подскажите, пожалуйста, ход решения
-
Тогда можно ли у Вас попросить помощи в том, в каком ещё направлении стоит двигаться?
-
Величин в начальном условии и не было (кроме тех, что изначально были указаны), мы предположили, что они будут являться таковыми, исходя из различных табличных данных. Погрешность пипетки на 25 мл - 0,1. С погрешностью титранта уже сложнее, раз в доверительном интервале его среднее 0,10000, то мы просто отбросили нули и отправили 0,1 в формулу для нахождения нормальности соляной кислоты.
-
Сначала найти нормальную концентрацию соляной кислоты: Сн=(0,1*25)/20,68=0,1209, затем по формуле суммарной погрешности S(V)/V=sqrt(0,05/20,68)^2+(0,15/25,00)^2=0,006, где 0,05 - погрешность бюретки, 0,15 - погрешность колбы на 250мл. После наши Sv=0,006*0,1209=0,0007. После - оформили в доверительный интервал (0,1209±0,0007)
-
Рассчитать погрешность определения нормальности HCl, если на титрование 25,00 мл этого раствора пошло 20,68 мл стандартного раствора соды с нормальностью (0,10000±0,00004) мг-экв/л.
-
Всем огромное спасибо!
-
Спасибо, а как можно объяснить, что бензол в данном случае не изолирует CrCl2 от воздуха (до этого встряхивали пробирку с раствором и бензолом)?
-
Почему раствор CrCl2 (в целом любых растворов (II)), изолированный от воздуха бензолом, при стоянии изменяет свою окраску?
-
С твёрдой солью и концентрированной кислотой
-
Спасибо, но при проведении опыта мы как раз брали несколько кристаллов Na2SO3 и концентрированную серную. Не знаю, было ли правдивым моё предположение насчёт того, почему использовали концентрированную кислоту, но почему использовали твёрдую соль, у меня нет как таковых идей
-
Почему для получения SO2 берут концентрированную серную кислоту и твёрдую соль (Na2SO3)? Можно ли кислоту заменить на соляную или азотную? Как я поняла, то у концентрированной серной кислоты сульфат-ион будет действовать как окислитель, он окислит металл и восстановится до SO2. Но тогда почему берут твёрдую соль? Ещё предполагаю, что твёрдая соль, а не раствор соли, потому что реакция с концентрированной серной кислотой не пойдёт? Почему, если так?
-
Почему при взаимодействии FeSO4 c H2S образовался осадок белого цвета, которого в теории быть не должно? Почему именно такая окраска? Разве концентрация ионов S2- у H2S была достаточной для выпадения осадка? Помогите тогда, пожалуйста, проследить разницу на примере с MnSO4+H2S = (реакция не идёт), где раствор так и остался прозрачным (как и в теории), используя ПР и там, и там.