-
Постов
305 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные axeman
-
-
19.31. Рассчитайте минимальный объем раствора гидроксида калия (массовая доля KOH 20%, плотность 1,19 г/мл), который потребуется для полной нейтрализации оксида углерода (IV), выделившегося при сгорании 8,4 л бутана (объем приведен к н.у.)
2C4H10 + 13O2 = 8CO2 + 10H2O
N(C4H10)=8.4/22.4 = 0.375
N(CO2)=N(C4H10)/2*8=1.5
Вариант со средней солью убираем, т.к. спрашивается минимальный объем гидроксида.
KOH+CO2=KHCO3
N(CO2)=1.5
N(KOH)=1.5
m(KOH)=1.5*56=84
m(p KOH)=420
V=m/S=420/1.19=352.941
Проверьте.
-
2CH3I + 2 Na = C2H6 + 2NaI
N(CH3I)=m/M=2.84/142=0.02 - недостаток
N(Na)=0.69/23=0.03 - избыток
N(C2H6 teor)=N(CH3I)/2=0.02/2=0.01
N(C2H6 prakt)=0.1792/22.4=0.008
Выход= N(prakt) / N(teor) = 0.008/0.01 = 0.8 = 80 %
-
СnH2n+1Br
0.65=80/(14n+1+80)
n=3
C3H7Br
-
Может когда сразу на смесь хлорэтана и 1-хлорпропана ?
-
CnH2n+2 + (3n+1)/2O2 = nCO2 + (n+1)H2O
V(CO2)=5.6
N(CO2)=5.6/22.4=0.25
N(CnH2n+2)=0.25/n
M(CnH2n+2)=m/N=3.6/(0.25/n)
12n+2n+2=3.6/(0.25/n)
n=5
C5H12 + 8O2 = 5CO2 + 6H2O
N(O2)=N(CO2)/5*8=0.25/5*8=0.4
V(O2)=0.4*22.4=8.96
-
1.
2C2H5Cl + 2Na = C4H10 + 2NaCl
2.
2C3H7Cl + 2Na = C6H14 + 2NaCl
-
Хм, наши учителя заказали нам (выпускникам 11-ых ) - мартини и конфеты. Как вам такая идея ?
-
Помогите пожалуйста написать графическую формулу дигидрофосфата магния.
-
Cr2(SO4)3 + 3Na2CO3 + 3H2O = 2Cr(OH)3 + 3CO2 + 3Na2SO4
2Cr3+ + 3SO42- + 6Na+ +3CO32- + 3H2O = 2Cr(OH)3 + 3CO2 + 6Na+ + 3SO42-
2Cr3+ +3CO32- + 3H2O = 2Cr(OH)3 + 3CO2
-
-
CnH2n + HBr = CnH2n+1Br
m(CnH2n)=16.8 г
V(HBr)=6.72 л
N(HBr)=6.72/22.4=0.3
N(CnH2n)=0.3
M(CnH2n)=m/N=16.8/0.3=56
12n+2n=56
14n=56
n=4
-
Na2SO3+ KMnO4+ H2O = Na2SO4+ MnO2 + KOH
2|MnO4- + 2H2O + 3e = MnO2 + 4OH-
3|SO32- + 2OH- -2e = SO42- + H2O
2MnO4- + 4H2O + 3SO32- + 6OH- = 2MnO2 + 8OH- + 3SO42- + 3H2O
3Na2SO3+ 2KMnO4+ H2O = 3Na2SO4+ 2MnO2 + 2KOH
-
Na2SO3+H2SO4+KMnO4=Na2SO4+MnSO4+H2O+K2SO4
2|MnO4− + 8H+ + 5e = Mn2+ + 4H2O
5|SO32− + H2O − 2e = SO42− + 2H+
2MnO4− + 6H+ + 5SO32− = 2Mn2+ + 3H2O + 5SO42−
5Na2SO3+3H2SO4+2KMnO4=5Na2SO4+2MnSO4+3H2O+K2SO4
K Mn O4+ KOH+NaSO3= K2MnO4+H2 -
-
3363. Какой объем 15,2%-го раствора гидроксида калия (пл. 1,14 г/мл) потребуется для гидролиза смеси этилового эфира аминоуксусной кислоты и эфира, образованного аминоэтанолом и уксусной кислотой, если известно, что число атомов кислорода в этой смеси равно 3,07*1023 ?
Проверьте пожалуйста реакции :


-
Большое спасибо.
И как я понял :
HNO3 (k) + ... = NO2
HNO3 (p) + ... = NO2 или NO или N2O
Так ?
-
И еще, такие реакции возможны :
K2Cr2O7 + H2SO4 + NaF = F2 + Na2SO4 + Cr2(SO4)3 + H2O + K2SO4
K2Cr2O7 + H2SO4 + RbOH = Cr(OH)3 + Rb2SO4 + K2SO4 + H2O
-
-
-
Рассчитайте массу алкоголята натрия, полученного при взаимодействии металлического натрия массой 4,6г с абсолютным (безводным) этанолом объемом 40 мл (плотность 0,79 г/мл).
2Na+2C2H5OH → 2C2H5O-Na+H2
m(Na)=4.6
N(Na)=4.6/23 = 0.2 - недостаток
V(C2H5OH)=40
S(C2H5OH)=0.79
m(C2H5OH)=40*0.78=31.6
N(C2H5OH)=31.6/46=0.686 - избыток
N(C2H5ONa)=N(Na)=0.2
m(C2H5ONa)=0.2*68 = 13.8
-
-
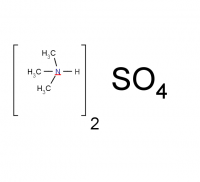
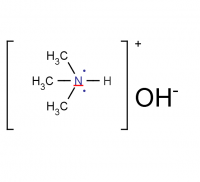
(CH3)3NHOH + Al2(SO4)3 = ((CH3)3N)2SO4 + Al(OH)3
Так ?
-
(CH3)3N + H2O = (CH3)3NHOH
6(CH3)3NHOH + Al2(SO4)3 = 3((CH3)3N)2SO4 + 2Al + 6H2O
Как то так ?
-
Извиняюсь за лень перепечатывать задание. Но реакции все равно не будет ?
3244
Какой объем триметиламина (нормальное давление, 25С) следует пропустить через 20,0г 17,1%-го раствора сульфата алюминия для полного осаждения ионов алюминия.





Алканы
в Решение заданий
Опубликовано
C2H5OH = C2H4 + H2O
N(C2H5OH)=(300-(300*0.08)) / 46 = 6
N(C2H4)= 6
V(C2H4) = 6 *22.4 = 134.4