-
Постов
305 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные axeman
-
-
23.10. В результате спиртового брожения глюкозы получили этанол, который окислили до кислоты. При действии избытка гидрокарбоната калия на всю полученную кислоту выделился газ объемом 8,96 л (нормальные условия). Определите массу глюкозы, подвергнутую брожению. Ответ: 36 г.
C6H12O6 = 2 C2H5OH + 2 CO2
C2H5OH + 2Cu(OH)2 = CH3COOH + Cu2O + 2H2O
CH3COOH + KHCO3 = CO2 + CH3COOK + H2O
V(CO2)=8.96
N(CO2=0.4
N(CH3COOH)=0.4
N(C2H5OH)=0.4
N(C6H12O6)=0.2
m(C6H12O6)=0.2*184=36.8 г
-
 1
1
-
-
Нет, соль уксусной кислоты и вода не будет получаться. А даже если и будут, то должно быть еще что-то. Ведь сказано, что газ будет.
-
23.10. В результате спиртового брожения глюкозы получили этанол, который окислили до кислоты. При действии избытка гидрокарбоната калия на всю полученную кислоту выделился газ объемом 8,96 л (нормальные условия). Определите массу глюкозы, подвергнутую брожению. Ответ: 36 г.
C6H12O = 2 C2H5OH + 2 CO2
C2H5OH + CuO = CH3CHO + Cu + H2O
CH3CHO + KHCO3 = CO2 + ...- ?
Что тут еще будет ?
-
C6H10O5 + H2O = C6H12O6
m(C6H10O5)= 8.1 г
N(C6H10O5)=8.1 / 162 = 0.05 моль
N(teor C6H12O6)= 0.05 моль
Выход реакции = 70 %
N(prak C6H12O6)=0.05 / 0.7 = 0.035 моль
С6H12O6 + Ag2O = C6H12O7 + 2Ag
N(prak C6H12O6)= 0.035 моль
N(Ag)=N(C6H12O6)=0.035/1*2=0.7 моль
m(Ag)=0.7 * 108 = 7.56 г
-
23.11. При спиртовом брожении глюкозы получен газ, который прореагировал с раствором гидроксида натрия объемом 60,2 мл и плотностью 1,33 г/мл, образовав среднюю соль. Массовая доля гидроксида натрия в этом растворе равна 30%. Какая масса раствора с массовой долей этанола 60% получена при этом? Ответ: 23 г.
C6H12O = 2 C2H5OH + 2 CO2
2 NaOH + CO2 = Na2CO3+H2O
V(NaOH)=60.2 мл
S(NaOH)=1.33 г/мл
m(p NaOH)=60.2 * 1,33 = 80 г
w(NaOH)=0.3
m(NaOH)=80 * 0.3 = 24 г
N(NaOH)=24/40= 0.6 моль
N(CO2)=N(NaOH)/2=0.3 моль
Возвращаемся к первой реакции
C6H12O = 2 C2H5OH + 2 CO2
N(CO2)=N(NaOH)/2=0.3 моль
N(C2H5OH)=N(CO2)/2*2=0.3 моль
m(C2H5OH)=0.3 * 46 = 13.832 г
w(C2H5OH)=0.6
m(p C2H5OH)= 13.832 / 0.6 = 23.05 г
-
----
2CH3CHO = CH3COOC2H5 - возможно ?
-
Имея 2-бром-3-иодбутан, алюминий, воду, гидроксид натрия и необходимые катализаторы, получите, не прибегая к крекингу, метан.
H3C-CH(Br)-CH(I)-CH3 + 2NaOH = H3C-CH(OH)-CH(OH)-CH3 + NaBr + NaI
2NaBr(расплав) = ток = 2Na + Br2
H3C-CH(OH)-CH(OH)-CH3 + 2Na = H3C-CH(ONa)-CH(ONa)-CH3 + H2
2H3C-CH(ONa)-CH(ONa)-CH3 + 2NaOH + 5H2O = 11CH4 + 5Na2CO3
Проверьте пожалуйста.
-
-
Имея 2-бром-3-иодбутан, алюминий, воду, гидроксид натрия и необходимые катализаторы, получите, не прибегая к крекингу, метан.
Получил пока водород, гидроксид алюминия, комплексную соль, бромид натрия, иодид натрия, спирт двух атомный
Дайте пожалуйста подсказку
-
Хорошо, спасибо, всё получилось.
-
Спасибо.
Если реакции с бензолом не будет, то вообще реакции не будет, или будет радикальное галогенирование ?
-
Бензольный раствор, содержащий линоленовую кислоты массой 5,60г, обработали иодом массой 12,7. Вычислите массу иод производного.
С бензолом - простое галогенирование. А дальше, проблема, проверьте пожалуйста
-
Из уксусного альдегида нужно получить бутан.
Мой вариант: альдегид -> карбоновая кислота -> метан -> вюрца -> галогенирование -> вюрца -> бутан
Есть более простые варианты ?
-
-
... --H2O-> ... --O2--> метаналь <--O2-- ... <--H2-- ...
Метаналь тут, в обоих случаях, будет получаться из спирта ?
-
А, спасибо FilIgor.
-
-
Опыт 2
3Na2SO3+4H2SO4+K2Cr2O7=3Na2SO4+Cr2(SO4)3+4H2O+K2SO4
-
-
Хорошо, спасибо, решилось.
-------------
2456. Раствор о-крезола в этилен гликоле общей массой 61,2 г обработали избытком калия, в результате чего выделилось 20,7 л (н.у.) газа. Вычислите массовую долю о-крезола в исходном растворе.
Проверьте пожалуйста реакции, а то что-то составляю систему, получаю как обычно отрицательный результат..
-
Так будет реакция присоединения или нет ?
-
2460 При действие на раствор фенола в бензоле избытком брома в отсутствие катализаторов выпало 99,3 г осадка. При сгорание такой же смеси выделилось 67,2 л углекислого газа (н.у.). Вычислите массовые доли веществ в исходном растворе.
Первая реакция понятно, фенол + бром = 2,4,6 трибромфенол + hbr, а вот вторая реакция,
С6H6 + Br2 = C6H5Br + Hbr - ну она не возможно, потому что сказано что в "отсутствие катализаторов". Тогда что, будет гексахлорциклогексан ?
-
Я извиняюсь, но еще раз Up.
Это такое простое задание где нужно просто подумать или оно действительно сложное ?

-




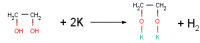

Цепочка превращения по алюминию
в Решение заданий
Опубликовано
Из муравьиной кислоты нужно получить уксусную кислоту, и не использовать другие углерод содержащие средства.
У меня, получилось вот так
1. HCOOH = CO + H2O
2. CO + 3H2 = CH4 + H2O
3. CH4+Cl2=CH3Cl + HCl
4. 2CH3Cl + 2Na = C2H6 + 2NaCl
5. C2H6 + Cl2 = C2H5Cl + HCl
6. 2C2H5Cl + 2Na = C4H10 + 2NaCl
7. C4H10 + 5O2 = 4CH3COOH + CO2
Есть более разумные способы ?