-
Постов
196 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Georg
-
-
Эпоксидные смолы типа ЭП-20 с аминным отвердителем (Полиэтиленполиамин или ОП-300) в разы быстрее отверждаются при наличии излучения, близкого к УФ-области.
-
......А насчет параболического зеркала дома никак не сделаешь, только на заводе, там же надо выдерживать отклонение формы до 1 мкм.
В какой-то книжке по астрономии читал, что делали, шлифуя лист стекла пастой ГОИ, пока параболу не получишь.
Я не понаслышке знаю сколько придется пырхаться чтобы получить нужную кривизну. Мой однокашник как-то разбил зеркало у телескопа. В итоге год вышаркивал и выравнивал разными абразивами а результата при мне так и не достиг.
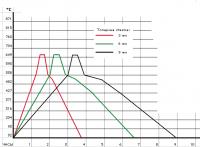
Есть гораздо более простой способ - МОЛИРОВАНИЕ стекла. Берешь лист, ложешь его на сферическую форму и в печь. Вот ориентировочный режим термообработки для оконного стекла (5мм).
-
-
Да можно, но зачем эту воду испарять? Ведь на единицу конечного продукта придется затратить колосальное кол-во энергии. Поэтому обычно сразу проводят электролиз. Ведь известно, что при нём, улетающий водород и кислород обеднены своими более тяжелыми изотопами.
Таким вот образом из 20 л воды, в несколько сложных этапов, можно получить 0,5 мл воды с плотностью 1,075, содержащей уже 65,7% D2O.
Тяжелая вода кипит при 101,44° С, замерзает при 3,82° С, имеет плотность при 20° С 1,10539 г/см3, причем максимум плотности приходится не на 4° С, как у обычной воды, а на 11,2° С (1,10602 г/см3). Кристаллы D2O имеют такую же структуру, как и обычный лед, но они более тяжелые (0,982 г/см3 при 0°С по сравнению с 0,917 г/см3 для обычного льда). В смесях с обычной водой с большой скоростью происходит изотопный обмен: Н2О + D2O=2HDO. Поэтому в разбавленных растворах атомы дейтерия присутствуют в основном в виде HDO.
Собственно , используя эти свойства и производят дальнейшее разделение.
Есть еще некоторые оригинальные способы разделения (фотостимулированно-адсорбционные), но о внедрении их на промышленно-широкую ногу не слышал пока, т.к. они "совсем свежей выпечки" .
-
SnCl4- где достать? или сделать
Можно так, но без солянки в этом случае ваще никак:
CuCl2+SnCl2=Cuосадок+SnCl4
1.Раствори хлорид меди в минимальном количестве воды и прилей дымящей солянки столько же сколько и воды,
2. дихлорид олова раствори в дымящей солянке в отдельной склянке.
3. приливай хлорид олова к хлориду меди. Должен выпадать осадок металлической меди.
4. раствор хлорида олова - жутко дымящая дрянь, крайне склонен к гидролизу. Осторожнее, работай под тягой!!!!!!!
-
А кстати та же проблема и с комплексными солями (гидроксо-хлоридами ) цинка.
Самое интересное, что точно установить строение этих молекул оч трудно и классические методы растворения , блин, не действенны.
Но если для растворения цинкатов рекомендуется кипячение в крепкой серной кислоте, то на гидроксо-хлорид-алюминаты мне реагент-растворитель не известен.
Legus, вы похоже гальванщик и у вас проблемы с ванной анодного оксидирования?
-
-
А чем вас , скажем, не устраивает электро- (или хим-)полировка готового штампа?
См. ГОСТ 9.305-84, там есть карта №21. Это готовый рецепт решения вашей проблемы.
Задайте в яндексе "скачать бесплатно ГОСТ 9.305-84" и дело в шляпе!
-
-
Спасибо большое. Но если детали лежат друг на друге или в месте соприкосновения с корзинкой травление будет неоднородным, и, потом, на это уйдет много кислоты. Скорость травления вроде как нормальная, острые углы детали не скругляются, если рассматривать невооруженным взглядом, правда я перешла на раствор 1:4, с тех пор.
Наоборот, травление однородное, но при условии полного погружения деталей в раствор. Необходимо встряхивание. Кислоты уйдет не много, один раз разведете и надолго. Данный раствор как раз и отличается невысокой скоростью травления (но при условии что температура его не поднимется более 45-50град С, что бывает только при больтшой площади травящейся поверхности и малом объеме). Раствор всегда держите плотно закрытым, это не даст улетать азотке в атмосферу.
-
Я травлю большое количество медных деталей в растворе азотной кислоты 1:3. При этом т.к. деталей много, в целях экономии кислоты, заливаю раствором детали в банке, закрываю ее и трясу. Сливаю кислоту, когда раствор начинает нагреваться и синеть, ну и дым там начинает выделяться (работаю в вытяжном шкафу). Затем прмываю детали в водопроводной воде. Проблема в том, что мне не удается смыть кислоту окончательно, на воздухе появляются разводы на детали, которые как я понимаю являются окислами меди, и от которых я хотела избавиться. Деталь нужна для герметизации пайкой, а к окисленным частям припой олово- свинец не пристает. Деталей много - тереть каждую в отдельности нет возможности. Хорошо получалось промыть если в той же банке трясти детали и менять воду, но от этого детали несколько портятся - от трения друг о друга. Подскажите пожалуйста варианты решения проблемы! Может поможет ацетон при промывке?
Евгения, приведенная вами тема не проблема.
1. Отставьте банку, сделайте корзинку из нерж. или полимерной сеточки. Использование корзинки дает стократно-лучшее промывание чем бы то нибыло. Подготовьте емкость для обезжиривания - пластмасс. ванну, пластик.ведро или подобное тому залейте в нее нефрас, бензин-галоша или ацетон (лучше ацетон или спирт).
2. Далее возмите еще одно ведро, в нем приготовте раствор глянцевого травления Азотная к-та/серная к-та = 1/1 (объемное отношение).
азотка уд. вес 1,38-1,4 г/мл, серная уд. вес 1,83 г/мл.
3. пластиковое ведро с теплой водой для промывки.
порядок:
1. Обезжирить органикой маканием 1-2 мин.
2. просушить феном или обдувом воздуха
3. макнуть на 5-10 сек в р-р глянцевого травления
быстро ватащить и промыть в теплой воде, затем тщательно под холодной проточной.
4. затем сушка теплым воздухом
Кач-во 100%. Сами такое ежедневно делаем - сотни деталей. Этот же способ и для латуней, а для бронз не рекомендую. Там другой состав.
Я травлю большое количество медных деталей в растворе азотной кислоты 1:3.Ну это уж слишком беспощадно. Там наверное скорость травления около 0,5мм/мин?
-
Смотря для каких целей переводите в водн. рас-р.
Может полезное почерпнете тут: http://planetadisser.com/see/dis_162914.html
-
есть всё тут в свободном доступе:
нехудлит. ру
гальваникворд. ру
инженер.ру
ихтика. ру
Вам нужна книга "Гальванические покрытия в машиностроении", там она есть в халявном скачивании. Да и не только она.
-
1. Естественно в том, что при уменьшении концентрации дисперсных частиц, уменьшится скорость коагуляции(как впрочем для любой хим. реакции). Для достижения той же скорости коагуляции что и при не разбавленном р-ре необходимо будет нагреть ваш V.
2. При разбавлении может изменится рН раствора, что может привести как к увеличению, так и к уменьшению скорости коаг-ии. В данном случае всё будет зависить от строения мицеллы.
3. Необходимо смотреть, какая теплота выделится или поглотится при разбавлении коллоида. Ее количество немаловажно, т.к. тоже ведет как к уменьшению так и к увеличению скорости коаг-ии. Но в основном к увеличению.
-
-
Уважаемые, химики! Помогите пожалуйста! Я совсем запуталась. Давно уже закончила школу, и кое-что забыла. Недавно умер один знаменитый певец (знаменитый в определенных кругах), и после того, как была проведена суд.-мед. экспертиза, установили, что он умер от этанола, написали "умер от нехватки воздуха, попросту задохнулся". Как можно задохнуться этанолом? Объясните пожалуйста, если кто-то сможет. Заранее благодарю.
Этанол - это обычный спирт, водка - это его 40% раствор в воде. Пить надо меньше!
-
Мой совет как можно быстрее вытащить манганат из раствора, т.к. в водной среде шестивалентный марганец крайне склонен к диспропорционированию (распад на 4х и 7и валентный одновременно).
Да, манганат в сухом состоянии тоже к этому склонен, но насухую скорость распада его в сотни и тысячи раз меньше чем в растворе. Нагрев сухого тоже приведет к его распаду.Манганат имеет темно-зел кристаллы.
-
В данном случае очень важна стехиометрия(особенно кол-во щелечи) и постоянство температуры кипячения раствора. Наличие осадка (это 100% MnO2) - это следствие нарушения этих 2-х параметров. При перегреве и недостатке щелочи манганат распадается на перманганат и двуокись марганца.
К сожалению нет практикума по неорг. синтезу под рукой, по скольку в инет выхожу с работы. кол-ва перманганата и щелочи уже не помню, т.к. такой опыт ставил давно - на 1 курсе, а было это в 2000г.
-
еще проще так:
Ни какой перекиси не надо.Кипяти раствор перманганата с избытком калиевой щелочи пока не преобретет красивый зеленый цвет, после полного изменения окраски еще кипяти 10 мин. потом фильтруй на стеклянном(!!!) фильтре - бумажный сгорит. промывай горячей а затем холодной дистил. водой. суши. И готово!
-
Получают гидролизом алкосиланов. Структуры мицелл и как следствие устойчивость зависят от рН гидролиза, температуры, скорости перемешивания (т.к. реакция гетерогенная), от чистоты исх. продуктов. Но полученные коллоиды не содержат более 22% окиси кремния. Далее необходимы операции концентрирования.
Полученные коллоиды при таких концентрациях как указано выше (30-40%) не сильно-то и устойчивы. На своем опыте скажу, что не более месяца, только в полимерных емкостях (фторопласт, полистирол).
Если что звоните 9090785707.


Способы снижения мутности пластовой воды
в Коллоидная химия
Опубликовано
А вода проточная или стоячая?
Какие основные частицы мути?